工业上用MnO2和KOH为原料制取高锰酸钾,主要生产过程分两步进行:第一步将 MnO2 和固体 KOH 粉碎,混合均匀,在空气中加热至熔化,并连续搅拌,制取 K2MnO4;第二步将 K2MnO4 的浓溶液进行电解,制取 KMnO4。试回答以下问题:
(1)写出第一步的反应方程式_______ ;连续搅拌的目的是_______ ;
(2)电解 K2MnO4 的浓溶液时,两极发生的电极反应式:阴极是_______ , 阳极是_______ ,电解总的反应方程式是_______ 。
(1)写出第一步的反应方程式
(2)电解 K2MnO4 的浓溶液时,两极发生的电极反应式:阴极是
更新时间:2021/02/11 19:56:39
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】氯酸钾和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯。
(1) 2KClO3+4HCl(浓) = 2KCl+2ClO2↑+Cl2↑+2H2O
浓盐酸在反应中显示出来的性质是___________ (填序号)
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)若反应中生成标准状况下13.44 L气体,则消耗还原剂的物质的量为___________ 。ClO2具有很强的氧化性,常用作消毒剂,其消毒的效率(以单位物质的量得到的电子数表示)是H2O2的___________ 倍。
(3)过氧化钙也是一种优良消毒剂,供氧剂。通常情况下用CaCl2在稀氨水条件下与H2O2反应得到CaO2·8H2O沉淀,请写出该反应的化学方程式:___________ 。
(4)取2.76 g CaO2·8H2O样品受热脱水过程的热重曲线(140 ℃时完全脱水,杂质受热不分解)如图所示。
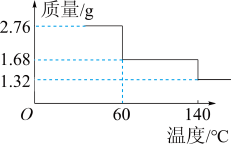
试确定60 ℃时CaO2·xH2O中x=___________ 。
(5)该样品中CaO2的质量分数为___________ 。(保留一位小数)
(1) 2KClO3+4HCl(浓) = 2KCl+2ClO2↑+Cl2↑+2H2O
浓盐酸在反应中显示出来的性质是
A.只有还原性 B.还原性和酸性 C.只有氧化性 D.氧化性和酸性
(2)若反应中生成标准状况下13.44 L气体,则消耗还原剂的物质的量为
(3)过氧化钙也是一种优良消毒剂,供氧剂。通常情况下用CaCl2在稀氨水条件下与H2O2反应得到CaO2·8H2O沉淀,请写出该反应的化学方程式:
(4)取2.76 g CaO2·8H2O样品受热脱水过程的热重曲线(140 ℃时完全脱水,杂质受热不分解)如图所示。

试确定60 ℃时CaO2·xH2O中x=
(5)该样品中CaO2的质量分数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】填写下列空白:
(1)34g NH3共有__________ mol原子,0.1molH2S共约 有_____ 个氢原子。同温同压下,等体积的NH3和H2S气体的质量比为____________ 。等质量的NH3和H2S中分子数目之比为_________ 。
(2)在标准状况下,35.5g Cl2的体积约是_________ L,将其与足量氢气完全化合生成氯化氢气体溶于1000 g水中,得到密度为a g·cm-3的盐酸,则该盐酸的物质的量浓度是_____ mol/L。
(3)欲配制500mL 0.2mol/L Na2CO3溶液,需要用天平称量Na2CO3·10H2O晶体质量为_____ 。若从配好的上述溶液中取出50mL于一试剂瓶中,需要给它贴上标签,标签上的内容是_____ ;若再从中取出10mL溶液加水稀释至20mL,则此溶液中Na+的物质的量浓度为_____ 。
(4)过氧化氢H2O2,(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~F涉及H2O2的反应,回答相关问题:
A.Na2O2 +2HCl= 2NaCl+H2O2 B.Ag2O+ H2O2=2Ag+O2↑+ H2O
C.2 H2O2=2 H2O+O2↑ D.3 H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8 H2O
E.H2O2+MnSO4 = MnO2 + H2SO4 F.H2O2+ Fe2+ + H+ == Fe3+ + H2O
①H2O2仅体现还原性的反应是_____ (填代号)。
②上述反应说明H2O2、Ag2O、K2CrO4氧化性由强到弱的顺序是:_____ 。
③请配平化学反应F,并画出电子转移情况_____ 。
H2O2+ Fe2+ + H+== Fe3++ H2O
(1)34g NH3共有
(2)在标准状况下,35.5g Cl2的体积约是
(3)欲配制500mL 0.2mol/L Na2CO3溶液,需要用天平称量Na2CO3·10H2O晶体质量为
(4)过氧化氢H2O2,(氧的化合价为-1价),俗名双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。对于下列A~F涉及H2O2的反应,回答相关问题:
A.Na2O2 +2HCl= 2NaCl+H2O2 B.Ag2O+ H2O2=2Ag+O2↑+ H2O
C.2 H2O2=2 H2O+O2↑ D.3 H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8 H2O
E.H2O2+MnSO4 = MnO2 + H2SO4 F.H2O2+ Fe2+ + H+ == Fe3+ + H2O
①H2O2仅体现还原性的反应是
②上述反应说明H2O2、Ag2O、K2CrO4氧化性由强到弱的顺序是:
③请配平化学反应F,并画出电子转移情况
H2O2+ Fe2+ + H+== Fe3++ H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】纯过氧化氢(H2O2,俗称双氧水)是淡蓝色的粘稠液体,可任意比例与水混溶。双氧水在医疗以及生产、生活中有广泛的应用。请分析在下列反应中,H2O2的作用(填写“氧化剂”或“还原剂”),并用单线桥标出反应过程中电子转移方向和数目。
(1)双氧水在氧化剂的作用下,可定量地产生O2,这在分析化学中,具有重要的意义。
___________ 。反应中,H2O2在反应中的作用是___________ 。
(2)双氧水曾在文艺复兴时期的油画修复中发挥很大的作用。其中发生的反应是:
___________ 。反应中,H2O2在反应中的作用是___________ 。
(3)稀释以后的双氧水常用于医疗中的杀菌消毒,使用过程中可见有气体产生,涉及到的反应有:
___________ 。H2O2在反应中的作用是___________ 。
(4)将双氧水滴加到FeCl3溶液中,也会产生有趣的现象。
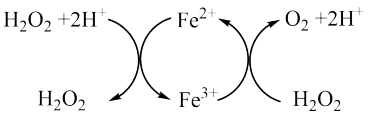
虽说H2O2可以将Fe2+氧化为Fe3+,可是反应中依然有气体生成。研究表明,在此主要涉及到Fe2+、Fe3+和H2O2发生的循环反应(如图)。请根据图示,写出两个相应反应的离子方程式。___________ 、___________
(1)双氧水在氧化剂的作用下,可定量地产生O2,这在分析化学中,具有重要的意义。

(2)双氧水曾在文艺复兴时期的油画修复中发挥很大的作用。其中发生的反应是:

(3)稀释以后的双氧水常用于医疗中的杀菌消毒,使用过程中可见有气体产生,涉及到的反应有:

(4)将双氧水滴加到FeCl3溶液中,也会产生有趣的现象。
虽说H2O2可以将Fe2+氧化为Fe3+,可是反应中依然有气体生成。研究表明,在此主要涉及到Fe2+、Fe3+和H2O2发生的循环反应(如图)。请根据图示,写出两个相应反应的离子方程式。

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某校“化学社”同学用如图装置电解硫酸钾溶液来获得氧气、氢气、硫酸和氢氧化钾。
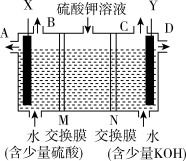
(1)Y极与电源的____ (填“正”或“负”)极相连,氧气从____ (填B或C)口导出。
(2)离子交换膜只允许一类离子通过,则M为____ (填“阴离子”或“阳离子”,下同)交换膜,N为___ 交换膜。
(3)若将制得的氢气、氧气和硫酸溶液组合为氢氧燃料电池(石墨为电极),则电池正极的电极反应式为____ 。
(4)若使用铅蓄电池作电源完成上述电解,当制得5.6L标准状况下的氧气时,理论上铅蓄电池消耗硫酸____ mol,正极板质量增加____ g。

(1)Y极与电源的
(2)离子交换膜只允许一类离子通过,则M为
(3)若将制得的氢气、氧气和硫酸溶液组合为氢氧燃料电池(石墨为电极),则电池正极的电极反应式为
(4)若使用铅蓄电池作电源完成上述电解,当制得5.6L标准状况下的氧气时,理论上铅蓄电池消耗硫酸
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】某课外小组设计如图1所示装置为电源对粗铜(含有Cu,少量Fe、Zn、Ag、Au等)进行精炼。
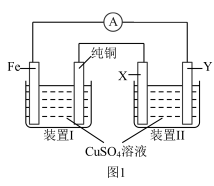
(1)装置Ⅰ中Fe电极上发生反应的电极反应式为___________ 。
(2)当反应一段时间后,经测量发现,Fe电极质量减少0.80 g,纯铜电极质量增重0.96 g,则实际经过电流表的电子的物质的量为___________ mol,装置Ⅰ的能量转化率为___________ 。(已知:装置Ⅰ中 足量)
足量)
(3)有同学提议,为避免副反应的发生,应将装置Ⅰ改为如图2所示装置,则溶液Z中溶质的化学式为___________ ,阴离子交换膜的作用为___________ (任写一条)。
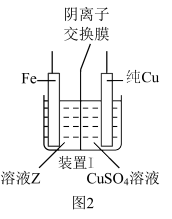
(4)装置Ⅱ中X电极材料的名称为___________ ,Y电极上的电极反应式为___________ ,一段时间后,装置Ⅱ溶液中阳离子主要为 和
和___________ 。

(1)装置Ⅰ中Fe电极上发生反应的电极反应式为
(2)当反应一段时间后,经测量发现,Fe电极质量减少0.80 g,纯铜电极质量增重0.96 g,则实际经过电流表的电子的物质的量为
 足量)
足量)(3)有同学提议,为避免副反应的发生,应将装置Ⅰ改为如图2所示装置,则溶液Z中溶质的化学式为

(4)装置Ⅱ中X电极材料的名称为
 和
和
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ.能源的开发、利用与人类社会的可持续发展息息相关,充分利用好能源是摆在人类面前的重大课题。
(1)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是_______ (填字母)
A.C(s)+CO2(g)=2CO(g) ΔH>0
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH<0
C.2H2O(l)=2H2(g)+O2(g) ΔH>0
D.C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(l) ΔH<0
若以稀硫酸为电解质溶液,则该原电池的负极反应式为_______
Ⅱ.如图所示的装置,X、Y都是惰性电极。将电路接通后,向乙中滴入酚酞溶液,在Fe极附近显红色。试回答下列问题:
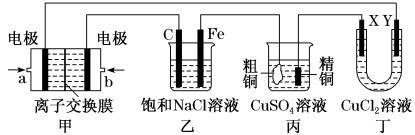
(2)甲装置是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,则a处通入的是_______ (填“CH4”或“O2”),电极上发生的电极反应是_______
(3)在乙装置中,总反应的离子方程式是_______
(4)如果丙装置中精铜电极的质量增加了6.4 g,则甲装置中消耗的CH4的质量为_______
(5)丁装置中在通电一段时间后,Y电极上发生的电极反应是_______
(1)依据原电池的构成原理,下列化学反应在理论上可以设计成原电池的是
A.C(s)+CO2(g)=2CO(g) ΔH>0
B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(l) ΔH<0
C.2H2O(l)=2H2(g)+O2(g) ΔH>0
D.C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(l) ΔH<0
若以稀硫酸为电解质溶液,则该原电池的负极反应式为
Ⅱ.如图所示的装置,X、Y都是惰性电极。将电路接通后,向乙中滴入酚酞溶液,在Fe极附近显红色。试回答下列问题:

(2)甲装置是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,则a处通入的是
(3)在乙装置中,总反应的离子方程式是
(4)如果丙装置中精铜电极的质量增加了6.4 g,则甲装置中消耗的CH4的质量为
(5)丁装置中在通电一段时间后,Y电极上发生的电极反应是
您最近一年使用:0次



