2.4 g镁与100 mL稀盐酸完全反应,反应前后溶液体积的变化忽略不计。
求:(1)产生的气体在标准状况下的体积___________________________ 。
(2)反应完全后,所得溶液中镁离子的物质的量浓度___________________________ 。
求:(1)产生的气体在标准状况下的体积
(2)反应完全后,所得溶液中镁离子的物质的量浓度
15-16高一上·河北保定·期末 查看更多[4]
(已下线)微专题02 以物质的量为中心的计算-备战2022年高考化学考点微专题甘肃省镇原县第二中学2020-2021学年高一上学期期末考试化学试题甘肃省武威第五中学2017-2018学年高一上学期第一次月考化学试题2015-2016学年河北省保定市望都中学高一上学期期末化学试卷
更新时间:2021-01-20 17:52:25
|
相似题推荐
填空题
|
容易
(0.94)
名校
解题方法
【推荐1】根据物质的量的相关知识回答下列问题
(1)与 氧气所含原子总数相同的氨气是
氧气所含原子总数相同的氨气是_______ g。
(2)已知某硫酸铜溶液的质量百分数为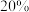 ,密度为
,密度为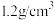 ,该溶液的物质的量浓度为
,该溶液的物质的量浓度为____ 。
(3)等质量的 和
和 的原子个数比为
的原子个数比为_______ 。
(4)标准状况下的 和
和 的混合气体
的混合气体 ,其质量为
,其质量为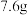 ,则混合气体平均相对分子质量为
,则混合气体平均相对分子质量为_______ ,该混合气体对 的相对密度为
的相对密度为_______ , 的质量为
的质量为_______ 。
(5)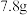 过氧化钠中共含有
过氧化钠中共含有_______  离子,它与足量水反应时转移的电子数
离子,它与足量水反应时转移的电子数_______ 个,产生标况下的气体体积约为_______ L。
(6)标况下 的密度约为
的密度约为_______  (保留三位有效数字)。
(保留三位有效数字)。
(1)与
 氧气所含原子总数相同的氨气是
氧气所含原子总数相同的氨气是(2)已知某硫酸铜溶液的质量百分数为
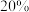 ,密度为
,密度为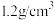 ,该溶液的物质的量浓度为
,该溶液的物质的量浓度为(3)等质量的
 和
和 的原子个数比为
的原子个数比为(4)标准状况下的
 和
和 的混合气体
的混合气体 ,其质量为
,其质量为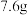 ,则混合气体平均相对分子质量为
,则混合气体平均相对分子质量为 的相对密度为
的相对密度为 的质量为
的质量为(5)
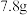 过氧化钠中共含有
过氧化钠中共含有 离子,它与足量水反应时转移的电子数
离子,它与足量水反应时转移的电子数(6)标况下
 的密度约为
的密度约为 (保留三位有效数字)。
(保留三位有效数字)。
您最近半年使用:0次
填空题
|
容易
(0.94)
【推荐2】试回答下列问题:
(1)0.5mol的 气体中:
气体中:
①质量为________ g,②约含________ 个氢原子,③标准状况下的体积为________ L;
(2)含 的
的 溶液100mL,取出10mL,
溶液100mL,取出10mL, 的物质的量浓度为
的物质的量浓度为________ mol/L。
(1)0.5mol的
 气体中:
气体中: ①质量为
(2)含
 的
的 溶液100mL,取出10mL,
溶液100mL,取出10mL, 的物质的量浓度为
的物质的量浓度为
您最近半年使用:0次
【推荐1】水煤气因其燃烧速度快、抗爆性好等优点,广泛应用于燃料和化工原料。制备水煤气的主要反应方程式为: 。
。
(1)作还原剂的物质是_______ ,碳元素的化合价_____ (填“升高”或“降低”)。
(2)若反应中消耗了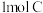 ,则生成CO的物质的量为
,则生成CO的物质的量为________ mol,转移电子的物质的量为______ mol。
 。
。(1)作还原剂的物质是
(2)若反应中消耗了
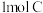 ,则生成CO的物质的量为
,则生成CO的物质的量为
您最近半年使用:0次
填空题
|
容易
(0.94)
【推荐2】(1)在实验室中用MnO2和浓盐酸反应制备氯气,其反应的化学方程式为_______________ ;
(2)某同学欲制取2.24L(标况)氯气,其做法是称取8.7g二氧化锰与40mL10mol·L—1的浓盐酸反应,其做法能否达到目的_______________ (填“能”、“或“不能”)。通过计算和文字叙述说明之_______________ 。
(2)某同学欲制取2.24L(标况)氯气,其做法是称取8.7g二氧化锰与40mL10mol·L—1的浓盐酸反应,其做法能否达到目的
您最近半年使用:0次



