水煤气因其燃烧速度快、抗爆性好等优点,广泛应用于燃料和化工原料。制备水煤气的主要反应方程式为: 。
。
(1)作还原剂的物质是_______ ,碳元素的化合价_____ (填“升高”或“降低”)。
(2)若反应中消耗了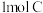 ,则生成CO的物质的量为
,则生成CO的物质的量为________ mol,转移电子的物质的量为______ mol。
 。
。(1)作还原剂的物质是
(2)若反应中消耗了
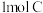 ,则生成CO的物质的量为
,则生成CO的物质的量为
更新时间:2023-12-30 16:17:48
|
相似题推荐
填空题
|
容易
(0.94)
解题方法
【推荐1】有19gNa2CO3和NaHCO3的混合物,与足量的稀盐酸反应,放出标准状况下CO2的体积为4.48L。则混合物中Na2CO3和NaHCO3的质量分别是_______ 、_______ 。
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】在空气中煅烧 生成钴氧化物和
生成钴氧化物和 ,测得充分煅烧后固体质量为2.41g,
,测得充分煅烧后固体质量为2.41g, 体积为1.344L(标准状况),则钴氧化物的化学式为
体积为1.344L(标准状况),则钴氧化物的化学式为________ 。
 生成钴氧化物和
生成钴氧化物和 ,测得充分煅烧后固体质量为2.41g,
,测得充分煅烧后固体质量为2.41g, 体积为1.344L(标准状况),则钴氧化物的化学式为
体积为1.344L(标准状况),则钴氧化物的化学式为
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐3】(1)0.5 mol H2O的质量为________ g,其中含有_______ 个水分子,共有____ 个原子。
(2)质量都是50 g的 HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是______ ,在相同温度和相同压强条件下,体积最大的是____ ,体积最小的是______ 。
(3)配制50 mL 0.2 mol/L CuSO4溶液,需要CuSO4____ g;需要CuSO4·5H2O____ g。
(4)中和相同体积、相同物质的量浓度的NaOH溶液,并使其生成正盐,需要相同物质的量浓度的HCl、H2SO4、H3PO4溶液的体积比为_________ 。
(2)质量都是50 g的 HCl、NH3、CO2、O2四种气体中,含有分子数目最少的是
(3)配制50 mL 0.2 mol/L CuSO4溶液,需要CuSO4
(4)中和相同体积、相同物质的量浓度的NaOH溶液,并使其生成正盐,需要相同物质的量浓度的HCl、H2SO4、H3PO4溶液的体积比为
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐1】回答下列问题:
(1)在S2-、Fe3+、Fe2+、Mg2+、S、I-、H+中,只有氧化性的是________ ,只有还原性的是________ ,既有氧化性又有还原性的是________ 。
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3→N2O3+H2O
②N2O4+H2O→HNO3+HNO2
③NH3+NO→HNO2+H2O
其中你认为一定不可能实现的是________ (填序号)。
(3)在反应2FeCl3+2KI=2FeCl2+2KCl+I2中:还原产物为________ 。
(1)在S2-、Fe3+、Fe2+、Mg2+、S、I-、H+中,只有氧化性的是
(2)某同学写出以下三个化学方程式(未配平):
①NO+HNO3→N2O3+H2O
②N2O4+H2O→HNO3+HNO2
③NH3+NO→HNO2+H2O
其中你认为一定不可能实现的是
(3)在反应2FeCl3+2KI=2FeCl2+2KCl+I2中:还原产物为
您最近一年使用:0次
填空题
|
容易
(0.94)
名校
解题方法
【推荐2】有下列物质:①氢氧化钡固体②KHSO4③HNO3④稀硫酸⑤二氧化碳气体⑥铜⑦碳酸钠粉末⑧蔗糖晶体⑨熔融氯化钠⑩CuSO4·5H2O晶体。请用序号填空:
(1)上述状态下可导电的是___ 。
(2)属于电解质的是____ 。
(3)属于非电解质的是___ 。
(4)②在水溶液中的电离方程式为___ ,①与②在溶液中反应使溶液呈中性的离子方程式为____ 。
(5)③与⑥可以发生如下反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
I.还原产物是___ 。
II.用单线桥法标出反应中电子转移的方向和数目___ 。
(1)上述状态下可导电的是
(2)属于电解质的是
(3)属于非电解质的是
(4)②在水溶液中的电离方程式为
(5)③与⑥可以发生如下反应:Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
I.还原产物是
II.用单线桥法标出反应中电子转移的方向和数目
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐1】实验室用足量MnO2和密度1.09g/mL,质量分数33.5%的盐酸混合加热制取氯气。
(1)写出该反应的化学方程式_______ 。
(2)计算盐酸物质的量浓度_______ 。
(3)若反应中收集到氯气4.48L(标准状况),应向反应器中加入浓盐酸的体积是______ ,说明理由____ 。
(1)写出该反应的化学方程式
(2)计算盐酸物质的量浓度
(3)若反应中收集到氯气4.48L(标准状况),应向反应器中加入浓盐酸的体积是
您最近一年使用:0次
填空题
|
容易
(0.94)
【推荐2】根据反应8NH3+3Cl2=6NH4Cl+N2回答下列问题。
(1)氧化剂_________ ,还原剂__________ ,氧化产物________ ,还原产物________ 。
(2)氧化剂与氧化产物的质量比________________________________ 。
(3)当生成28gN2时,被氧化的物质的质量是____________________ g。
(1)氧化剂
(2)氧化剂与氧化产物的质量比
(3)当生成28gN2时,被氧化的物质的质量是
您最近一年使用:0次

 填“下口放出”或“上口倒出”
填“下口放出”或“上口倒出”
 的反应:
的反应: 。
。 ,理论上转移的电子数是
,理论上转移的电子数是

