已知:将Cl2通入适量NaOH溶液,产物中可能有NaCl、NaClO、NaClO3,且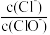 的值与温度高低有关,当n(NaOH)=amol时,下列有关说法不正确的是
的值与温度高低有关,当n(NaOH)=amol时,下列有关说法不正确的是
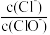 的值与温度高低有关,当n(NaOH)=amol时,下列有关说法不正确的是
的值与温度高低有关,当n(NaOH)=amol时,下列有关说法不正确的是A.参加反应的氯气的物质的量为 mol mol |
B.改变温度,产物中NaClO3的最大理论产量为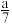 mol mol |
C.改变温度,反应中转移电子的物质的量n(e-)的范围: mol≤n(e-)≤ mol≤n(e-)≤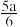 mol mol |
D.某温度下,若反应后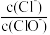 =11,则溶液中 =11,则溶液中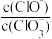 = = |
2017·河北衡水·一模 查看更多[25]
黑龙江省鸡西市第一中学2021-2022学年高一上学期期中考试化学试题福建泉州市第一中学2021-2022学年高三上学期期中考化学试题辽宁省昌图第一高级中学2021-2022学年高一上学期期中考试化学试题湖南省长沙市明德中学2020-2021学年高二下学期期中考试化学试题江西省新余市第四中学2020-2021学年高一上学期第二次段考化学试题(已下线)【浙江新东方】72四川省成都市树德中学2020-2021学年高一上学期12月阶段性测试化学试题(已下线)【浙江新东方】【2020】【高一上】【期中】【HD-LP409】【化学】辽宁省沈阳市郊联体2020-2021学年高一上学期期中考试化学试题夯基提能2020届高三化学选择题对题专练——化学计算中的常见方法和应用安徽省六安市霍邱县第二中学2019-2020学年高一上学期段考化学试题辽宁省实验中学2019-2020学年高一上学期期中考试化学试题内蒙古鄂尔多斯市第一中学2020届高三10月月考化学试题【全国百强校】安徽省合肥市第六中学2018-2019学年高一下学期开学考试化学试题【全国百强校】河南省信阳高级中学2018-2019学年高一上学期期末考试化学试题【全国百强校】新疆维吾尔自治区兵团第二师华山中学2019届高三上学期第二次月考化学试题【全国百强校】内蒙古自治区赤峰二中2019届高三上学期第二次月考化学试题【全国百强校】内蒙古自治区赤峰第二中学2019届高三上学期第二次月考化学试题河北省衡水中学2019届高三开学二调考试化学试题辽宁省葫芦岛市第六中学2019届高三上学期开学考试(8月)化学试题安徽省皖中地区2019届高三入学摸底考试化学试题(已下线)二轮复习测试专项-专题12 非金属及其化合物云南省临沧市第一中学2018届高三上学期第七次月考化学试题湖北省沙市中学2018届高三上学期第二次双周考试化学试题河北省衡水中学2018届高三上学期二调考试化学试题
更新时间:2021-01-20 19:20:18
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】现有部分被氧化的Fe、Cu混合物(氧化物为Fe2O3、CuO)样品共5.60 g,经如下处理:

下列说法正确的是

下列说法正确的是
| A.V= 672 |
| B.滤液A中的阳离子为Fe2+、Fe3+、H+ |
| C.样品中氧元素的物质的量为0. 02 mol |
| D.溶解样品的过程中消耗硫酸的总物质的量为0.05 mol |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】11.6 gFe3O4加到100 mL某浓度的盐酸中,再加入9.8 g铁粉,反应停止时,溶液中无固体存在。向溶液中滴加硫氰化钾溶液,未见颜色变化,为了中和过量的盐酸(不考虑盐酸的挥发),且使铁完全转化成Fe(OH)2,共消耗5.0 mol·L-1NaOH溶液160mL。则原盐酸的物质的量浓度为( )
| A.2 mol·L-1 | B.4 mol·L-1 | C.6 mol·L-1 | D.8 mol·L-1 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】将0.1 mol镁和铝的混合物溶于100 mL 2 mol/L 稀硫酸中,然后滴加1 mol/L的NaOH溶液。若在滴加NaOH溶液的过程中,沉淀质量随加入NaOH溶液体积的变化如图所示,下列说法正确的是
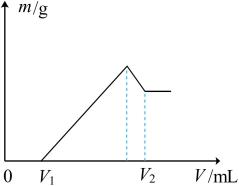

| A.当V1=150 mL时,金属粉末中镁粉的质量分数为50% |
| B.若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)=400mL。 |
C.若其中镁粉的物质的量分数为a,用100 mL 2 mol/L稀硫酸溶解此混合物后,再加入450 mL 1 mol/L NaOH溶液,所得沉淀中无Al(OH)3,则a的取值范围为 <a<1 <a<1 |
| D.若在滴加NaOH溶液的体积为V2时,溶液中溶质为NaAlO2 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】已知在酸性介质中,MnSO与(NH4)2S2O8(过二硫酸铵)溶液会发生反应:Mn2++S2O82—→MnO4—+SO42—,下列说法正确的是,
| A.反应过程中,因消耗溶液中的H+反应后溶液pH增大 |
| B.氧化性:S2O82—> MnO4— |
| C.该反应中酸性介质可以为盐酸 |
| D.0.1mol氧化剂参加反应,转移电子0.5mol |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】Cl2通入足量的氢氧化钠溶液,温度不同时充分反应后产物溶液中除大量OH-外,还有Cl-、ClO-、ClO3-,已知:Cl2+OH-→Cl-+ClO-+H2O(冷碱)、Cl2+OH-→Cl-+ClO3-+H2O(热碱),并知ClO-、ClO3-离子的物质的量比为2:1,试问原混合气体中Cl2与反应后溶液中的Cl-物质的量之比为( )
| A.2:5 | B.3:1 | C.1:1 | D.5:7 |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】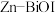 电池以
电池以 水溶液作为锌离子电池的氧化还原介质,可实现快速可逆的协同转化反应,具有超高的可逆容量和超长循环寿命。下列说法
水溶液作为锌离子电池的氧化还原介质,可实现快速可逆的协同转化反应,具有超高的可逆容量和超长循环寿命。下列说法不正确 的是
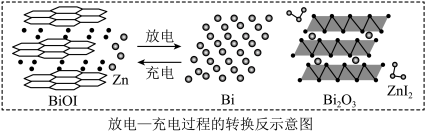
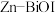 电池以
电池以 水溶液作为锌离子电池的氧化还原介质,可实现快速可逆的协同转化反应,具有超高的可逆容量和超长循环寿命。下列说法
水溶液作为锌离子电池的氧化还原介质,可实现快速可逆的协同转化反应,具有超高的可逆容量和超长循环寿命。下列说法
A. 能加快电极反应速率 能加快电极反应速率 |
B.放电时,正极反应为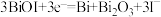 |
C.充电时, 与外接电源正极相连 与外接电源正极相连 |
D.充电时,若转移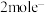 ,两电极总质量增加 ,两电极总质量增加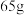 |
您最近半年使用:0次
【推荐2】实验研究发现,金属与硝酸发生氧化还原反应时,硝酸的浓度越稀,对应还原产物中氮元素的化合价越低。现有一定量的铝粉和铁粉的混合物与足量很稀的硝酸充分反应,反应过程中无气体放出,在反应结束后的溶液中逐滴加入5mol/LNaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示,下列说法不正确的是

A.硝酸的还原产物全部是 | B.b点与a点的差值为0.05mol |
| C.原硝酸溶液中硝酸的物质的量为0.47mol | D.样品中铝粉和铁粉的物质的之比为5:3 |
您最近半年使用:0次

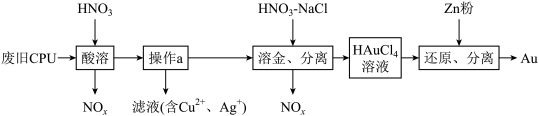
 。下列说法正确的是
。下列说法正确的是 的量比用稀硝酸的少
的量比用稀硝酸的少 也可以溶解金
也可以溶解金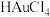 完全还原为Au,参加反应的Zn为1.5mol
完全还原为Au,参加反应的Zn为1.5mol

