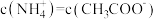某二元酸H2A,在溶液中发生电离的方程式:H2A=H++HA-、HA- H++A2-,则下列四种溶液中c(HA-)最大的是
H++A2-,则下列四种溶液中c(HA-)最大的是
 H++A2-,则下列四种溶液中c(HA-)最大的是
H++A2-,则下列四种溶液中c(HA-)最大的是| A.0.01mol·L-1的H2A溶液 |
| B.0.01mol·L-1的NaHA溶液 |
| C.0.03mol·L-1的盐酸与0.02mol·L-1的Na2A溶液等体积混合液 |
| D.0.03mol·L-1的NaOH与0.02mol·L-1的H2A溶液等体积混合液 |
更新时间:2021-01-25 13:47:59
|
【知识点】 弱电解质的电离平衡
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】常温下,下列溶液中微粒的物质的量浓度关系正确的是
A.向氨水中加入氯化铵固体,溶液中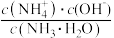 比值变大 比值变大 |
B.少量 通入过量冷的 通入过量冷的 溶液中: 溶液中: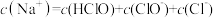 |
C. 的 的 溶液和 溶液和 的NaOH溶液,由水电离产生的 的NaOH溶液,由水电离产生的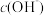 相等 相等 |
D.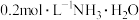 溶液与 溶液与 溶液等体积混合: 溶液等体积混合: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】室温下,通过下列实验探究0.1 mol/L的H2S溶液的性质
下列有关说法不正确的是
| 实验 | 实验操作及现象 |
| 1 | 用pH计测定0.1 mol/L的H2S溶液pH约为3.9 |
| 2 | 向0.1 mol/L的H2S溶液中通入足量SO2,溶液变浑浊 |
| 3 | 向0.1 mol/L的H2S溶液中滴加硫酸铜溶液,产生黑色沉淀,再加入硫酸锰溶液,沉淀量增加 |
| A.Ka1(H2S)约为10-6.8 |
| B.实验1中溶液存在c(H+)=c(HS-)+2c(S2-)+c(OH-) |
| C.实验2中的溶液pH先增大后减小,最终保持不变 |
| D.实验3可以说明Ksp(CuS)>Ksp(MnS) |
您最近一年使用:0次

 ,
,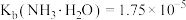 。下列说法正确的是
。下列说法正确的是 的氨水加水稀释,溶液中
的氨水加水稀释,溶液中 变大
变大 溶液加水稀释,所有离子的浓度均减小
溶液加水稀释,所有离子的浓度均减小 溶液中阴离子浓度之和,前者小于后者
溶液中阴离子浓度之和,前者小于后者