A、B、C、W均为中学常见的物质,它们之间有如下所示的转化关系(其他产物及反应条件已略去,反应可以在水溶液中进行)。
A B
B C
C
(1)若A、B、C三种物质的焰色反应均为黄色,A俗称苛性钠,W为无色无味气体,C受热分解可转化为B。
①A溶液与C溶液反应的离子方程式为___________ 。
(2)若A、B、C、W四种物质均为气体,其中A、W为单质,C的摩尔质量为46g·mol-1
①实验室制取B时,___________ (填“能”或“不能”)用向上排空气法收集B。
②C与水反应的化学方程式为___________ 。
(3)若A为淡黄色固体单质,W为气体单质,B、C均为酸性氧化物。
①由B生成C时,每生成0.5molC,电子转移的数目为___________ 。
②C溶于水形成化合物D,在加热的情况下,D的浓溶液与A反应的化学方程式为___________ 。
A
 B
B C
C (1)若A、B、C三种物质的焰色反应均为黄色,A俗称苛性钠,W为无色无味气体,C受热分解可转化为B。
①A溶液与C溶液反应的离子方程式为
(2)若A、B、C、W四种物质均为气体,其中A、W为单质,C的摩尔质量为46g·mol-1
①实验室制取B时,
②C与水反应的化学方程式为
(3)若A为淡黄色固体单质,W为气体单质,B、C均为酸性氧化物。
①由B生成C时,每生成0.5molC,电子转移的数目为
②C溶于水形成化合物D,在加热的情况下,D的浓溶液与A反应的化学方程式为
更新时间:2021-02-04 18:28:40
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】有关物质存在如图所示的转化关系(部分产物已省略)。通常C为气体单质,G为紫黑色固体单质。实验室中,常用固体E在B的催化下加热制取气体单质H。

请回答下列问题:
(1)闻气体C的方法为___________ ;收集气体C时验满的方法为___________ 。
(2)反应①的化学方程式为___________ 。
(3)反应②的离子方程式为___________ 。
(4)写出另外一种实验室制取H的化学方程式___________ 。

请回答下列问题:
(1)闻气体C的方法为
(2)反应①的化学方程式为
(3)反应②的离子方程式为
(4)写出另外一种实验室制取H的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下图中的每一方格表示有关的一种反应物或生成物,其中粗框表示初始反应物( 反应时加入或生成的水,以及生成沉淀J时的其它产物均已略去)。

已知:2NaCl+2H2O 2NaOH+Cl2↑+H2↑ F是常见的金属单质
2NaOH+Cl2↑+H2↑ F是常见的金属单质
请填写下列空白:
(1)B中元素在周期表中的位置是_____ ;H的电子式是_____ ;J是_____ ;(用化学式作答)
(2)反应②的方程式是________________________ ;现象是:___________________________ 。
(3)E是一种二元化合物,请用电子式表示其形成过程______________________________ 。

已知:2NaCl+2H2O
 2NaOH+Cl2↑+H2↑ F是常见的金属单质
2NaOH+Cl2↑+H2↑ F是常见的金属单质请填写下列空白:
(1)B中元素在周期表中的位置是
(2)反应②的方程式是
(3)E是一种二元化合物,请用电子式表示其形成过程
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C是中学化学常见的三种物质,它们之间的相互转化关系如图所示(部分反应条件及产物略去)。

(1)若A是一种黄色非金属单质固体,将B气体通入到酸性高锰酸钾溶液中能使其褪色,试写出B使酸性高锰酸钾溶液褪色的化学方程式_________________________________________ ;试写出D的浓溶液与碳反应的化学方程式为___________ 。
(2)若C是红棕色气体,则A的化学式为______ 或_____ ;试写出D的稀溶液与铜反应的离子方程式_____________ ;该反应中D的稀溶液表现出来的性质为______________ 。

(1)若A是一种黄色非金属单质固体,将B气体通入到酸性高锰酸钾溶液中能使其褪色,试写出B使酸性高锰酸钾溶液褪色的化学方程式
(2)若C是红棕色气体,则A的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D四种物质之间有下图所示的转化关系。已知:A是空气中的主要成分,B、C、D均为化合物,且C与水反应可得到B。

请回答下列问题:
(1)写出B的名称:_______________________ 。
(2)在上图D→C的过程中,Cu在反应中________ (填“被氧化”或”被还原”)。
(3)在D的稀溶液中滴入Na2CO3溶液,其反应的离子方程式是_______________________ 。

请回答下列问题:
(1)写出B的名称:
(2)在上图D→C的过程中,Cu在反应中
(3)在D的稀溶液中滴入Na2CO3溶液,其反应的离子方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
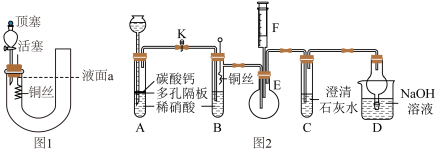
【推荐2】为了探究铜与稀硝酸反应产生的气体是NO,某课外活动小组设计了如下两套装置进行实验,请回答相关问题。
(1)如何检查该装置的气密性?___________ 。
(2)检验气密性后,重新组装好装置,打开分液漏斗的顶塞和活塞,从长管加入稀硝酸至液面到达a处,关闭活塞,微热短管,可观察到的实验现象为___________ 。
(二)乙同学设计了如图2所示装置(加热装置和固定装置均已略去)。装置气密性已检查,A中大理石,B、C、D中溶液均已装好,铜丝未浸入稀硝酸,止水夹K处于关闭状态,F是一半空的注射器。
(3)设计A装置的目的是___________ 。
(4)为达到上述目的应如何操作?___________ 。
(5)B装置中发生反应的离子方程式为___________ 。
(6)反应进行一段时间后,关闭止水夹K,将铜丝旋出稀硝酸液面。为验证铜和稀硝酸产生的气体是NO,应进行的操作和对应的现象是___________ 。
(1)如何检查该装置的气密性?
(2)检验气密性后,重新组装好装置,打开分液漏斗的顶塞和活塞,从长管加入稀硝酸至液面到达a处,关闭活塞,微热短管,可观察到的实验现象为
(二)乙同学设计了如图2所示装置(加热装置和固定装置均已略去)。装置气密性已检查,A中大理石,B、C、D中溶液均已装好,铜丝未浸入稀硝酸,止水夹K处于关闭状态,F是一半空的注射器。
(3)设计A装置的目的是
(4)为达到上述目的应如何操作?
(5)B装置中发生反应的离子方程式为
(6)反应进行一段时间后,关闭止水夹K,将铜丝旋出稀硝酸液面。为验证铜和稀硝酸产生的气体是NO,应进行的操作和对应的现象是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】某强酸性溶液X,含有 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的一种或几种离子,取溶液进行连续实验,能实现如下转化:
中的一种或几种离子,取溶液进行连续实验,能实现如下转化:

依据以上信息,回答下列问题:
(1)上述离子中,溶液X中肯定含有的是_______ ;对不能确定是否存在的离子,可以另取X溶液于一支试管中,选择下列试剂中的一种加入X溶液中,根据现象就可判断,则该试剂是:_______ 。(选填:①NaOH溶液,②酚酞试剂,③石蕊试剂,④pH试纸,⑤KSCN溶液,⑥KMnO4溶液)
(2)气体F的化学式为_______ ,沉淀G的化学式为_______ ,沉淀K的化学式为_______ ,实验中,可以观察到反应②的现象是_______ 。
(3)写出步骤①反应生成气体A的离子方程式_______ 。
(4)要使步骤③中,D、H2O、O2三种物质恰好发生化合反应,则D、H2O、O2物质的量之比是_______ 。
 、
、 、
、 、
、 、
、 、
、 、
、 、
、 、
、 中的一种或几种离子,取溶液进行连续实验,能实现如下转化:
中的一种或几种离子,取溶液进行连续实验,能实现如下转化:
依据以上信息,回答下列问题:
(1)上述离子中,溶液X中肯定含有的是
(2)气体F的化学式为
(3)写出步骤①反应生成气体A的离子方程式
(4)要使步骤③中,D、H2O、O2三种物质恰好发生化合反应,则D、H2O、O2物质的量之比是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D、M均为中学化学中的常见物质,A~D含有相同元素。其转化关系如下:
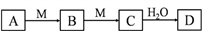
请回答:
(1)若A为淡黄色固体单质。
①A元素在周期表中的位置是_____ 。
②下列叙述正确的是_____ (填字母序号)。
a.B属于大气污染物,是导致酸雨的重要原因之一
b.C可以与CaO反应生成CaSO3
c.D的浓溶液可以在加热条件下与金属Cu反应生成B
(2)若A为能使湿润红色石蕊试纸变蓝的气体。
①写出C→D的化学方程式:_____________________ 。
②A与C反应生成一种空气中含量最多的气体E,若该反应中转移6mol电子,则生成的E在标准状况下的体积为_____ L。
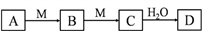
请回答:
(1)若A为淡黄色固体单质。
①A元素在周期表中的位置是
②下列叙述正确的是
a.B属于大气污染物,是导致酸雨的重要原因之一
b.C可以与CaO反应生成CaSO3
c.D的浓溶液可以在加热条件下与金属Cu反应生成B
(2)若A为能使湿润红色石蕊试纸变蓝的气体。
①写出C→D的化学方程式:
②A与C反应生成一种空气中含量最多的气体E,若该反应中转移6mol电子,则生成的E在标准状况下的体积为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】同学们欲验证 与
与 的转化,在实验室中进行了如下图所示的实验。(夹持仪器已省略)
的转化,在实验室中进行了如下图所示的实验。(夹持仪器已省略)_______ 。
(2)待石灰石反应停止后,将铜丝插入过量浓硝酸中,铜丝与浓硝酸反应的离子方程式是_______ ,插入铜丝后在具支试管中溶液上方观察到的现象是_______ 。
(3)广口瓶中水的作用是_______ ,有关反应的化学方程式是_______ 。
(4)欲证明圆底烧瓶中收集到的无色气体是 ,应进行的操作是
,应进行的操作是_______ ,观察到的现象是_______ 。
 与
与 的转化,在实验室中进行了如下图所示的实验。(夹持仪器已省略)
的转化,在实验室中进行了如下图所示的实验。(夹持仪器已省略)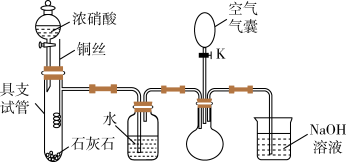
(2)待石灰石反应停止后,将铜丝插入过量浓硝酸中,铜丝与浓硝酸反应的离子方程式是
(3)广口瓶中水的作用是
(4)欲证明圆底烧瓶中收集到的无色气体是
 ,应进行的操作是
,应进行的操作是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A~H等8种物质存在如下转化关系(反应条件,部分产物未标出)。已知:A是正盐,B是能使品红溶液褪色的气体,G是红棕色气体。按要求回答问题:
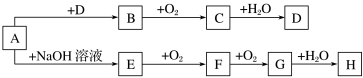
(1)写出下列物质的化学式:A____________ ,B____________ 。
(2)写出下列反应的化学方程式:
E→F___________________ G→H__________________ ;D的溶液与木炭反应的化学方程式: ________________ 。
(3)检验某溶液中是否含D中阴离子的方法是_________________ 。

(1)写出下列物质的化学式:A
(2)写出下列反应的化学方程式:
E→F
(3)检验某溶液中是否含D中阴离子的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】硫酸是当今世界最重要的化工产品之一、
I.硫酸的各种制法:
(1)早在1000多年前,我国就已采用加热胆矾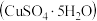 或绿矾
或绿矾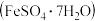 的方法制取硫酸。
的方法制取硫酸。 受热分解的化学方程式:
受热分解的化学方程式: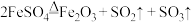 。
。
①将 受热产生的气体通入如图1装置中,以检验产生的气体中是否含有
受热产生的气体通入如图1装置中,以检验产生的气体中是否含有 和
和 。能说明
。能说明 存在的实验现象是
存在的实验现象是_______ 。能不能将图1中氯化钡溶液换成硝酸钡溶液?_______ (填“能”或“不能”)

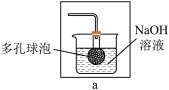
②有同学提出图1虚线框内盛装NaOH溶液的装置可以换成a装置,其中多孔玻璃球泡的作用是_____ 。
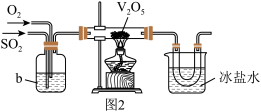
(2)目前工业上主要采用接触法制备硫酸,其中一步为: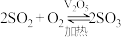 。实验室模拟该过程常用图2装置进行实验。b装置中装有浓硫酸,写出b装置的作用
。实验室模拟该过程常用图2装置进行实验。b装置中装有浓硫酸,写出b装置的作用_______ (写出两点)。
II.硫酸的性质
(3)图3中甲试管内发生反应的化学方程式为_______ 。
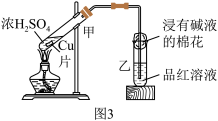
(4)当铜片与浓硫酸充分反应后,试管内并未出现蓝色溶液,而是看到了白色固体,请分别写出检验该白色固体离子组成的方法_______ 。
I.硫酸的各种制法:
(1)早在1000多年前,我国就已采用加热胆矾
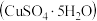 或绿矾
或绿矾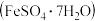 的方法制取硫酸。
的方法制取硫酸。 受热分解的化学方程式:
受热分解的化学方程式: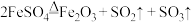 。
。①将
 受热产生的气体通入如图1装置中,以检验产生的气体中是否含有
受热产生的气体通入如图1装置中,以检验产生的气体中是否含有 和
和 。能说明
。能说明 存在的实验现象是
存在的实验现象是
②有同学提出图1虚线框内盛装NaOH溶液的装置可以换成a装置,其中多孔玻璃球泡的作用是

(2)目前工业上主要采用接触法制备硫酸,其中一步为:
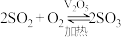 。实验室模拟该过程常用图2装置进行实验。b装置中装有浓硫酸,写出b装置的作用
。实验室模拟该过程常用图2装置进行实验。b装置中装有浓硫酸,写出b装置的作用
II.硫酸的性质
(3)图3中甲试管内发生反应的化学方程式为

(4)当铜片与浓硫酸充分反应后,试管内并未出现蓝色溶液,而是看到了白色固体,请分别写出检验该白色固体离子组成的方法
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】为研究含硫化合物的性质,某兴趣小组在老师的指导下设计了如下实验。
(1)A装置试管中主要反应的化学方程式是___________ 。反应中,浓硫酸表现出的性质是___________ (填正确选项的字母)。
A.酸性B.氧化性C.脱水性D.吸水性
(2)仪器a的名称是___________ ,在本实验中的作用是___________ 。
(3)B中溴水出现的现象是___________ ,说明SO2具有的性质是___________ 。
(4)D中Na2O2与SO2反应生成Na2SO4,反应的化学方程式是___________
(5)实验中,取一定质量铜片和一定体积18mol·L-1硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是___________ 。
②若将反应后的烧瓶中溶液继续加热至气体完全排出,下列药品中能用来证明反应结束后的烧瓶中确有余酸的是___________ (填字母)。
a.铁粉b.BaCl2溶液c.银粉d.紫色石蕊溶液

(1)A装置试管中主要反应的化学方程式是
A.酸性B.氧化性C.脱水性D.吸水性
(2)仪器a的名称是
(3)B中溴水出现的现象是
(4)D中Na2O2与SO2反应生成Na2SO4,反应的化学方程式是
(5)实验中,取一定质量铜片和一定体积18mol·L-1硫酸放在圆底烧瓶中共热,直到反应完毕,发现烧瓶中还有铜片剩余,该小组学生根据所学的化学知识认为还有一定量的硫酸剩余。
①有一定量的余酸但未能使铜片完全溶解,你认为原因是
②若将反应后的烧瓶中溶液继续加热至气体完全排出,下列药品中能用来证明反应结束后的烧瓶中确有余酸的是
a.铁粉b.BaCl2溶液c.银粉d.紫色石蕊溶液
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】硫酸是用途广泛的化工原料,可作脱水剂、吸水剂、氧化剂和催化剂等。
(1)工业制硫酸铜的方法很多。
①方法一、用浓硫酸和铜制取硫酸铜。该反应的化学方程式是_______ 。
②方法二、用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如下图所示:

稀硫酸和氧化铁反应的离子方程式是_________ ;铜和上述反应得到的物质反应的离子方程式是_________ ;向混合溶液中通入热空气的反应的离子方程式是_________ ;分离蓝色滤液和红褐色沉淀的实验操作是_________ 。
(2)氨法脱硫技术可吸收硫酸工业尾气中的二氧化硫,同时制得硫酸铵。主要的工艺流程如下图所示:

①吸收塔中发生反应的化学方程式是_________ 。
②检验硫酸铵中的NH4+的离子方程式是_________ 。
(1)工业制硫酸铜的方法很多。
①方法一、用浓硫酸和铜制取硫酸铜。该反应的化学方程式是
②方法二、用稀硫酸、铜和氧化铁制取硫酸铜,生产的主要过程如下图所示:

稀硫酸和氧化铁反应的离子方程式是
(2)氨法脱硫技术可吸收硫酸工业尾气中的二氧化硫,同时制得硫酸铵。主要的工艺流程如下图所示:

①吸收塔中发生反应的化学方程式是
②检验硫酸铵中的NH4+的离子方程式是
您最近一年使用:0次



