(1)漂白粉的有效成分是______ (填化学式),漂白粉在空气中与CO2反应生成次氯酸,次氯酸不稳定,请写出次氯酸分解的化学方程式______ 。
(2)过氧化钠常用作呼吸面具或潜水艇中的供氧剂,它可以将人体呼出的二氧化碳转化为所需要的氧气,试写出其化学方程式______ ,若需要氧气224 L(已折算成标况下的体积),则至少需要过氧化钠的质量为______ g。
(3)铝与NO 在酸性或碱性条件下均可反应,为了降低饮用水中NO
在酸性或碱性条件下均可反应,为了降低饮用水中NO 的浓度,可以在碱性条件下用铝粉将NO
的浓度,可以在碱性条件下用铝粉将NO 还原为N2,完善并配平该反应:
还原为N2,完善并配平该反应:______
______Al+______NO +______OH-=______+______N2↑+______H2O
+______OH-=______+______N2↑+______H2O
每消耗1 mol NO ,转移的电子数目为
,转移的电子数目为______ 。
(4)已知:CCl4与水不相溶且密度比水大,Cl2的CCl4溶液呈黄绿色,Br2的CCl4溶液呈橙红色,且Br2易从水溶液中溶入CCl4中。Cl2既能氧化Br-,也能氧化Fe2+。取10 mL 0.1 mol/L FeBr2溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为红色。另取少量反应后的溶液加入CCl4,振荡后,下层为无色液体。
①以上实验结论表明还原性:Fe2+______ Br-(填“>”或“<”)。
②若在40 mL 0.1 mol/L FeBr2溶液中通入标准状况下67.2 mL的Cl2,取少量反应后的溶液加入CCl4,振荡后下层液体呈______ 色,写出该反应的离子方程式______ 。
(2)过氧化钠常用作呼吸面具或潜水艇中的供氧剂,它可以将人体呼出的二氧化碳转化为所需要的氧气,试写出其化学方程式
(3)铝与NO
 在酸性或碱性条件下均可反应,为了降低饮用水中NO
在酸性或碱性条件下均可反应,为了降低饮用水中NO 的浓度,可以在碱性条件下用铝粉将NO
的浓度,可以在碱性条件下用铝粉将NO 还原为N2,完善并配平该反应:
还原为N2,完善并配平该反应:______Al+______NO
 +______OH-=______+______N2↑+______H2O
+______OH-=______+______N2↑+______H2O每消耗1 mol NO
 ,转移的电子数目为
,转移的电子数目为(4)已知:CCl4与水不相溶且密度比水大,Cl2的CCl4溶液呈黄绿色,Br2的CCl4溶液呈橙红色,且Br2易从水溶液中溶入CCl4中。Cl2既能氧化Br-,也能氧化Fe2+。取10 mL 0.1 mol/L FeBr2溶液,向其中滴加几滴新制的氯水,振荡后溶液呈黄色。取少量反应后的溶液加入KSCN溶液,溶液变为红色。另取少量反应后的溶液加入CCl4,振荡后,下层为无色液体。
①以上实验结论表明还原性:Fe2+
②若在40 mL 0.1 mol/L FeBr2溶液中通入标准状况下67.2 mL的Cl2,取少量反应后的溶液加入CCl4,振荡后下层液体呈
更新时间:2021-02-27 14:28:08
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】双氧水和84消毒液是生活中常用的两种消毒剂,了解物质的性质是科学合理使用化学品的基础和前提。请回答下列问题:
(1)某同学设计如下实验研究H2O2的性质:
① 从理论上看H2O2既有氧化性又有还原性,具有还原性的原因是______ 。
② 能证明H2O2具有还原性的实验是______ (填序号)。可作为证据的实验现象是______ (填字母序号)。
(2)84消毒液的有效成分为NaClO
① 将Cl2通入NaOH溶液中可制得84消毒液,化学反应方程式为:______
② 84消毒液不能用于钢制器具的消毒,原因是NaClO具有______ 性。
③ 84消毒液的溶液在浸泡餐具过程中,因吸收空气中CO2消毒杀菌能力增强,该反应说明酸性强弱为______
(3)2016年巴西奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。
① 该反应说明氧化性:NaClO______ H2O2的(填“>”或“<”)。
② 当有0.1mol O2生成时,转移电子______ mol
(1)某同学设计如下实验研究H2O2的性质:
| 序号 | 实验 | 实验现象 |
| ⅰ | 向5%H2O2溶液中滴加酸性KMnO4溶液 | a. 溶液紫色褪去 b. 有大量气泡产生 |
| ⅱ | 向5%H2O2溶液中滴加淀粉碘化钾溶液 | c. 溶液变蓝 |
① 从理论上看H2O2既有氧化性又有还原性,具有还原性的原因是
② 能证明H2O2具有还原性的实验是
(2)84消毒液的有效成分为NaClO
① 将Cl2通入NaOH溶液中可制得84消毒液,化学反应方程式为:
② 84消毒液不能用于钢制器具的消毒,原因是NaClO具有
③ 84消毒液的溶液在浸泡餐具过程中,因吸收空气中CO2消毒杀菌能力增强,该反应说明酸性强弱为
(3)2016年巴西奥运会期间,由于工作人员将84消毒液与双氧水两种消毒剂混用,导致游泳池藻类快速生长,池水变绿。一种可能的原因是NaClO与H2O2反应产生O2促进藻类快速生长。
① 该反应说明氧化性:NaClO
② 当有0.1mol O2生成时,转移电子
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某一反应体系中有反应物和生成物共6种:HCl、H2SO4、SnCl2、SnCl4、FeSO4、Fe2(SO4)3,在反应后的溶液中滴加KSCN溶液不显红色。
(1)该反应中,被氧化的元素是____________ ,氧化剂是____________ 。
(2)写出该反应的化学方程式并标明电子转移的方向和数目:_____________________ 。
(3) 由此可知,氧化性强弱的关系是:Fe2(SO4)3____________ 。SnCl4, 还原性强弱的关系是:SnCl2__ FeSO4(填>,﹤或 = )
(1)该反应中,被氧化的元素是
(2)写出该反应的化学方程式并标明电子转移的方向和数目:
(3) 由此可知,氧化性强弱的关系是:Fe2(SO4)3
您最近一年使用:0次
【推荐3】过氧化氢溶液俗称双氧水,有杀菌消毒的作用,医疗上常用它来清洗伤口,工业上有时也可作为矿业废液消毒剂,有“绿色氧化剂”的美称。某小组设计如下实验探究H2O2的性质:
(1)已知 H2O2的稳定性与溶液pH的关系如图所示(pH越小代表溶液酸性越强)。

①H2O2中氧元素的化合价为_______ ,请写出H2O2分解反应的化学方程式:_______ 。
②根据题中信息可知新配制好的H2O2溶液中需滴入几滴_______ 以保证溶液的稳定性(填“稀硫酸”或“氨水”)。
(2)向硫酸酸化的KMnO4溶液中滴加H2O2溶液,振荡,溶液紫红色褪去并产生大量无色气泡,把带火星的木条靠近试管口木条复燃。已知反应生成了无色的MnSO4溶液,则该反应的氧化产物为_______ ,证明H2O2具有性_______ 性(填“氧化”或“还原”)。
(3)向双氧水中通入H2S气体,有淡黄色S沉淀产生,该反应证明H2O2具有_______ 性(填“氧化”或“还原”)。
(4)下列反应中H2O2表现出来的性质与 中H2O2表现出来的性质相同的是
中H2O2表现出来的性质相同的是_______ 。
A.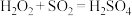
B.
C.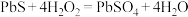
(5)已知I-、Fe2+、SO2、H2O2均有一定的还原性,它们在酸性溶液中还原性的强弱顺序为:SO2>I->H2O2>Fe2+,则下列反应不能发生的是_______。
(1)已知 H2O2的稳定性与溶液pH的关系如图所示(pH越小代表溶液酸性越强)。

①H2O2中氧元素的化合价为
②根据题中信息可知新配制好的H2O2溶液中需滴入几滴
(2)向硫酸酸化的KMnO4溶液中滴加H2O2溶液,振荡,溶液紫红色褪去并产生大量无色气泡,把带火星的木条靠近试管口木条复燃。已知反应生成了无色的MnSO4溶液,则该反应的氧化产物为
(3)向双氧水中通入H2S气体,有淡黄色S沉淀产生,该反应证明H2O2具有
(4)下列反应中H2O2表现出来的性质与
 中H2O2表现出来的性质相同的是
中H2O2表现出来的性质相同的是A.
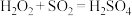
B.

C.
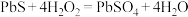
(5)已知I-、Fe2+、SO2、H2O2均有一定的还原性,它们在酸性溶液中还原性的强弱顺序为:SO2>I->H2O2>Fe2+,则下列反应不能发生的是_______。
A. | B. |
C.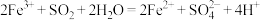 | D.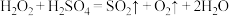 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】土壤中的硝酸盐会被细菌分解。有一种脱氧硫杆菌能够利用土壤中的硫化物来分解硝酸盐,其主要化学原理如下:
____ ____
____ ____
____ ___
___ ____
____ _____KOH,配平反应方程式,并
_____KOH,配平反应方程式,并标出电子转移的方向和数目 _______ 。
____
 ____
____ ____
____ ___
___ ____
____ _____KOH,配平反应方程式,并
_____KOH,配平反应方程式,并
您最近一年使用:0次
【推荐2】Ⅰ某一反应体系有反应物和生成物共五种物质: 、
、 、
、 、
、 、
、 已知该反应中
已知该反应中 只发生如下过程:
只发生如下过程:
(1)该反应中的还原剂是_____________ 。
(2)写出该反应的化学方程式,并用单线桥法标出电子转移的方向和数目:_____________
(3)上述反应中每生成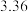 升氧气
升氧气 标准状况
标准状况 ,转移电子数是
,转移电子数是_________________ 。
Ⅱ四氧化三铁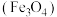 磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。水热法制备
磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。水热法制备 纳米颗粒的反应是
纳米颗粒的反应是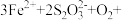 x
x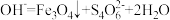 。请回答下列问题。
。请回答下列问题。
(4)水热法制备 纳米颗粒的反应中,还原剂是
纳米颗粒的反应中,还原剂是____________ 。
(5)反应的化学方程式中x
________ 。
(6)每生成 ,反应转移的电子为
,反应转移的电子为________ mol,被 还原的
还原的 的物质的量为
的物质的量为________ mol。
 、
、 、
、 、
、 、
、 已知该反应中
已知该反应中 只发生如下过程:
只发生如下过程:
(1)该反应中的还原剂是
(2)写出该反应的化学方程式,并用单线桥法标出电子转移的方向和数目:
(3)上述反应中每生成
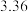 升氧气
升氧气 标准状况
标准状况 ,转移电子数是
,转移电子数是Ⅱ四氧化三铁
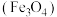 磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。水热法制备
磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。水热法制备 纳米颗粒的反应是
纳米颗粒的反应是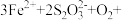 x
x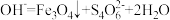 。请回答下列问题。
。请回答下列问题。(4)水热法制备
 纳米颗粒的反应中,还原剂是
纳米颗粒的反应中,还原剂是(5)反应的化学方程式中x

(6)每生成
 ,反应转移的电子为
,反应转移的电子为 还原的
还原的 的物质的量为
的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】根据所学知识回答下列问题:
(1)H2O2是常见氧化剂,为了验证其氧化性,进行了下列实验:
①取2mLH2O2于试管中,通入H2S气体,溶液变浑浊,反应的化学方程式为__________ 。
②有同学认为Na2SO3也有还原性,可以选择其作为试剂验证H2O2氧化性。该观点是否正确,请从化合价的角度说明理由:__________ 。
(2)饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,某饮用水研究人员提出两种处理方案:
的浓度,某饮用水研究人员提出两种处理方案:
方案一:碱性条件下用 还原[氧化产物为
还原[氧化产物为 ]
] 生成
生成 ,反应中氧化剂和还原剂物质的量之比为
,反应中氧化剂和还原剂物质的量之比为__________ 。
方案二:在碱性条件下,用铝粉处理,已知反应时Al与 为
为 ,且Al转化为
,且Al转化为 ,被氧化的元素是
,被氧化的元素是__________ ,还原产物是__________ ,请写出反应的离子方程式:__________ 。
(1)H2O2是常见氧化剂,为了验证其氧化性,进行了下列实验:
①取2mLH2O2于试管中,通入H2S气体,溶液变浑浊,反应的化学方程式为
②有同学认为Na2SO3也有还原性,可以选择其作为试剂验证H2O2氧化性。该观点是否正确,请从化合价的角度说明理由:
(2)饮用水中的
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,某饮用水研究人员提出两种处理方案:
的浓度,某饮用水研究人员提出两种处理方案:方案一:碱性条件下用
 还原[氧化产物为
还原[氧化产物为 ]
] 生成
生成 ,反应中氧化剂和还原剂物质的量之比为
,反应中氧化剂和还原剂物质的量之比为方案二:在碱性条件下,用铝粉处理,已知反应时Al与
 为
为 ,且Al转化为
,且Al转化为 ,被氧化的元素是
,被氧化的元素是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】2010年4月14日7时49分在青海省玉树地区发生7.1级地震,造成了重大的人员伤亡和财产损失。为了保证震区的卫生环境,常使用漂白液和漂白粉对环境和饮用水进行杀菌、消毒,以抑制大规模传染病爆发。
回答下列问题:
(1)漂白液的有效成分是(填化学式)____________________ ;
(2)某研究性学习小组对漂白液进行了如下实验探究:取漂白液少量,滴入3~5滴紫色石蕊试液,发现溶液先变蓝色后褪色,可以证明漂白液具有的性质____________ (填序号)。
(3)工业上用氯气通入石灰乳[Ca(OH)2]制取漂白粉的化学方程式:
_____________________________________________________________________________ 。
(4)已知二氧化硫和亚硫酸盐具有较强的还原性。若将少量的SO2通入漂白粉溶液中,有同学认为发生的反应为:Ca(ClO)2+SO2+H2O=CaSO3↓+2HClO。你认为该同学的说法是否正确?
(填“正确”或“不正确”),请说明理由______________________________________________ 。
(5)二氧化氯是世卫组织确认的A级新型高效安全的消毒剂,其安全性远高于氯气。制备方法之一是:2NaClO3+4HCl =2ClO2↑+ Cl2↑+ 2NaCl + 2H2O,当转移0.2mol电子时,参加反应的还原剂的物质的量为___________ 。
回答下列问题:
(1)漂白液的有效成分是(填化学式)
(2)某研究性学习小组对漂白液进行了如下实验探究:取漂白液少量,滴入3~5滴紫色石蕊试液,发现溶液先变蓝色后褪色,可以证明漂白液具有的性质
| A.酸性 | B.碱性 | C.强氧化性 | D.还原性 |
(3)工业上用氯气通入石灰乳[Ca(OH)2]制取漂白粉的化学方程式:
(4)已知二氧化硫和亚硫酸盐具有较强的还原性。若将少量的SO2通入漂白粉溶液中,有同学认为发生的反应为:Ca(ClO)2+SO2+H2O=CaSO3↓+2HClO。你认为该同学的说法是否正确?
(填“正确”或“不正确”),请说明理由
(5)二氧化氯是世卫组织确认的A级新型高效安全的消毒剂,其安全性远高于氯气。制备方法之一是:2NaClO3+4HCl =2ClO2↑+ Cl2↑+ 2NaCl + 2H2O,当转移0.2mol电子时,参加反应的还原剂的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】84 消毒液是生活中常见的一种消毒剂,常用于环境的消毒,其主要成分是NaClO。
(1)84 消毒液使用时除了要按一定比例稀释,对消毒时间也有要求,一般在 10-20 分钟左右。结合有关的化学方程式解释原因_______ ,家庭使用 84 消毒液时,可以采取哪些措施缩短消毒时间_______ 。
(2)次氯酸钠可以用于去除废水中的铵态氮,配平下列离子方程式______ 。
_______NH +_______ClO-→_______N2+_______Cl-+_______H2O+_______H+
+_______ClO-→_______N2+_______Cl-+_______H2O+_______H+
(3)84 消毒液的制取和漂粉精的制取原理相同,都是用氯气和碱反应来制取,84 消毒液所用的碱是氢氧化钠溶液,写出该反应的离子方程式_______ 。
(4)消毒学专家指出,将 84 消毒液与洁厕灵(主要成分:浓盐酸)一起合并使用,可能会导致使用者的呼吸道伤害。结合有关的化学方程式分析可能的原因_______ 。
(5)有同学看到某品牌的 84 消毒液的注意事项有指出:“不得将本品与酸性产品同时使用”。这里酸并没有特指盐酸,该品牌的产品说明是否具备科学性呢?说出你的理由,并设计实验进行验证_______ 。
(1)84 消毒液使用时除了要按一定比例稀释,对消毒时间也有要求,一般在 10-20 分钟左右。结合有关的化学方程式解释原因
(2)次氯酸钠可以用于去除废水中的铵态氮,配平下列离子方程式
_______NH
 +_______ClO-→_______N2+_______Cl-+_______H2O+_______H+
+_______ClO-→_______N2+_______Cl-+_______H2O+_______H+(3)84 消毒液的制取和漂粉精的制取原理相同,都是用氯气和碱反应来制取,84 消毒液所用的碱是氢氧化钠溶液,写出该反应的离子方程式
(4)消毒学专家指出,将 84 消毒液与洁厕灵(主要成分:浓盐酸)一起合并使用,可能会导致使用者的呼吸道伤害。结合有关的化学方程式分析可能的原因
(5)有同学看到某品牌的 84 消毒液的注意事项有指出:“不得将本品与酸性产品同时使用”。这里酸并没有特指盐酸,该品牌的产品说明是否具备科学性呢?说出你的理由,并设计实验进行验证
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】根据所学知识,回答下列问题:
(1)自来水厂用氯气杀菌、消毒,其消毒原理主要是氯气溶于水后生成了 。氯水中存在的离子有
。氯水中存在的离子有___________ ; 的结构式为
的结构式为___________ ; 在溶液中电离本质是
在溶液中电离本质是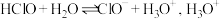 的电子式是
的电子式是___________ 。
(2) 氮的氧化物
氮的氧化物 中,含
中,含 物质的量为
物质的量为 ,则
,则 的摩尔质量为
的摩尔质量为___________ 。
(3)已知反应: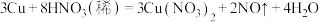 。若有
。若有 被氧化,则被还原的
被氧化,则被还原的 的物质的量是
的物质的量是___________  。
。
(4) 是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备
是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备 的一种方法为在平底烧瓶中加入
的一种方法为在平底烧瓶中加入 固体、足量草酸
固体、足量草酸 、稀硫酸,
、稀硫酸, 水浴加热。已知草酸被氧化为
水浴加热。已知草酸被氧化为 ,该反应的化学方程式为
,该反应的化学方程式为___________ 。
(5)消毒效率是指消毒剂的有效氯。有效氯 有效系数
有效系数 含氯量,其中有效系数
含氯量,其中有效系数 夺取电子数,含氯量
夺取电子数,含氯量 的消毒效率为
的消毒效率为___________ 。
(1)自来水厂用氯气杀菌、消毒,其消毒原理主要是氯气溶于水后生成了
 。氯水中存在的离子有
。氯水中存在的离子有 的结构式为
的结构式为 在溶液中电离本质是
在溶液中电离本质是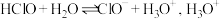 的电子式是
的电子式是(2)
 氮的氧化物
氮的氧化物 中,含
中,含 物质的量为
物质的量为 ,则
,则 的摩尔质量为
的摩尔质量为(3)已知反应:
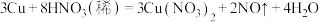 。若有
。若有 被氧化,则被还原的
被氧化,则被还原的 的物质的量是
的物质的量是 。
。(4)
 是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备
是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备 的一种方法为在平底烧瓶中加入
的一种方法为在平底烧瓶中加入 固体、足量草酸
固体、足量草酸 、稀硫酸,
、稀硫酸, 水浴加热。已知草酸被氧化为
水浴加热。已知草酸被氧化为 ,该反应的化学方程式为
,该反应的化学方程式为(5)消毒效率是指消毒剂的有效氯。有效氯
 有效系数
有效系数 含氯量,其中有效系数
含氯量,其中有效系数 夺取电子数,含氯量
夺取电子数,含氯量 的消毒效率为
的消毒效率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】化学与人类生活密切相关。请按要求,回答下列问题:
(1)酸雨的pH小于______________ 。
(2)漂白粉有效成分的化学式为______________ ,其能消毒杀菌是因有强_________ 性。
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为_____________ 。
⑷KA1(SO4)2 • 12H2O的俗名为_________ ,因其溶于水生成______________ (化学式)而具有净水作用。
(5)向一铝制易拉罐中充满CO2后,再往罐中注入足量的质量分数为20%的NaOH溶液,立即严封罐口,不—会儿就发现易拉罐变瘪,再过一会易拉罐又鼓胀起来,解释上述实验现象,易拉罐又鼓胀起来的原因是________________ (用化学方程式表示)。
(1)酸雨的pH小于
(2)漂白粉有效成分的化学式为
(3)小苏打可用于治疗胃酸过多,其反应的离子方程式为
⑷KA1(SO4)2 • 12H2O的俗名为
(5)向一铝制易拉罐中充满CO2后,再往罐中注入足量的质量分数为20%的NaOH溶液,立即严封罐口,不—会儿就发现易拉罐变瘪,再过一会易拉罐又鼓胀起来,解释上述实验现象,易拉罐又鼓胀起来的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】高铁酸钾( )是一种新型绿色消毒剂,其在消毒(发生氧化还原反应)后可形成
)是一种新型绿色消毒剂,其在消毒(发生氧化还原反应)后可形成 胶体,常用于处理饮用水。碱性条件下,高铁酸钾可由次氯酸钾氧化氯化铁制得。
胶体,常用于处理饮用水。碱性条件下,高铁酸钾可由次氯酸钾氧化氯化铁制得。
(1)制备高铁酸钾( )的反应体系中有7种微粒:
)的反应体系中有7种微粒: 、
、 、
、 、
、 、
、 、
、 、
、 。写出制高铁酸钾的离子方程式:
。写出制高铁酸钾的离子方程式:___________ 。
(2)在小烧杯甲中加入25mL蒸馏水,加热至沸腾后,向沸水中滴加饱和 溶液,继续煮沸至溶液呈
溶液,继续煮沸至溶液呈___________ 色,即可制得 胶体。区分溶液和胶体的一种常用的物理方法是
胶体。区分溶液和胶体的一种常用的物理方法是___________ 。
(3)“84”消毒液是日常生活中常用的消毒液,有效成分是 。
。
①用“84”消毒液漂白衣物时,滴加少量白醋漂白效果更好,其原因是___________ ;若用浓盐酸代替白醋,是否可行___________ (填“是”或“否”),原因是___________ 。
②实验室常用烧碱溶液吸收 制
制 溶液,写出反应的化学方程式:
溶液,写出反应的化学方程式:___________ 。
③ 、
、 、
、 均可用作消毒剂,
均可用作消毒剂, 、
、 、
、 消毒效率(消毒效率是指单位质量的氧化剂转移的电子数,转移电子数越多,消毒效率越高)最高的是
消毒效率(消毒效率是指单位质量的氧化剂转移的电子数,转移电子数越多,消毒效率越高)最高的是___________ (填化学式)。
 )是一种新型绿色消毒剂,其在消毒(发生氧化还原反应)后可形成
)是一种新型绿色消毒剂,其在消毒(发生氧化还原反应)后可形成 胶体,常用于处理饮用水。碱性条件下,高铁酸钾可由次氯酸钾氧化氯化铁制得。
胶体,常用于处理饮用水。碱性条件下,高铁酸钾可由次氯酸钾氧化氯化铁制得。(1)制备高铁酸钾(
 )的反应体系中有7种微粒:
)的反应体系中有7种微粒: 、
、 、
、 、
、 、
、 、
、 、
、 。写出制高铁酸钾的离子方程式:
。写出制高铁酸钾的离子方程式:(2)在小烧杯甲中加入25mL蒸馏水,加热至沸腾后,向沸水中滴加饱和
 溶液,继续煮沸至溶液呈
溶液,继续煮沸至溶液呈 胶体。区分溶液和胶体的一种常用的物理方法是
胶体。区分溶液和胶体的一种常用的物理方法是(3)“84”消毒液是日常生活中常用的消毒液,有效成分是
 。
。①用“84”消毒液漂白衣物时,滴加少量白醋漂白效果更好,其原因是
②实验室常用烧碱溶液吸收
 制
制 溶液,写出反应的化学方程式:
溶液,写出反应的化学方程式:③
 、
、 、
、 均可用作消毒剂,
均可用作消毒剂, 、
、 、
、 消毒效率(消毒效率是指单位质量的氧化剂转移的电子数,转移电子数越多,消毒效率越高)最高的是
消毒效率(消毒效率是指单位质量的氧化剂转移的电子数,转移电子数越多,消毒效率越高)最高的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氯气极其相关产品在生产生活中应用广泛。
(1)氯气属于有毒气体,贮氯罐意外泄漏时,消防员会喷洒稀氢氧化钠溶液,其作用是__________ 。(用化学方程式表示)。
实验室常用NaOH溶液吸收多余的氯气,下列也可用于吸收氯气的是_________ (填字母)。
a.NaCl溶液 b.FeSO4溶液 c.KMnO4溶液
(2)家庭中常用消毒液(主要成分NaClO)、洁厕灵(主要成分盐酸)等清洁卫生。某品牌消毒液包装上的说明如下图。
①分析“对金属制品有腐蚀作用”的原因:_______________ 。
②需“密闭保存”的原因:______________ 。
③“与洁厕灵同时使用”会产生有毒的氯气,请写出反应的离子方程式_____________ 。
(3)已知空气中氯气含量超过0.1mg/m3就会引起中毒。某液氯生产车间在一次测定空气中氯气的含量时,测得消耗0.001ml/L Kl溶液100mL,为了判断空气中氯气的含量是否超标,还需要获得的数据是_______ 。
(1)氯气属于有毒气体,贮氯罐意外泄漏时,消防员会喷洒稀氢氧化钠溶液,其作用是
实验室常用NaOH溶液吸收多余的氯气,下列也可用于吸收氯气的是
a.NaCl溶液 b.FeSO4溶液 c.KMnO4溶液
(2)家庭中常用消毒液(主要成分NaClO)、洁厕灵(主要成分盐酸)等清洁卫生。某品牌消毒液包装上的说明如下图。

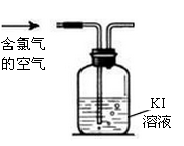
①分析“对金属制品有腐蚀作用”的原因:
②需“密闭保存”的原因:
③“与洁厕灵同时使用”会产生有毒的氯气,请写出反应的离子方程式
(3)已知空气中氯气含量超过0.1mg/m3就会引起中毒。某液氯生产车间在一次测定空气中氯气的含量时,测得消耗0.001ml/L Kl溶液100mL,为了判断空气中氯气的含量是否超标,还需要获得的数据是
您最近一年使用:0次



