以黄铁矿为原料制硫酸会产生大量的废渣,合理利用废渣可以减少环境污染,变废为宝,工业上利用废渣(含Fe2+、Fe3+的硫酸盐及少量CaO和MgO)制备铁红(Fe2O3)和回收(NH4)2SO4,具体生产流程如下:
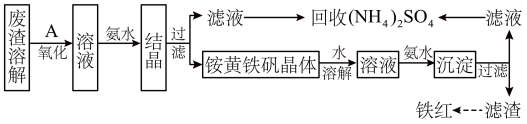
注:铵黄铁钒的化学式为(NH4)2Fe6(SO4)4(OH)12
(1)在废渣溶液操作时,应选用_____ 溶解(填字母)。
A.氨水 B.氢氧化钠溶液 C.盐酸 D.硫酸
(2)物质A是一种氧化剂,工业上最好选______ (供选择使用的有:空气、Cl2、MnO2),其理由是________ (至少写两个理由)。氧化过程中发生反应的离子方程式为__________ 。
(3)铵黄铁矾中可能混有的杂质有Fe(OH)3和__________ 。铵黄铁矾与氨水反应的化学方程式为_______ 。

注:铵黄铁钒的化学式为(NH4)2Fe6(SO4)4(OH)12
(1)在废渣溶液操作时,应选用
A.氨水 B.氢氧化钠溶液 C.盐酸 D.硫酸
(2)物质A是一种氧化剂,工业上最好选
(3)铵黄铁矾中可能混有的杂质有Fe(OH)3和
更新时间:2021-02-08 16:49:09
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】一些氧化物和单质之间可发生如图所示的反应:
其中,氧化物(Ⅰ)是红棕色固体,氧化物(Ⅱ)、(Ⅲ)、(Ⅳ)在反应条件下都是气体.

(1)氧化物(Ⅰ)的化学式(分子式)是_____________ ;氧化物(Ⅱ)的化学式是___________ .
(2)反应①的化学方程式是____________________ ;反应②的化学方程式是__________________ .
其中,氧化物(Ⅰ)是红棕色固体,氧化物(Ⅱ)、(Ⅲ)、(Ⅳ)在反应条件下都是气体.

(1)氧化物(Ⅰ)的化学式(分子式)是
(2)反应①的化学方程式是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐2】某工厂的工业废水中含有大量的FeSO4和CuSO4,为了减少污染并变废为宝,工厂拟定用以下流程从该废水中回收FeSO4和金属Cu。请根据以下流程图,回答相关问题:
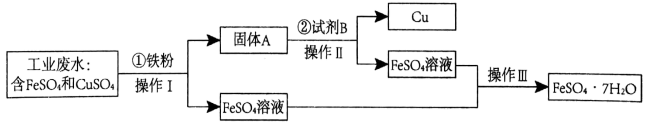
(1)操作Ⅰ和操作Ⅱ的方法是___ 。
(2)为了将CuSO4完全 转化,步骤①加入的铁粉应___ (选填“过量”或“少量”),其对应的化学方程式 为___ 。
(3)固体A的成分是铁和____ (填名称)。
(4)操作Ⅱ加入试剂B的稀溶液,B的化学式为___ ,该物质在该反应中作___ 剂(选填“氧化”或“还原”)。
(5)取1~2mLFeSO4溶液于试管中,滴加几滴NaOH溶液,生成的白色沉淀迅速变为灰绿色,最后变成红褐色,写出该反应中沉淀转化对应的化学反应方程式___ 。
(6)另取1~2mLFeSO4溶液于试管中,滴加几滴氯水,再滴加几滴___ 溶液,溶液变为血红色。

(1)操作Ⅰ和操作Ⅱ的方法是
(2)为了将CuSO4
(3)固体A的成分是铁和
(4)操作Ⅱ加入试剂B的稀溶液,B的化学式为
(5)取1~2mLFeSO4溶液于试管中,滴加几滴NaOH溶液,生成的白色沉淀迅速变为灰绿色,最后变成红褐色,写出该反应中沉淀转化对应的化学反应方程式
(6)另取1~2mLFeSO4溶液于试管中,滴加几滴氯水,再滴加几滴
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
【推荐3】电子工业常用FeCl3溶液腐蚀绝缘板上的铜箔,制造印刷电路板。为改善环境,废物利用,可从腐蚀废液(主要含FeCl3、FeCl2、CuCl2)中回收铜并使腐蚀液再生。处理流程如图:
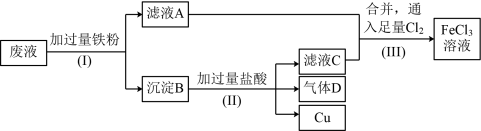
(1)检验废液中是否含有Fe3+所需要的试剂为_____ 。
(2)沉淀B中含有_____ 。
(3)步骤(I)中发生的离子反应方程式有(按反应顺序写出):_____ 。
(4)取少量滤液A于试管中,滴加NaOH溶液,现象是_____ 。
(5)步骤(Ⅲ)中,将氯气换成H2O2也能达到同样的目的。写出H2O2将Fe2+氧化为Fe3+的离子方程式:_____ 。

(1)检验废液中是否含有Fe3+所需要的试剂为
(2)沉淀B中含有
(3)步骤(I)中发生的离子反应方程式有(按反应顺序写出):
(4)取少量滤液A于试管中,滴加NaOH溶液,现象是
(5)步骤(Ⅲ)中,将氯气换成H2O2也能达到同样的目的。写出H2O2将Fe2+氧化为Fe3+的离子方程式:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐1】高铁酸钾(K2FeO4)是一种新型净水剂,制备流程如下。
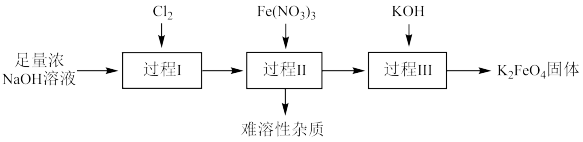
资料:在碱性溶液中的溶解度K2FeO4<Na2FeO4
(1)K2FeO4具有强氧化性,其中铁元素的化合价为______ 价。
(2)过程Ⅰ中制备NaClO的离子方程式为______ 。
(3)除Na2FeO4外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式为______ 。
(4)下列说法正确的是______ (填字母)。
a.过程Ⅱ中生成了Na2FeO4
b.过程Ⅰ~Ⅲ中,需要进行过滤操作的是过程Ⅲ

资料:在碱性溶液中的溶解度K2FeO4<Na2FeO4
(1)K2FeO4具有强氧化性,其中铁元素的化合价为
(2)过程Ⅰ中制备NaClO的离子方程式为
(3)除Na2FeO4外,过程Ⅱ中还可能生成一种含铁元素的难溶性杂质,该物质的化学式为
(4)下列说法正确的是
a.过程Ⅱ中生成了Na2FeO4
b.过程Ⅰ~Ⅲ中,需要进行过滤操作的是过程Ⅲ
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
名校
【推荐2】氯化钠样品中含有少量的杂质Na2SO4,按下列流程进行净化,流程中的( )中是合适的试剂,在[ ]中是实验操作名称。写出有关反应的化学方程式:

(1)操作①、②、③、⑤中所需加入试剂分别为_______ 、______ 、______ 、_____ 。
(2)操作①、④、⑥的操作名称分别为_________ 、_______ 、_______ 。
(3)写出有关的离子反应方程式:
第②步:_____________________________ 。
第⑤步:_____________________________ 。

(1)操作①、②、③、⑤中所需加入试剂分别为
(2)操作①、④、⑥的操作名称分别为
(3)写出有关的离子反应方程式:
第②步:
第⑤步:
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐3】海水是巨大的资源宝库,从海水中提取食盐和溴的过程如图所示:

(1)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为________________ 。
(2)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为________ 。
(3)从理论上考虑,,下列物质也能吸收Br2的是___ (填标号)。
A H2O B NaCl溶液C NaSO3溶液 D FeCl3溶液
(4)查阅资料知,Br2的沸点为58.8℃,微溶于水,有毒性和强腐蚀性。步骤Ⅲ中对蒸馏烧瓶采取的加热方式是_____ 。

(1)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为
(2)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为
(3)从理论上考虑,,下列物质也能吸收Br2的是
A H2O B NaCl溶液C NaSO3溶液 D FeCl3溶液
(4)查阅资料知,Br2的沸点为58.8℃,微溶于水,有毒性和强腐蚀性。步骤Ⅲ中对蒸馏烧瓶采取的加热方式是
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
【推荐1】工业上制备铝一般是从铝土矿(主要成分是Al2O3,含有Fe2O3杂质)中得到纯净的Al2O3,然后电解Al2O3得到铝。下图是从铝土矿中提纯Al2O3的简单示意图。其中涉及到的一个反应是:2NaAlO2+CO2+3H2O=Na2CO3+2Al(OH)3↓。

(1)图示中(1)的实验操作是________ ;图示中(2)加入的试剂__________ 。
(2)试写出下列物质(或溶液中的溶质)的化学式:
B__________________ ;C__________________ ;H________________ ;F______________ 。
(3)写出化学方程式:
①_____________________________________ 。
③_____________________________________ 。
④_________________________________ 。

(1)图示中(1)的实验操作是
(2)试写出下列物质(或溶液中的溶质)的化学式:
B
(3)写出化学方程式:
①
③
④
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
解题方法
【推荐2】实验室利用橄榄石尾矿(主要成分为MgO及少量FeO、Fe2O3、Al2O3等)制备纯净氯化镁晶体(MgCl2·6H2O),实验流程如下:

已知几种金属阳离子形成氢氧化物沉淀时的pH如下表:
回答下列问题:
(1)“浸取”步骤中,能加快浸取速率的方法有____ (任写一种)。
(2)滤渣1为Fe(OH)3,则调节pH的范围为____ 。
(3)“一系列操作”主要包括加入足量盐酸,然后经过蒸发浓缩、冷却结晶、过滤、洗涤,即得到氯化镁晶体。加入足量 盐酸的作用为①溶解滤渣2,②____ 。
(4)准确称取2.000 g氯化镁晶体产品于250 mL锥形瓶中,加50 mL蒸馏水使其完全溶解,在不断振荡下,调节pH并加入合适的指示剂,用0.5000 mol/L的EDTA(在方程式中用Y4−表示)标准溶液进行滴定,其反应原理为Mg2++Y4− = MgY2−,滴定达到终点时消耗EDTA标准溶液的体积为19.00 mL。
①计算产品中MgCl2·6H2O的质量分数。____ (写出计算过程,结果保留三位有效数字)。
②下列滴定操作会导致测量结果偏高的是____ (填字母)。
a.滴定终点时仰视读数
b.锥形瓶洗涤后没有干燥
c.滴定时锥形瓶中有液体溅出
d.滴定前滴定管尖嘴处有气泡,滴定后气泡消失

已知几种金属阳离子形成氢氧化物沉淀时的pH如下表:
| Fe2+ | Fe3+ | Al3+ | Mg2+ | |
| 开始沉淀时 | 7.6 | 2.7 | 4.2 | 9.6 |
| 沉淀完全时 | 9.6 | 3.7 | 5.4 | 11.1 |
回答下列问题:
(1)“浸取”步骤中,能加快浸取速率的方法有
(2)滤渣1为Fe(OH)3,则调节pH的范围为
(3)“一系列操作”主要包括加入足量盐酸,然后经过蒸发浓缩、冷却结晶、过滤、洗涤,即得到氯化镁晶体。加入
(4)准确称取2.000 g氯化镁晶体产品于250 mL锥形瓶中,加50 mL蒸馏水使其完全溶解,在不断振荡下,调节pH并加入合适的指示剂,用0.5000 mol/L的EDTA(在方程式中用Y4−表示)标准溶液进行滴定,其反应原理为Mg2++Y4− = MgY2−,滴定达到终点时消耗EDTA标准溶液的体积为19.00 mL。
①计算产品中MgCl2·6H2O的质量分数。
②下列滴定操作会导致测量结果偏高的是
a.滴定终点时仰视读数
b.锥形瓶洗涤后没有干燥
c.滴定时锥形瓶中有液体溅出
d.滴定前滴定管尖嘴处有气泡,滴定后气泡消失
您最近一年使用:0次
解答题-工业流程题
|
较易
(0.85)
名校
解题方法
【推荐3】纯碱是一种非常重要的化工原料,在玻璃、肥料、合成洗涤剂等工业中有着广泛的应用。
(1)工业上“侯氏制碱法”以NaCl、NH3、CO2及水等为原料制备纯碱,其反应原理为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。生产纯碱的工艺流程示意图如下:

请回答下列问题:
①操作A 的方法是_______ ,得到的NaHCO3晶体中可能含有少量NaCl、NH4Cl等杂质,检验该晶体中是否含有氯离子杂质的操作方法是_______ 。
②该工艺流程中可回收再利用的物质是_______ 。
(2)若称取10.5 g纯净的NaHCO3固体,加热一段时间后,剩余固体的质量为8.02 g。如果把剩余的固体全部加入到100 mL 2 mol·L-1的盐酸中充分反应。求溶液中剩余的盐酸的物质的量浓度(设溶液的体积变化及盐酸的挥发忽略不计)(写出计算过程)。_______
(1)工业上“侯氏制碱法”以NaCl、NH3、CO2及水等为原料制备纯碱,其反应原理为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl。生产纯碱的工艺流程示意图如下:

请回答下列问题:
①操作A 的方法是
②该工艺流程中可回收再利用的物质是
(2)若称取10.5 g纯净的NaHCO3固体,加热一段时间后,剩余固体的质量为8.02 g。如果把剩余的固体全部加入到100 mL 2 mol·L-1的盐酸中充分反应。求溶液中剩余的盐酸的物质的量浓度(设溶液的体积变化及盐酸的挥发忽略不计)(写出计算过程)。
您最近一年使用:0次



