(1)使用“84”消毒液(含NaClO)时,按一定比例与水混合,并在空气中浸泡一段时间,使NaClO与H2O及空气中的CO2充分反应,目的是得到消毒效果更好的___________ (填物质名称),将该反应的离子方程式补充完整:___________ ClO-+CO2+H2O=_____+_____。
(2)将铁粉投入到盛有Cu2+、Ag+、Fe3+的溶液中,反应完毕时,若烧杯底部有铁粉剩余,溶液中一定不含的金属离子是___________ ,若烧杯中没有铁粉剩余,则溶液中一定含有的金属离子是___________ ,若溶液中不含有Cu2+时,则一定不含有的金属离子是___________ 。
(2)将铁粉投入到盛有Cu2+、Ag+、Fe3+的溶液中,反应完毕时,若烧杯底部有铁粉剩余,溶液中一定不含的金属离子是
更新时间:2021-03-01 09:38:15
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】已知甲、乙、丙物质分别由H、C、Na、O、Cl、Fe元素中的一种或几种组成。
(1)若甲物质俗称为小苏打,则甲的化学式为_______ 。
(2)若乙物质在空气中迅速变成灰绿色,最后变成红褐色,,则该反应的化学方程式为_______ 。
(3)若丙物质在常温常压下为黄绿色气体,则实验室制取丙的化学方程式为:_______ 。
(4)2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂( )。
)。 的一种制备方法如下。
的一种制备方法如下。

① 中,铁元素的化合价为
中,铁元素的化合价为_______ 价。
②将反应Ⅰ的离子方程式配平:_______ 。
_______ _______
_______ _______
_______ _______
_______ _______
_______
(1)若甲物质俗称为小苏打,则甲的化学式为
(2)若乙物质在空气中迅速变成灰绿色,最后变成红褐色,,则该反应的化学方程式为
(3)若丙物质在常温常压下为黄绿色气体,则实验室制取丙的化学方程式为:
(4)2019年诺贝尔化学奖颁给锂离子电池领域,获奖科学家的重要贡献之一是研发出了电极材料——磷酸亚铁锂(
 )。
)。 的一种制备方法如下。
的一种制备方法如下。
①
 中,铁元素的化合价为
中,铁元素的化合价为②将反应Ⅰ的离子方程式配平:
_______
 _______
_______ _______
_______ _______
_______ _______
_______
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】按要求书写下列反应的化学方程式或离子方程式。
(1)写出Ba(OH)2溶液和H2SO4溶液反应的离子方程式:_________________________
(2)写出K2CO3溶液与足量稀硫酸的反应的离子方程式:_______________________
(3)写出醋酸与氨水反应的离子方程式:_________________________
(4)写出向碳酸钠溶液中通入二氧化碳气体的化学方程式:______________
(5)写过氧化钠与二氧化碳反应的化学方程式:______________________
(1)写出Ba(OH)2溶液和H2SO4溶液反应的离子方程式:
(2)写出K2CO3溶液与足量稀硫酸的反应的离子方程式:
(3)写出醋酸与氨水反应的离子方程式:
(4)写出向碳酸钠溶液中通入二氧化碳气体的化学方程式:
(5)写过氧化钠与二氧化碳反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】A、B是两种常见的无机物,它们分别能与下图中周围4种物质在一定条件下反应:
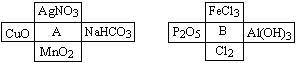
请回答下列问题:
(1)A溶液与B溶液反应的离子方程式_______________________ 。
(2)若A与其周围某物质在一定条件下反应,产物之一是B周围的一种,则此反应的离子方程式为________________
(3)请写出B溶液分别与Cl2、Al(OH)3反应的离子方程式:_________ ,____________
(4)在A、B周围的8种物质中,有些既能与A反应又能与B反应。则这些物质可能是:_______________

请回答下列问题:
(1)A溶液与B溶液反应的离子方程式
(2)若A与其周围某物质在一定条件下反应,产物之一是B周围的一种,则此反应的离子方程式为
(3)请写出B溶液分别与Cl2、Al(OH)3反应的离子方程式:
(4)在A、B周围的8种物质中,有些既能与A反应又能与B反应。则这些物质可能是:
您最近一年使用:0次
【推荐1】已知离子还原性Br﹣<Fe2+<I﹣,则氧化性Fe3+___________ I2(填“>”、“=”或“<”),有一混合溶液,其中只含有Fe2+、Br﹣、I﹣,其中Br﹣、I﹣的个数比为3:4,向该溶液中通入少量氯气,一定会发生的反应的离子方程式是___________ 。如果要使溶液中Br﹣、I﹣的个数比为3:1,通入氯气与溶液中剩余Fe2+的物质的量之比为___________ 。
您最近一年使用:0次
【推荐2】2022年第14号台风“梅花”过后,对环境进行消毒杀菌、获取洁净的饮用水都需要大量消毒剂,开发具有广谱、高效、低毒的杀菌消毒剂是今后发展的趋势。
(1)传统杀菌消毒剂漂白粉在水体中产生强氧化性物质而发挥作用,其化学方程式为:_____ 。
(2)过氧乙酸(CH3COOOH)是一种多用途的新型液体消毒杀菌剂,它具有CH3COOH和H2O2的双重性质。下列物质与过氧乙酸混合,不会使过氧乙酸失效的是_____ (填序号)。
(3)Cl2、H2O2、ClO2(还原产物为Cl-)、O3(1molO3转化为1molO2和1molH2O)等物质常被用作消毒剂。等物质的量的上述物质中消毒效率最高的是_____ (填序号)。
(1)传统杀菌消毒剂漂白粉在水体中产生强氧化性物质而发挥作用,其化学方程式为:
(2)过氧乙酸(CH3COOOH)是一种多用途的新型液体消毒杀菌剂,它具有CH3COOH和H2O2的双重性质。下列物质与过氧乙酸混合,不会使过氧乙酸失效的是
| A.FeCl2溶液 | B.KMnO4溶液 | C.稀盐酸 | D.NaHCO3溶液 |
| A.Cl2 | B.H2O2 | C.O3 | D.ClO2 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】高铁酸钾( )是一种新型绿色消毒剂,其在消毒(发生氧化还原反应)后可形成
)是一种新型绿色消毒剂,其在消毒(发生氧化还原反应)后可形成 胶体,常用于处理饮用水。碱性条件下,高铁酸钾可由次氯酸钾氧化氯化铁制得。
胶体,常用于处理饮用水。碱性条件下,高铁酸钾可由次氯酸钾氧化氯化铁制得。
(1)制备高铁酸钾( )的反应体系中有7种微粒:
)的反应体系中有7种微粒: 、
、 、
、 、
、 、
、 、
、 、
、 。写出制高铁酸钾的离子方程式:
。写出制高铁酸钾的离子方程式:___________ 。
(2)在小烧杯甲中加入25mL蒸馏水,加热至沸腾后,向沸水中滴加饱和 溶液,继续煮沸至溶液呈
溶液,继续煮沸至溶液呈___________ 色,即可制得 胶体。区分溶液和胶体的一种常用的物理方法是
胶体。区分溶液和胶体的一种常用的物理方法是___________ 。
(3)“84”消毒液是日常生活中常用的消毒液,有效成分是 。
。
①用“84”消毒液漂白衣物时,滴加少量白醋漂白效果更好,其原因是___________ ;若用浓盐酸代替白醋,是否可行___________ (填“是”或“否”),原因是___________ 。
②实验室常用烧碱溶液吸收 制
制 溶液,写出反应的化学方程式:
溶液,写出反应的化学方程式:___________ 。
③ 、
、 、
、 均可用作消毒剂,
均可用作消毒剂, 、
、 、
、 消毒效率(消毒效率是指单位质量的氧化剂转移的电子数,转移电子数越多,消毒效率越高)最高的是
消毒效率(消毒效率是指单位质量的氧化剂转移的电子数,转移电子数越多,消毒效率越高)最高的是___________ (填化学式)。
 )是一种新型绿色消毒剂,其在消毒(发生氧化还原反应)后可形成
)是一种新型绿色消毒剂,其在消毒(发生氧化还原反应)后可形成 胶体,常用于处理饮用水。碱性条件下,高铁酸钾可由次氯酸钾氧化氯化铁制得。
胶体,常用于处理饮用水。碱性条件下,高铁酸钾可由次氯酸钾氧化氯化铁制得。(1)制备高铁酸钾(
 )的反应体系中有7种微粒:
)的反应体系中有7种微粒: 、
、 、
、 、
、 、
、 、
、 、
、 。写出制高铁酸钾的离子方程式:
。写出制高铁酸钾的离子方程式:(2)在小烧杯甲中加入25mL蒸馏水,加热至沸腾后,向沸水中滴加饱和
 溶液,继续煮沸至溶液呈
溶液,继续煮沸至溶液呈 胶体。区分溶液和胶体的一种常用的物理方法是
胶体。区分溶液和胶体的一种常用的物理方法是(3)“84”消毒液是日常生活中常用的消毒液,有效成分是
 。
。①用“84”消毒液漂白衣物时,滴加少量白醋漂白效果更好,其原因是
②实验室常用烧碱溶液吸收
 制
制 溶液,写出反应的化学方程式:
溶液,写出反应的化学方程式:③
 、
、 、
、 均可用作消毒剂,
均可用作消毒剂, 、
、 、
、 消毒效率(消毒效率是指单位质量的氧化剂转移的电子数,转移电子数越多,消毒效率越高)最高的是
消毒效率(消毒效率是指单位质量的氧化剂转移的电子数,转移电子数越多,消毒效率越高)最高的是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】以化合价为纵坐标,物质类别为横坐标的图像称为“价—类”二维图。如图是氯元素的部分“价—类”二维图。

回答下列问题:
(1)Cl2呈________ 色,工业上干燥的Cl2贮存在________ 中。
(2)Y的化学式为________ 。已知反应:2ClO2+2NaOH=NaClO2+NaClO3+H2O,则ClO2________ (填“是”或“不是”)酸性氧化物。
(3)Cl2转化成T和HCl的离子方程式为________ 。
(4)实验室制备Cl2的化学方程式为________ 。
(5)除去Cl2中的HCl和水蒸气杂质,依次通过的试剂是________ 、________ 。
(6)已知酸性强弱:H2CO3>HClO>HCO 。向一定量的漂白液中通入少量CO2气体,发生反应的离子方程式为
。向一定量的漂白液中通入少量CO2气体,发生反应的离子方程式为________ 。

回答下列问题:
(1)Cl2呈
(2)Y的化学式为
(3)Cl2转化成T和HCl的离子方程式为
(4)实验室制备Cl2的化学方程式为
(5)除去Cl2中的HCl和水蒸气杂质,依次通过的试剂是
(6)已知酸性强弱:H2CO3>HClO>HCO
 。向一定量的漂白液中通入少量CO2气体,发生反应的离子方程式为
。向一定量的漂白液中通入少量CO2气体,发生反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
(1)所含铁元素既有氧化性又有还原性的物质是________ (用字母代号填)。
A.Fe B.FeCl3 C.FeSO4 D.Fe2O3
(2)向沸水中逐滴滴加1 mol/L FeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是________ nm。
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:______________________________ 。
(1)所含铁元素既有氧化性又有还原性的物质是
A.Fe B.FeCl3 C.FeSO4 D.Fe2O3
(2)向沸水中逐滴滴加1 mol/L FeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】向100 mL 浓度均为1 mol·L-1的Fe2(SO4)3和CuSO4的混合溶液中加入一定量铁粉,充分反应后针对下列情况填空,忽略溶液体积的变化。(已知:氧化性Fe3+>Cu2+>Fe2+)
(1)反应完毕后,无固体沉积物存在,则溶液中一定含有的阳离子为___________ 。
(2)无固体沉积物存在时溶液中发生反应的离子方程为___________ 。
(3)该溶液最多能够溶解铁粉的质量为___________ g。
(4)当Cu2+恰好反应后溶液中溶质的物质的量浓度为___________ mol·L-1。
(1)反应完毕后,无固体沉积物存在,则溶液中一定含有的阳离子为
(2)无固体沉积物存在时溶液中发生反应的离子方程为
(3)该溶液最多能够溶解铁粉的质量为
(4)当Cu2+恰好反应后溶液中溶质的物质的量浓度为
您最近一年使用:0次



