向100 mL 浓度均为1 mol·L-1的Fe2(SO4)3和CuSO4的混合溶液中加入一定量铁粉,充分反应后针对下列情况填空,忽略溶液体积的变化。(已知:氧化性Fe3+>Cu2+>Fe2+)
(1)反应完毕后,无固体沉积物存在,则溶液中一定含有的阳离子为___________ 。
(2)无固体沉积物存在时溶液中发生反应的离子方程为___________ 。
(3)该溶液最多能够溶解铁粉的质量为___________ g。
(4)当Cu2+恰好反应后溶液中溶质的物质的量浓度为___________ mol·L-1。
(1)反应完毕后,无固体沉积物存在,则溶液中一定含有的阳离子为
(2)无固体沉积物存在时溶液中发生反应的离子方程为
(3)该溶液最多能够溶解铁粉的质量为
(4)当Cu2+恰好反应后溶液中溶质的物质的量浓度为
更新时间:2022-01-08 18:28:16
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】氯气是氯碱工业的重要产品之一,是一种化学性质活泼、用途广泛的物质。化学兴趣小组在打算用二氧化锰和浓盐酸反应,在实验室制备氯气。
(1)氯原子的结构示意图为___ 。氯原子没有达到稳定结构,因为___ 。
(2)写出实验室制备氯气的化学方程式___ ,制备时可以选择的发生装置为___ (选填字母序号)。
A. B.
B. C.
C. D.
D.
(3)标准状况下,某同学先使用足量浓盐酸与2.61g二氧化锰反应,制得氯气的体积为___ L。作为对比,相同条件下他还用10mL12mol/L浓盐酸与足量二氧化锰反应,刚得氯气的体积与前者相比___ (选填“更多”、“相等”、“可少”)。
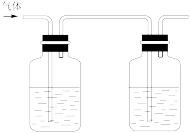
(4)为了制得纯净、干燥的氯气,兴趣小组的成员将发生装置制得的混合气体通过如图的两个洗气瓶进行洗气。左瓶内装有饱和食盐水,作用是___ ;右瓶内装有___ ,可以干燥氯气。
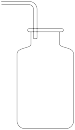
(5)兴趣小组的成负想用如图的装置收集氯气,你认为是否可行?请说明原因。___ 。
(6)盐酸溶液的溶质氯化氢(HCl),也是一种含氯元素的气体。同温同压下,相同体积的氯气与氯化氢气体,所含氛原子个数比为___ ,氯气的质量是氯化氢的___ 倍(保留2位小效)。
(1)氯原子的结构示意图为
(2)写出实验室制备氯气的化学方程式
A.
 B.
B. C.
C. D.
D.
(3)标准状况下,某同学先使用足量浓盐酸与2.61g二氧化锰反应,制得氯气的体积为
(4)为了制得纯净、干燥的氯气,兴趣小组的成员将发生装置制得的混合气体通过如图的两个洗气瓶进行洗气。左瓶内装有饱和食盐水,作用是

(5)兴趣小组的成负想用如图的装置收集氯气,你认为是否可行?请说明原因。

(6)盐酸溶液的溶质氯化氢(HCl),也是一种含氯元素的气体。同温同压下,相同体积的氯气与氯化氢气体,所含氛原子个数比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】 为棕褐色固体,在化工生产中有许多应用。
为棕褐色固体,在化工生产中有许多应用。
(1) 元素有
元素有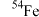 、
、 、
、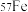 、
、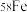 四种核素,它们互为
四种核素,它们互为___________ ,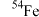 的中子数为
的中子数为___________ ,1个 原子的质量是
原子的质量是___________ 。
(2)书写利用单质反应制备氯化铁的化学方程式,并标出电子转移的方向和数目:___________ 。
(3)氯化铁溶于水后,电离方程式为___________ 。检验氧化铁溶液中的溶质负离子的操作、现象和结论是:___________ 。
(4)将少量饱和 溶液分别滴加到下列物质中,得到三种分散系甲、乙、丙。
溶液分别滴加到下列物质中,得到三种分散系甲、乙、丙。

用红色激光灯分别照射分散系甲和丙,现象的差异为:___________ 。向丙中加入少量稀盐酸,会出现和乙中相同的现象,原因是:___________ 。
(5)5.410g氧化铁晶体( )与100mL
)与100mL  溶液恰好完全沉淀,则
溶液恰好完全沉淀,则 溶液的物质的量浓度为
溶液的物质的量浓度为___________ 。
(6)若用氯化铁晶体( )配制100mL
)配制100mL 
 溶液,下列会造成所配溶液物质的量浓度偏高的是___________。
溶液,下列会造成所配溶液物质的量浓度偏高的是___________。
(7)将饱和氯化铁溶液与小苏打溶液混合时,会产生红褐色沉淀和一种无色无味且能使石灰水变浑浊的气体,则该气体在标况下的密度为___________ 。(保留三位小数)
 为棕褐色固体,在化工生产中有许多应用。
为棕褐色固体,在化工生产中有许多应用。(1)
 元素有
元素有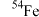 、
、 、
、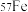 、
、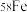 四种核素,它们互为
四种核素,它们互为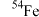 的中子数为
的中子数为 原子的质量是
原子的质量是(2)书写利用单质反应制备氯化铁的化学方程式,并标出电子转移的方向和数目:
(3)氯化铁溶于水后,电离方程式为
(4)将少量饱和
 溶液分别滴加到下列物质中,得到三种分散系甲、乙、丙。
溶液分别滴加到下列物质中,得到三种分散系甲、乙、丙。
用红色激光灯分别照射分散系甲和丙,现象的差异为:
(5)5.410g氧化铁晶体(
 )与100mL
)与100mL  溶液恰好完全沉淀,则
溶液恰好完全沉淀,则 溶液的物质的量浓度为
溶液的物质的量浓度为(6)若用氯化铁晶体(
 )配制100mL
)配制100mL 
 溶液,下列会造成所配溶液物质的量浓度偏高的是___________。
溶液,下列会造成所配溶液物质的量浓度偏高的是___________。| A.定容时,俯视凹液面最低点 |
| B.转移时,有少量液体溅出 |
C. 晶体已部分失水 晶体已部分失水 |
| D.烧杯、玻璃棒未洗涤 |
(7)将饱和氯化铁溶液与小苏打溶液混合时,会产生红褐色沉淀和一种无色无味且能使石灰水变浑浊的气体,则该气体在标况下的密度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某文献资料上记载的相对原子质量数据摘录如表所示:
(1)则65Cu的相对原子质量=____ (保留三位小数)。
常温下,向20mL0.1mol·L-1的硫酸中逐滴加入相同物质的量浓度的Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液的体积关系如图所示:

(2)判断溶液处于A、B、C时的酸碱性,A:____ ;B:____ ;C:____ 。
(3)溶液处于____ 点时的导电性最弱,写出该处发生的化学反应的离子方程式:____ 。
向含有I-和Cl-的稀溶液中滴入AgNO3溶液,产生沉淀的质量与加入AgNO3溶液体积的关系如图所示。
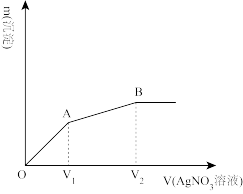
(4)OA段反应生成黄色沉淀,该黄色沉淀的化学式:____ 。
(5)AB段反应生成白色沉淀,写出生成该沉淀的离子方程式:____ 。
(6)原溶液中c(I-):c(Cl-)的比值为:____ (用V1、V2表示)。
| 原子 | 相对原子质量 | 质量数 | 丰度 | 元素的相对原子质量 | 元素的近似相对原子质量 |
| 63Cu | 62.928 | 63 | 69.15% | 63.546 | 63.618 |
| 65Cu | 65 | 30.85% |
常温下,向20mL0.1mol·L-1的硫酸中逐滴加入相同物质的量浓度的Ba(OH)2溶液,生成沉淀的质量与加入Ba(OH)2溶液的体积关系如图所示:

(2)判断溶液处于A、B、C时的酸碱性,A:
(3)溶液处于
向含有I-和Cl-的稀溶液中滴入AgNO3溶液,产生沉淀的质量与加入AgNO3溶液体积的关系如图所示。

(4)OA段反应生成黄色沉淀,该黄色沉淀的化学式:
(5)AB段反应生成白色沉淀,写出生成该沉淀的离子方程式:
(6)原溶液中c(I-):c(Cl-)的比值为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)氮原子的摩尔质量是_______ ;
 的质量是
的质量是_______ ,含有电子数是_______ 。
(2)标准状况下将
 气体溶于水中配成1L溶液,所得盐酸的物质的量浓度是
气体溶于水中配成1L溶液,所得盐酸的物质的量浓度是_______ 。
(3)
 分子中所含质子数与
分子中所含质子数与_______ 个 分子中所含质子数相等。
分子中所含质子数相等。
(4)有以下四种物质:①22g二氧化碳,②标准状况下,33.6L氢气,③ 个氮气分子,④4℃时18mL水。它们所含原子数最多的是
个氮气分子,④4℃时18mL水。它们所含原子数最多的是_______ (填序号),所含电子数最多的是_______ (填序号)。
(5)已知16gA和20gB恰好完全反应生成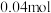 C和31.76gD,则C的摩尔质量为
C和31.76gD,则C的摩尔质量为_______ 。
(6)现有 、
、 、
、 三种物质,它们分别都含有
三种物质,它们分别都含有 氢原子,则三种物质的物质的量之比为
氢原子,则三种物质的物质的量之比为_______ 。
(1)氮原子的摩尔质量是

 的质量是
的质量是(2)标准状况下将

 气体溶于水中配成1L溶液,所得盐酸的物质的量浓度是
气体溶于水中配成1L溶液,所得盐酸的物质的量浓度是(3)

 分子中所含质子数与
分子中所含质子数与 分子中所含质子数相等。
分子中所含质子数相等。(4)有以下四种物质:①22g二氧化碳,②标准状况下,33.6L氢气,③
 个氮气分子,④4℃时18mL水。它们所含原子数最多的是
个氮气分子,④4℃时18mL水。它们所含原子数最多的是(5)已知16gA和20gB恰好完全反应生成
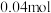 C和31.76gD,则C的摩尔质量为
C和31.76gD,则C的摩尔质量为(6)现有
 、
、 、
、 三种物质,它们分别都含有
三种物质,它们分别都含有 氢原子,则三种物质的物质的量之比为
氢原子,则三种物质的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知12.04×1023个O2分子,则O2的物质的量是________ 。已知CO2的质量是88g,则CO2的物质的量是________ 。标准状况下,已知N2的体积是11.2L,则N2的物质的量是________ 。将4.0gNaOH溶于蒸馏水中,配成2L溶液,则溶质的物质的量浓度是________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ.科学家在研究化学物质时,常对其进行分类,以便对同类物质的组成和性能进行深入研究。物质分类及转化思想贯穿整个化学学科学习的始终。
下列物质:①H2;②熔融氯化钠;③蔗糖;④CO2;⑤稀硝酸;⑥Ba(OH)2固体。能导电的是___________ (填序号,下同);属于电解质的是___________ ;上物质既不是电解质,又不是非电解质的是___________ 。
Ⅱ.有下列六个反应:
A.Cl2+H2O=HCl+HClO
B.Zn+H2SO4=ZnSO4+H2↑
C.2Cu2O+Cu2S 6Cu+SO2↑
6Cu+SO2↑
D.CaCO3 CaO+CO2↑
CaO+CO2↑
E.H2+Cl2 2HCl
2HCl
F.2KClO3 2KCl+3O2↑
2KCl+3O2↑
其中既属于分解反应又属于氧化还原反应的是___________ 。
Ⅲ.K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3+3Cl2+10KOH 2K2FeO4+6KCl+8H2O。在该反应中,还原剂是
2K2FeO4+6KCl+8H2O。在该反应中,还原剂是___________ ,当反应中有1mol K2FeO4生成时,转移电子的数目为___________ 。
Ⅳ.物质的量是化学计算的核心。请按要求完成下列填空:
①已知3.01×1023个X气体分子的质量为8g,则X气体的摩尔质量是___________ 。
②标准状况下,4.48L HCl气体完全溶解在水中,配成100mL溶液,所得溶液的浓度为___________ 。
③在NaCl、MgCl2和MgSO4形成的混合溶液中,c(Na+)=0.10mol•L﹣1,c(Mg2+)=0.25mol•L﹣1,c(Cl﹣)=0.20mol•L﹣1,则c(SO )为
)为___________ 。
④0.3mol SO 离子恰好将0.2mol XO
离子恰好将0.2mol XO 离子还原,SO
离子还原,SO 被氧化成SO
被氧化成SO ,则X元素在还原产物中的化合价是
,则X元素在还原产物中的化合价是___________ 。
下列物质:①H2;②熔融氯化钠;③蔗糖;④CO2;⑤稀硝酸;⑥Ba(OH)2固体。能导电的是
Ⅱ.有下列六个反应:
A.Cl2+H2O=HCl+HClO
B.Zn+H2SO4=ZnSO4+H2↑
C.2Cu2O+Cu2S
 6Cu+SO2↑
6Cu+SO2↑D.CaCO3
 CaO+CO2↑
CaO+CO2↑E.H2+Cl2
 2HCl
2HClF.2KClO3
 2KCl+3O2↑
2KCl+3O2↑其中既属于分解反应又属于氧化还原反应的是
Ⅲ.K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3+3Cl2+10KOH
 2K2FeO4+6KCl+8H2O。在该反应中,还原剂是
2K2FeO4+6KCl+8H2O。在该反应中,还原剂是Ⅳ.物质的量是化学计算的核心。请按要求完成下列填空:
①已知3.01×1023个X气体分子的质量为8g,则X气体的摩尔质量是
②标准状况下,4.48L HCl气体完全溶解在水中,配成100mL溶液,所得溶液的浓度为
③在NaCl、MgCl2和MgSO4形成的混合溶液中,c(Na+)=0.10mol•L﹣1,c(Mg2+)=0.25mol•L﹣1,c(Cl﹣)=0.20mol•L﹣1,则c(SO
 )为
)为④0.3mol SO
 离子恰好将0.2mol XO
离子恰好将0.2mol XO 离子还原,SO
离子还原,SO 被氧化成SO
被氧化成SO ,则X元素在还原产物中的化合价是
,则X元素在还原产物中的化合价是
您最近一年使用:0次
【推荐1】铁是人类较早使用的金属之一、运用铁及其化合物的知识,完成下列问题。
Ⅰ.(1)所含铁元素既有氧化性又有还原性的物质是___________ (填字母,下同)。
A.Fe B.FeCl3
C.FeSO4 D.Fe2O3
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是____
A.NaNO2被氧化
B.药品美蓝是还原剂
C.NaNO2是还原剂
D.药品美蓝被还原
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:___________ 。
Ⅱ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(4)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中FeSO4是___________ (填“氧化剂”或“还原剂”)。
(5)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO 、Cl-、H2O。
、Cl-、H2O。
①碱性条件下,氧化剂和还原剂的物质的量的比为3∶2发生反应,写出并配平湿法制高铁酸钾的离子方程式:___________ 。
②若反应过程中转移了0.3 mol电子,则还原产物的物质的量为___________ mol。
Ⅰ.(1)所含铁元素既有氧化性又有还原性的物质是
A.Fe B.FeCl3
C.FeSO4 D.Fe2O3
(2)血红蛋白(Hb)中的铁元素呈正二价,能与O2分子结合成氧合血红蛋白(HbO)从而有输送氧的能力。NaNO2因具有氧化性能使血红蛋白丧失与O2结合的能力,药品美蓝是其有效的解毒剂,下列说法中正确的是
A.NaNO2被氧化
B.药品美蓝是还原剂
C.NaNO2是还原剂
D.药品美蓝被还原
(3)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
Ⅱ.高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O2、ClO2、KMnO4氧化性更强,无二次污染,工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(4)干法制备高铁酸钠的主要反应为:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中FeSO4是
(5)湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO
 、Cl-、H2O。
、Cl-、H2O。①碱性条件下,氧化剂和还原剂的物质的量的比为3∶2发生反应,写出并配平湿法制高铁酸钾的离子方程式:
②若反应过程中转移了0.3 mol电子,则还原产物的物质的量为
您最近一年使用:0次
【推荐2】I.完成下列氧化还原反应相关问题。
(1)误食NaNO2会使人体血红蛋白中的Fe2+转化为Fe3+而导致中毒,该过程中NaNO2表现出___________ (填“氧化性”或“还原性”)。
(2)已知NaNO2可以与NH4Cl反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目:___________ 。
Ⅱ.KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物ClO2。其反应的化学方程式为2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O
(3)该反应中的氧化产物为___________ (填化学式)。
(4)浓盐酸在该反应中显示出来的性质是___________ (填序号)。
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(5)在碱性条件下加入NaClO3,可将NaCrO2转化为Na2CrO4,ClO 被还原为Cl−,其离子方程式为
被还原为Cl−,其离子方程式为___________ 。还原性:
___________ Cl−(填“>”“<”或“=”)。
(1)误食NaNO2会使人体血红蛋白中的Fe2+转化为Fe3+而导致中毒,该过程中NaNO2表现出
(2)已知NaNO2可以与NH4Cl反应生成氮气和氯化钠,写出该反应的化学反应方程式,并用单线桥表示其电子转移的方向和数目:
Ⅱ.KClO3和浓盐酸在一定温度下反应会生成黄绿色的易爆物ClO2。其反应的化学方程式为2KClO3+4HCl(浓)=2KCl+2ClO2↑+Cl2↑+2H2O
(3)该反应中的氧化产物为
(4)浓盐酸在该反应中显示出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(5)在碱性条件下加入NaClO3,可将NaCrO2转化为Na2CrO4,ClO
 被还原为Cl−,其离子方程式为
被还原为Cl−,其离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】物质类别和核心元素的价态是学习元素及其化合物性质的两个重要认识视角。如图为氯元素的“价-类”二维图。
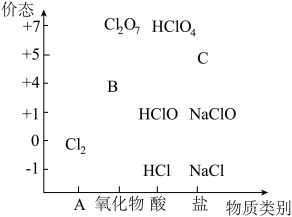
请回答下列问题:
(1)二维图中类别A是_______ ;B可以代替 成为新时代自来水消毒剂,则B是
成为新时代自来水消毒剂,则B是_______ (填化学式,下同);C的焰色试验呈黄色,则C是_______ 。
(2)某同学利用①FeO、② 、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与
、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与_______ (填序号)发生反应;从化合价角度看,盐酸中 具有
具有_______ 性,可能与(填序号)_______ 发生反应。
(3)实验室常用 固体和浓盐酸制取
固体和浓盐酸制取 ,可选用图中的
,可选用图中的_______ (填“A”或“B”)作为发生装置,反应的离子方程式为_______ 。

(4)若将84消毒液与双氧水混用给游泳池消毒,反应产生的 会促进藻类快速生长,使池水变绿,其反应原理为:
会促进藻类快速生长,使池水变绿,其反应原理为: 。
。
①该反应说明氧化性:NaClO_______  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
②用单线桥法表示该反应电子转移的方向和数目:________ 。
(5)一定温度下, 与NaOH溶液反应生成NaCl、NaClO和
与NaOH溶液反应生成NaCl、NaClO和 的混合物,若NaClO与
的混合物,若NaClO与 的系数之比为3∶1,则反应的离子方程式为
的系数之比为3∶1,则反应的离子方程式为_______ 。

请回答下列问题:
(1)二维图中类别A是
 成为新时代自来水消毒剂,则B是
成为新时代自来水消毒剂,则B是(2)某同学利用①FeO、②
 、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与
、③NaOH探究盐酸的性质,进行了如下预测:从物质类别上看,盐酸属于酸,可能与 具有
具有(3)实验室常用
 固体和浓盐酸制取
固体和浓盐酸制取 ,可选用图中的
,可选用图中的
(4)若将84消毒液与双氧水混用给游泳池消毒,反应产生的
 会促进藻类快速生长,使池水变绿,其反应原理为:
会促进藻类快速生长,使池水变绿,其反应原理为: 。
。①该反应说明氧化性:NaClO
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。②用单线桥法表示该反应电子转移的方向和数目:
(5)一定温度下,
 与NaOH溶液反应生成NaCl、NaClO和
与NaOH溶液反应生成NaCl、NaClO和 的混合物,若NaClO与
的混合物,若NaClO与 的系数之比为3∶1,则反应的离子方程式为
的系数之比为3∶1,则反应的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】铁是人类较早使用的金属之一。运用铁及其化合物的知识,完成下列问题。
(1)所含铁元素既有氧化性又有还原性的物质是________ (用字母代号填)。
A.Fe B.FeCl3 C.FeSO4 D.Fe2O3
(2)向沸水中逐滴滴加1 mol/L FeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是________ nm。
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:______________________________ 。
(1)所含铁元素既有氧化性又有还原性的物质是
A.Fe B.FeCl3 C.FeSO4 D.Fe2O3
(2)向沸水中逐滴滴加1 mol/L FeCl3溶液,至液体呈透明的红褐色,该分散系中粒子直径的范围是
(3)电子工业需要用30%的FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板,请写出FeCl3溶液与铜反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】氢氧化铜悬浊液中存在如下平衡:
Cu(OH)2(s)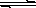 Cu2+(aq)+2OH-(aq),常温下其Ksp=2×10-20则:
Cu2+(aq)+2OH-(aq),常温下其Ksp=2×10-20则:
(1)某硫酸铜溶液里c(Cu2+)=0.02mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH大于______ 。
(2)除去CuCl2溶液中少量的Fe2+,可以按照下面的流程进行:
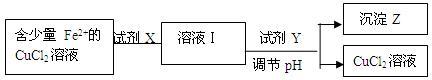
已知Fe2+、Cu2+、Fe3+三种离子开始沉淀和完全沉淀时溶液pH值如下:
①下列物质中适合作为试剂X的是___
A.H2O2 B.KMnO4 C.HNO3 D.Cl2
②加入的Y及调节的pH范围是___
A.CuCO3 3.7~4.3 B.CuO 3.7~6.4
C.NaOH 3.7~4.2 D.NH3·H2O 3.7~4.0
Cu(OH)2(s)
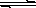 Cu2+(aq)+2OH-(aq),常温下其Ksp=2×10-20则:
Cu2+(aq)+2OH-(aq),常温下其Ksp=2×10-20则:(1)某硫酸铜溶液里c(Cu2+)=0.02mol/L,如要生成Cu(OH)2沉淀,应调整溶液pH大于
(2)除去CuCl2溶液中少量的Fe2+,可以按照下面的流程进行:

已知Fe2+、Cu2+、Fe3+三种离子开始沉淀和完全沉淀时溶液pH值如下:
| 金属离子 | pH | |
| 开始沉淀 | 完全沉淀 | |
| Fe2+ | 7.6 | 9.6 |
| Cu2+ | 4.4 | 6.4 |
| Fe3+ | 2.7 | 3.7 |
①下列物质中适合作为试剂X的是
A.H2O2 B.KMnO4 C.HNO3 D.Cl2
②加入的Y及调节的pH范围是
A.CuCO3 3.7~4.3 B.CuO 3.7~6.4
C.NaOH 3.7~4.2 D.NH3·H2O 3.7~4.0

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】氯化铜是一种广泛用于生产颜料、木材防腐剂等的化工产品。工业上用粗氧化铜(含Fe2O3、FeO、Cu2O以及少量不溶性杂质)为原料制取氯化铜晶体 (CuCl2·2H2O)的为生产流程如下:
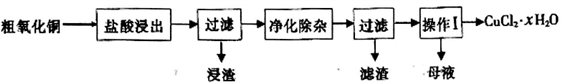
已知:Cu2O在酸性环境中可以生成Cu2+和Cu回答下列问题:
(1)已知“浸渣”中不含铜单质,写出Cu2O在“盐酸浸出”中发生反应的化学方程式:___________________________________________
(2)“盐酸浸出”中,铜的浸出率与浸出时间的关系如下图所示。由图可得出如下变化规律:
①____________________________
②______________________________ 。
(3)“净化除杂”需先加入C1O2,其作用是(用离子方程式表示)______________ 。
然后再调节溶液的pH约为4,可选用的试剂是(填选项字母)______________ 。
A. CuSO4B.CuOC.Cu2(OH)2CO3D.NH3·H2O
(4)“操作I”包含多步实验基本操作,依次是__________ 、洗涤和风干等。工业上常采用无水乙醇代替水进行洗涤的主要原因是______________ 。
(5)为了测定制得的氯化铜晶体(CuCl2·xH2O)中x值,称取ag晶体,加入足量10%的氢氧化钠溶液,过滤、洗涤后,用酒精灯加热至质量不再减轻为止,冷却、称量所得固体质量为bg。计算得x=______________ 。(用含a、b的代数式表示)。

已知:Cu2O在酸性环境中可以生成Cu2+和Cu回答下列问题:
(1)已知“浸渣”中不含铜单质,写出Cu2O在“盐酸浸出”中发生反应的化学方程式:
(2)“盐酸浸出”中,铜的浸出率与浸出时间的关系如下图所示。由图可得出如下变化规律:
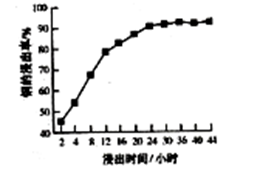
①
②
(3)“净化除杂”需先加入C1O2,其作用是(用离子方程式表示)
然后再调节溶液的pH约为4,可选用的试剂是(填选项字母)
A. CuSO4B.CuOC.Cu2(OH)2CO3D.NH3·H2O
(4)“操作I”包含多步实验基本操作,依次是
(5)为了测定制得的氯化铜晶体(CuCl2·xH2O)中x值,称取ag晶体,加入足量10%的氢氧化钠溶液,过滤、洗涤后,用酒精灯加热至质量不再减轻为止,冷却、称量所得固体质量为bg。计算得x=
您最近一年使用:0次



