为了净化汽车尾气,目前工业上采用CO与NO在催化剂的作用下反应转化为无害气体的工艺: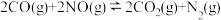 。某实验小组在实验室进行模拟实验。250℃条件下,在5L恒容密闭容器内通入等物质的量的CO和NO,测得n(CO)随时间的变化情况如下表:
。某实验小组在实验室进行模拟实验。250℃条件下,在5L恒容密闭容器内通入等物质的量的CO和NO,测得n(CO)随时间的变化情况如下表:
回答下列问题:
(1)0~2s内用N2表示的反应速率是_______ 。
(2)平衡时CO2的物质的量浓度为_______ 。
(3)达到平衡时,反应前后总压强之比p(前):p(后)=_______ 。
(4)达到平衡时,NO的转化率为_______ 。
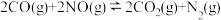 。某实验小组在实验室进行模拟实验。250℃条件下,在5L恒容密闭容器内通入等物质的量的CO和NO,测得n(CO)随时间的变化情况如下表:
。某实验小组在实验室进行模拟实验。250℃条件下,在5L恒容密闭容器内通入等物质的量的CO和NO,测得n(CO)随时间的变化情况如下表:时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(CO)/mol | 0.40 | 0.35 | 0.31 | 0.30 | 0.30 | 0.30 |
回答下列问题:
(1)0~2s内用N2表示的反应速率是
(2)平衡时CO2的物质的量浓度为
(3)达到平衡时,反应前后总压强之比p(前):p(后)=
(4)达到平衡时,NO的转化率为
更新时间:2021-03-07 16:04:01
|
【知识点】 化学平衡题中基于图表数据的相关计算解读
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】完成下列问题。
(1)在T1时,向体积为2L的恒容容器中充入物质的量之和为3mol的CO和H2,发生反应CO(g)+2H2(g)⇌CH3OH(g) △H<0,反应达到平衡时CH3OH(g)的体积分数(φ)与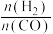 的关系如下图所示。
的关系如下图所示。
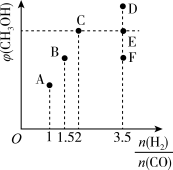
①当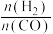 =2时,经过5min达到平衡,CO的转化率为0.6,则该反应的化学平衡常数K=
=2时,经过5min达到平衡,CO的转化率为0.6,则该反应的化学平衡常数K=_______ (保留一位小数)。
②当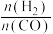 =3.5时,达到平衡后,CH3OH的体积分数可能是图象中的
=3.5时,达到平衡后,CH3OH的体积分数可能是图象中的_____ (填“D”“E”或“F”)点。
(2)另一科研小组控制起始时容器中只有amol/LCO和bmol/LH2,测得平衡时混合气体中CH3OH的物质的量分数[φ(CH3OH)]与温度(T)、压强(p)之间的关系如图2所示。

③若恒温(T1)恒容条件下,起始时 ,测得平衡时混合气体的压强为
,测得平衡时混合气体的压强为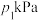 ,则
,则 时该反应的压强平衡常数
时该反应的压强平衡常数 =
=_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,用含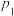 的代数式表示)。
的代数式表示)。
④若在温度为 、压强为
、压强为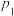 的条件下向密闭容器中加入CO、H2、CH3OH气体的物质的量之比为2∶1∶2,则反应开始时
的条件下向密闭容器中加入CO、H2、CH3OH气体的物质的量之比为2∶1∶2,则反应开始时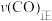
_______  (填“>”、“<”、“=”或“无法确定”)。
(填“>”、“<”、“=”或“无法确定”)。
(1)在T1时,向体积为2L的恒容容器中充入物质的量之和为3mol的CO和H2,发生反应CO(g)+2H2(g)⇌CH3OH(g) △H<0,反应达到平衡时CH3OH(g)的体积分数(φ)与
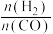 的关系如下图所示。
的关系如下图所示。
①当
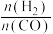 =2时,经过5min达到平衡,CO的转化率为0.6,则该反应的化学平衡常数K=
=2时,经过5min达到平衡,CO的转化率为0.6,则该反应的化学平衡常数K=②当
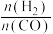 =3.5时,达到平衡后,CH3OH的体积分数可能是图象中的
=3.5时,达到平衡后,CH3OH的体积分数可能是图象中的(2)另一科研小组控制起始时容器中只有amol/LCO和bmol/LH2,测得平衡时混合气体中CH3OH的物质的量分数[φ(CH3OH)]与温度(T)、压强(p)之间的关系如图2所示。

③若恒温(T1)恒容条件下,起始时
 ,测得平衡时混合气体的压强为
,测得平衡时混合气体的压强为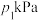 ,则
,则 时该反应的压强平衡常数
时该反应的压强平衡常数 =
=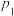 的代数式表示)。
的代数式表示)。④若在温度为
 、压强为
、压强为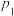 的条件下向密闭容器中加入CO、H2、CH3OH气体的物质的量之比为2∶1∶2,则反应开始时
的条件下向密闭容器中加入CO、H2、CH3OH气体的物质的量之比为2∶1∶2,则反应开始时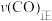
 (填“>”、“<”、“=”或“无法确定”)。
(填“>”、“<”、“=”或“无法确定”)。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】用活性炭还原法可以处理氮氧化物。如反应: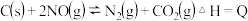
 。在
。在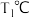 时,反应进行到不同时间测得各物质的浓度如下:
时,反应进行到不同时间测得各物质的浓度如下:
(1)T1℃时,该反应的平衡常数
______
(2)30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是______  答一种即可
答一种即可
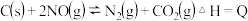
 。在
。在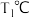 时,反应进行到不同时间测得各物质的浓度如下:
时,反应进行到不同时间测得各物质的浓度如下: | 0 | 10 | 20 | 30 | 40 | 50 | |
| NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
(1)T1℃时,该反应的平衡常数

(2)30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是
 答一种即可
答一种即可
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】随着人们的物质生活水平的不断提高和工业化快速发展,环境污染也日益加重,空气中有毒气体主要包括SO2、CO、NOx、烃类等等。在20 L的密闭容器中按物质的量之比1∶2充入CO和H2,发生反应:CO(g)+2H2(g)⇌CH3OH(g)。测得CO的转化率随温度及不同压强的变化如图所示,P2和195 ℃时n(H2)随时间的变化结果如表所示。

P2及195℃时n(H2)随时间变化
①在0~2 min,平均反应速率υ(CH3OH)=_____ 。(数值用小数形式表示)
②在P2及195 ℃时,该反应的平衡常数Kp=_____ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,结果用含P2的分式表示)。

P2及195℃时n(H2)随时间变化
| t/min | 0 | 1 | 2 | 3 | 4 |
| n(H2)/mol | 8 | 6 | 5 | 4 | 4 |
①在0~2 min,平均反应速率υ(CH3OH)=
②在P2及195 ℃时,该反应的平衡常数Kp=
您最近一年使用:0次



