某酸性工业废水中含有 。光照下,草酸(
。光照下,草酸( )能将其中的
)能将其中的 今转化为
今转化为 。某课题组研究发现,少量铁明矾
。某课题组研究发现,少量铁明矾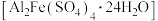 能对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
能对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
(1)在25 下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度的草酸溶液用量,作对比实验,完成以下实验设计表(表中不要留空格)。
下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度的草酸溶液用量,作对比实验,完成以下实验设计表(表中不要留空格)。
测得实验①和②溶液中的 浓度随时间变化关系如图所示。
浓度随时间变化关系如图所示。
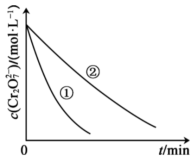
(2)实验①和②的结果表明___________ 对该反应的速率有影响。
(3)该课题组对铁明矾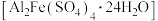 中起催化作用的成分提出如下假设(请你完成假设二和假设三):
中起催化作用的成分提出如下假设(请你完成假设二和假设三):
假设一: 起催化作用;
起催化作用;
假设二:___________ ;
假设三:___________ ;……
(4)请你设计实验验证上述假设一完成下表中内容[除了上述实验提供的试剂外,可供选择的药品有 、
、 、
、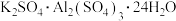 、
、 等。溶液中
等。溶液中 的浓度可用仪器测定]。
的浓度可用仪器测定]。
 。光照下,草酸(
。光照下,草酸( )能将其中的
)能将其中的 今转化为
今转化为 。某课题组研究发现,少量铁明矾
。某课题组研究发现,少量铁明矾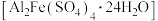 能对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:
能对该反应起催化作用。为进一步研究有关因素对该反应速率的影响,探究如下:(1)在25
 下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度的草酸溶液用量,作对比实验,完成以下实验设计表(表中不要留空格)。
下,控制光照强度、废水样品初始浓度和催化剂用量相同,调节不同的初始pH和一定浓度的草酸溶液用量,作对比实验,完成以下实验设计表(表中不要留空格)。| 实验编号 | 初始pH | 废水样品体积/mL | 草酸溶液体积/mL | 蒸馏水体积/mL |
| ① | 4 | 10 | 30 | |
| ② | 5 | 60 | 10 | |
| ③ | 60 | 20 |
测得实验①和②溶液中的
 浓度随时间变化关系如图所示。
浓度随时间变化关系如图所示。
(2)实验①和②的结果表明
(3)该课题组对铁明矾
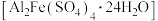 中起催化作用的成分提出如下假设(请你完成假设二和假设三):
中起催化作用的成分提出如下假设(请你完成假设二和假设三):假设一:
 起催化作用;
起催化作用;假设二:
假设三:
(4)请你设计实验验证上述假设一完成下表中内容[除了上述实验提供的试剂外,可供选择的药品有
 、
、 、
、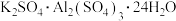 、
、 等。溶液中
等。溶液中 的浓度可用仪器测定]。
的浓度可用仪器测定]。| 实验方案(不要求写具体操作过程) | 预期实验结果和结论 |
| 取 | 反应进行相同时间后:若溶液中的 浓度,则假设一成立;若溶液中的 浓度,则假设一成立;若溶液中的 浓度 浓度 |
14-15高二上·辽宁沈阳·期末 查看更多[4]
(已下线)2013-2014学年辽宁省沈阳市高二上教学质量监测化学试卷(已下线)2014届辽宁省沈阳市高二上教学质量监测化学试卷 广西南宁市2020-2021学年高二上学期期末考试(原理)化学试题安徽省滁州九校2021-2022学年高二上学期第四次调研考试化学试题
更新时间:2021-03-09 11:09:09
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】零价铁活化过硫酸盐耦合类芬顿体系可以产生强氧化性的羟基自由基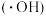 和硫酸根自由基(
和硫酸根自由基( ),被用于氧化降解废水中的抗生素。
),被用于氧化降解废水中的抗生素。
(1)该体系中产生自由基的机理如图所示。 在碱性溶液中可转化为
在碱性溶液中可转化为 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(2)为探究体系中 和
和 降解抗生素的能力,设计了自由基猝灭实验。
降解抗生素的能力,设计了自由基猝灭实验。 是
是 和
和 的猝灭剂,能与
的猝灭剂,能与 、
、 快速反应;
快速反应;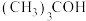 是
是 的猝灭剂,难和
的猝灭剂,难和 反应。零价铁活化过硫酸盐耦合类芬顿体系处理废水时分别加入上述猝灭剂,抗生素残留率与时间的关系如图所示。
反应。零价铁活化过硫酸盐耦合类芬顿体系处理废水时分别加入上述猝灭剂,抗生素残留率与时间的关系如图所示。 反应的原理是
反应的原理是 拔走了甲醇中的一个H原子,生成一个新的自由基,可能产物的相对能量如图所示,该反应最有可能的方程式为
拔走了甲醇中的一个H原子,生成一个新的自由基,可能产物的相对能量如图所示,该反应最有可能的方程式为___________ 。___________ 。
③降解抗生素的自由基主要是哪个,简述理由___________ 。
(3)探究 (PDS)的物质的量分数对抗生素去除率的影响。在
(PDS)的物质的量分数对抗生素去除率的影响。在 的废水中,PDS和H2O2总浓度为
的废水中,PDS和H2O2总浓度为 ,相同时间内,PDS的物质的量分数与抗生素残留率的关系如图所示。
,相同时间内,PDS的物质的量分数与抗生素残留率的关系如图所示。___________ 。
②PDS的物质的量分数降到0%时,抗生素残留率升高的原因是___________ 。
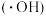 和硫酸根自由基(
和硫酸根自由基( ),被用于氧化降解废水中的抗生素。
),被用于氧化降解废水中的抗生素。(1)该体系中产生自由基的机理如图所示。

① 的结构为
的结构为 ,
, 的结构式为
的结构式为
 在碱性溶液中可转化为
在碱性溶液中可转化为 ,该反应的离子方程式为
,该反应的离子方程式为(2)为探究体系中
 和
和 降解抗生素的能力,设计了自由基猝灭实验。
降解抗生素的能力,设计了自由基猝灭实验。 是
是 和
和 的猝灭剂,能与
的猝灭剂,能与 、
、 快速反应;
快速反应;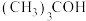 是
是 的猝灭剂,难和
的猝灭剂,难和 反应。零价铁活化过硫酸盐耦合类芬顿体系处理废水时分别加入上述猝灭剂,抗生素残留率与时间的关系如图所示。
反应。零价铁活化过硫酸盐耦合类芬顿体系处理废水时分别加入上述猝灭剂,抗生素残留率与时间的关系如图所示。
 反应的原理是
反应的原理是 拔走了甲醇中的一个H原子,生成一个新的自由基,可能产物的相对能量如图所示,该反应最有可能的方程式为
拔走了甲醇中的一个H原子,生成一个新的自由基,可能产物的相对能量如图所示,该反应最有可能的方程式为
③降解抗生素的自由基主要是哪个,简述理由
(3)探究
 (PDS)的物质的量分数对抗生素去除率的影响。在
(PDS)的物质的量分数对抗生素去除率的影响。在 的废水中,PDS和H2O2总浓度为
的废水中,PDS和H2O2总浓度为 ,相同时间内,PDS的物质的量分数与抗生素残留率的关系如图所示。
,相同时间内,PDS的物质的量分数与抗生素残留率的关系如图所示。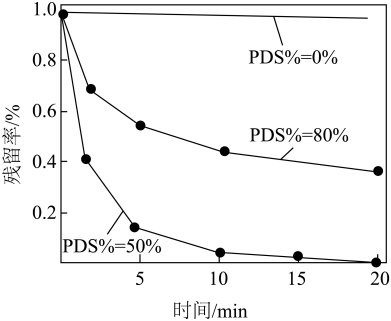
②PDS的物质的量分数降到0%时,抗生素残留率升高的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】I.H2O2不稳定、易分解,Fe3+、Cu2+等对其分解起催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组同学分别设计了如图甲、乙两种实验装置。

(1)A仪器的名称为_______ 。
(2)若利用图甲装置,可通过观察_______ 现象,从而定性比较得出结论。
(3)有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是_____ 。
(4)若利用乙实验可进行定量分析,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是_______ 。
II.KI溶液在酸性条件下能被氧气氧化为I2。现有以下实验记录,回答:
(5)该实验的目的是_______ 。
(6)实验试剂除了1mol/LKI溶液、0.1mol/LH2SO4溶液外,还需要的试剂是_____
(7)由上述实验记录可得出的结论是_______ 。

(1)A仪器的名称为
(2)若利用图甲装置,可通过观察
(3)有同学提出将FeCl3改为Fe2(SO4)3更为合理,其理由是
(4)若利用乙实验可进行定量分析,实验时均以生成40 mL气体为准,其他可能影响实验的因素均已忽略,实验中还需要测量的数据是
II.KI溶液在酸性条件下能被氧气氧化为I2。现有以下实验记录,回答:
| 实验编号 | ① | ② | ③ | ④ | ⑤ |
| 温度/℃ | 30 | 40 | 50 | 60 | 70 |
| 显色时间/s | 160 | 80 | 40 | 20 | 10 |
(6)实验试剂除了1mol/LKI溶液、0.1mol/LH2SO4溶液外,还需要的试剂是
(7)由上述实验记录可得出的结论是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】某温度下,在一个2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白:

(1)从开始至2 min,X的平均反应速率为___________ 。
(2)该反应的化学方程式为___________ 。
(3)1 min时,v(正)___________ v(逆),2 min时,v(正)___________ v(逆)。(填“ ”或“
”或“ ”或“
”或“ ”)。
”)。
(4)上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(X)=9 mol/(L·min),乙中v(Y)=0.5 mol/(L·s),则___________ 中反应更快。
(5)若X、Y、Z均为气体,在2 min时,向容器中通入氩气(容器体积不变),X的化学反应速率将_______ ,若加入适合的催化剂,Y的化学反应速率将______ (填“变大”或“不变”或“变小”)。

(1)从开始至2 min,X的平均反应速率为
(2)该反应的化学方程式为
(3)1 min时,v(正)
 ”或“
”或“ ”或“
”或“ ”)。
”)。(4)上述反应在甲、乙两个相同容器内同时进行,分别测得甲中v(X)=9 mol/(L·min),乙中v(Y)=0.5 mol/(L·s),则
(5)若X、Y、Z均为气体,在2 min时,向容器中通入氩气(容器体积不变),X的化学反应速率将
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】合成氨和制硫酸是中学阶段重要的化工生产反应。
(1)硫酸工业生产中接触室内发生的反应方程式为___ ;在实际生产过程中,操作温度选定400-500摄氏度,压强采用常压的原因分别是___ 。
(2)合成氨反应生成的氨气可用于工业制纯碱,写出以氨气、氯化钠、二氧化碳、水为原料制备纯碱的化学方程式___ 、___ 。
(3)合成氨每生成1g液氨,放出QkJ的热量,写出热化学反应方程式___ 。
(4)常用浓氨水来检查输氯管道是否泄漏,泄漏处会观察到大量的白烟(NH4Cl),还生成一种无色无味的单质气体,写出此反应的化学方程式并标出电子转移的方向和数目____ ,该反应中被还原的是___ ,还原产物是___ 。
(1)硫酸工业生产中接触室内发生的反应方程式为
(2)合成氨反应生成的氨气可用于工业制纯碱,写出以氨气、氯化钠、二氧化碳、水为原料制备纯碱的化学方程式
(3)合成氨每生成1g液氨,放出QkJ的热量,写出热化学反应方程式
(4)常用浓氨水来检查输氯管道是否泄漏,泄漏处会观察到大量的白烟(NH4Cl),还生成一种无色无味的单质气体,写出此反应的化学方程式并标出电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】工业合成氨的适宜条件
| 外部条件 | 工业合成氨的适宜条件 |
| 压强 | |
| 温度 | |
| 催化剂 | 使用 |
| 浓度 | 氨及时从混合气中分离出去,剩余气体 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】研究化学反应的快慢和限度具有十分重要的意义。回答下列问题:
(1)反应2SO2(g) + O2(g) 2SO3(g)是制备硫酸的重要反应,该反应为放热反应。降低温度,逆反应的速率
2SO3(g)是制备硫酸的重要反应,该反应为放热反应。降低温度,逆反应的速率_________ ;使用催化剂V2O5,正反应的速率__________ (以上填“增加”、“不变”或“减小”)。
(2)常温下,实验室用100 mL 6.0 mol·L-1硫酸跟足量锌粉反应制取氢气。
①为降低反应进行的速率,又不影响生成氢气的量,可向反应物中加入____ (填序号 )。
A.CH3COONa固体 B.KNO3固体
C.K2SO4溶液 D.KHSO4溶液
②向溶液中滴加少量硫酸铜溶液,反应速率加快,原因是___________________ 。
(3)一定温度下,在体积固定的密闭容器中,有色气体N与无色气体M的物质的量随时间变化曲线如图所示。反应达平衡的时间是____________ ,该反应的化学方程式可表示为______________________________ ,

下列说法中能够判定该反应处于平衡状态的是______________ (填 序号)
A.容器的压强不再变化 B.气体的颜色不再变化
C.每反应2 mol的N生成1 mol的M D.气体的密度不再发生变化
(1)反应2SO2(g) + O2(g)
 2SO3(g)是制备硫酸的重要反应,该反应为放热反应。降低温度,逆反应的速率
2SO3(g)是制备硫酸的重要反应,该反应为放热反应。降低温度,逆反应的速率(2)常温下,实验室用100 mL 6.0 mol·L-1硫酸跟足量锌粉反应制取氢气。
①为降低反应进行的速率,又不影响生成氢气的量,可向反应物中加入
A.CH3COONa固体 B.KNO3固体
C.K2SO4溶液 D.KHSO4溶液
②向溶液中滴加少量硫酸铜溶液,反应速率加快,原因是
(3)一定温度下,在体积固定的密闭容器中,有色气体N与无色气体M的物质的量随时间变化曲线如图所示。反应达平衡的时间是

下列说法中能够判定该反应处于平衡状态的是
A.容器的压强不再变化 B.气体的颜色不再变化
C.每反应2 mol的N生成1 mol的M D.气体的密度不再发生变化
您最近一年使用:0次



