现有原子序数依次增大且小于20的四种主族元素X、Y、Z、W,该四种元素的最外层电子数之和等于18,其中X、Y原子最外层电子数分别是其自身电子层数的2倍、3倍,W的单质会与水剧烈反应,W的简单离子的电子层结构与Z的简单离子的电子层结构相同,Z单质能使湿润的红色布条褪色。
请回答下列问题:
(1)Y的一种单质具有强氧化性,常用作漂白剂和消毒剂,其名称为___________ ,化合物XZ4的电子式为___________ 。
(2)W的单质与水反应的离子方程式为___________ 。
(3)X、Y的最简单氢化物的稳定性由强到弱的顺序为___________ (用氢化物的化学式表示)。
(4)X、Y、Z、W的原子半径由大到小的顺序为___________ (用元素符号表示)。
请回答下列问题:
(1)Y的一种单质具有强氧化性,常用作漂白剂和消毒剂,其名称为
(2)W的单质与水反应的离子方程式为
(3)X、Y的最简单氢化物的稳定性由强到弱的顺序为
(4)X、Y、Z、W的原子半径由大到小的顺序为
更新时间:2021-04-06 17:22:30
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
【推荐1】已知五种元素的原子序数的大小顺序为C>A>B>D>E,A、C同周期,B、C同主族;A与B形成的离子化合物A2B中所含阴、阳离子的电子数相同,其电子总数为30;D和E可形成4核10个电子分子。试回答下列问题:
(1)写出下列元素的符号:A_______ ,B_______ ,C_______ ,D_______ ,E_______
(2)用电子式表示离子化合物A2B的形成过程:_______
(3)写出D、C、E形成的离子化合物的化学式:_______
(1)写出下列元素的符号:A
(2)用电子式表示离子化合物A2B的形成过程:
(3)写出D、C、E形成的离子化合物的化学式:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】下表列出了①~⑩号元素在元素周期表中的位置:
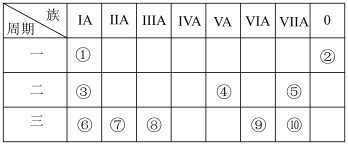
回答下列问题:
(1)①~⑩中,元素的化学性质最不活泼的是_____ (填元素符号,下同)。上述10种元素中,属于金属元素的有_______ 。
(2)写出①与④以原子个数比3:1形成的化合物的电子式:_________ 。
(3)元素④、⑤、⑩分别和①组成的简单化合物中,最稳定的是_______ (填化学式)。
(4)从元素原子得、失电子的角度看,⑤的单质具有_______ (填“氧化性”或“还原性”)。
(5)在盛有氢氧化钠溶液的小烧杯中通入元素⑩的单质,发生反应的离子方程式为_________ 。
(6)请从原子结构的角度解释元素⑥的金属性比元素③的金属性强的原因是________ 。

回答下列问题:
(1)①~⑩中,元素的化学性质最不活泼的是
(2)写出①与④以原子个数比3:1形成的化合物的电子式:
(3)元素④、⑤、⑩分别和①组成的简单化合物中,最稳定的是
(4)从元素原子得、失电子的角度看,⑤的单质具有
(5)在盛有氢氧化钠溶液的小烧杯中通入元素⑩的单质,发生反应的离子方程式为
(6)请从原子结构的角度解释元素⑥的金属性比元素③的金属性强的原因是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】元素周期表的形式多种多样,扇形元素周期表的一部分(1~36号元素)如图所示,对比中学常见的元素周期表,思考扇形元素周期表的填充规律。请用准确的化学符号和用语 回答下列问题:

(1)元素1在元素周期表中的位置_______ 。
(2)比较f、o、k简单离子的半径,由大到小的顺序是_______ (用离子符号表示)。
(3)b与e组成的化合物中,含有非极性共价键的化合物的电子式_______ 。
(4)i的最高价氧化物对应水化物的化学式_______ ,比较i、d最简单氢化物的稳定性_______ (用化学式表示)。
(5)比较m、f、g的金属性强弱,由强到弱的顺序是_______ (用元素符号表示)
(6)比较j和h的非金属性强弱,设计简单的实验方案_______ 。

(1)元素1在元素周期表中的位置
(2)比较f、o、k简单离子的半径,由大到小的顺序是
(3)b与e组成的化合物中,含有非极性共价键的化合物的电子式
(4)i的最高价氧化物对应水化物的化学式
(5)比较m、f、g的金属性强弱,由强到弱的顺序是
(6)比较j和h的非金属性强弱,设计简单的实验方案
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】A、B、C、D、E五种物质的焰色反应都显黄色,其中A为银白色质软的低熔点金属单质,B为淡黄色的固体化合物,A、B与水反应都有气体放出,A与水反应放出的气体具有还原性,而B与水反应生成的气体可供给呼吸,同时都生成溶液C,C与适量的CO2反应生成D,D溶液与过量的CO2反应生成E,E加热能变成D。
写出A~E的化学式:A___________ 、B___________ 、C___________ 、D___________ 、E___________ 。
写出A~E的化学式:A
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐2】如图所示,下列各项变化的未知物焰色反应均呈黄色,E为淡黄色粉末。
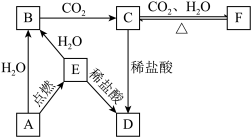
回答下列问题。
(1)写出A→B的化学方程式,_____________________ 。
(2)写出C→D的离子方程式,_____________ 。
(3)当C溶液中含有杂质F,如何除杂:____________________ ,反应涉及的离子方程式_____________ 。
(4)E与CO2反应气体体积减小了11.2L(标准状况下),反应中转移电子的数目是___________ 。
(5)在一密闭容器中有CO、H2、O2共16.5 g和足量的E,用电火花引燃,使其完全反应,固体增重7.5 g,则原混合气体中O2的质量是__________ g。

回答下列问题。
(1)写出A→B的化学方程式,
(2)写出C→D的离子方程式,
(3)当C溶液中含有杂质F,如何除杂:
(4)E与CO2反应气体体积减小了11.2L(标准状况下),反应中转移电子的数目是
(5)在一密闭容器中有CO、H2、O2共16.5 g和足量的E,用电火花引燃,使其完全反应,固体增重7.5 g,则原混合气体中O2的质量是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐3】某课外活动小组为了检验钠与水反应的产物,设计如图装置(夹持装置省略)。首先在U形管内加入少量煤油和几粒钠块,再从U形管高端加入水(含有酚酞),赶出空气,一段时间后加热铜丝。

根据反应中观察到的现象,回答下列问题:
(1)金属钠的变化现象________ 。
(2)U形管中溶液的颜色_____ ,说明有__________ 生成。
(3)铜丝的变化现象____________ ,说明有________ 生成;若去掉后面的装置,简述检验气体的方法____
(4)若a g钠与b mL水完全反应,则该溶液溶质的质量分数是_______ 。

根据反应中观察到的现象,回答下列问题:
(1)金属钠的变化现象
(2)U形管中溶液的颜色
(3)铜丝的变化现象
(4)若a g钠与b mL水完全反应,则该溶液溶质的质量分数是
您最近一年使用:0次
解答题-实验探究题
|
较易
(0.85)
解题方法
【推荐1】请按要求分别设计一个简单易行的验证实验。
(1)验证钠和镁的金属性强弱__________________________ ;
(2)验证硫和氯的非金属性强弱________________________ 。
(1)验证钠和镁的金属性强弱
(2)验证硫和氯的非金属性强弱
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】下表是现行中学化学教科书中元素周期表的一部分,除标出的元素外,表中的每个编号表示一种元素,请根据要求回答问题:

(1)④表示的元素是_______ (填元素符号)。
(2)②、③两种元素相比较,原子半径较大的是_______ (填元素符号)。
(3)写出①与⑥两种元素所形成化合物的电子式_______ 。
(4)③和⑤两种元素的非金属性强弱顺序是③_______ (填“<”或“>”)⑤。
(5)④和⑥两种元素组成的化合物中含有的化学键是_______ (填“共价”或“离子)键。

(1)④表示的元素是
(2)②、③两种元素相比较,原子半径较大的是
(3)写出①与⑥两种元素所形成化合物的电子式
(4)③和⑤两种元素的非金属性强弱顺序是③
(5)④和⑥两种元素组成的化合物中含有的化学键是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】下表是元素周期表的一部分,其中列出了①~⑥六种元素在周期表中的位置。
请回答下列问题:
(1)①的元素符号为_______ ;
(2)②的原子半径_______ ⑤的原子半径(选填“>”、“<”或“=”);
(3)③和⑥两元素形成的化合物的化学式为_______ ;
(4)④的最高价氧化物对应的水化物的化学式为_______ ;
(5)⑥的单质与水反应的化学方程式为_______ 。
(6)⑤的最高价氧化物对应的水化物,其浓溶液具有①酸性;②强氧化性;③吸水性;④脱水性等性质,根据题意填空(填序号):
I.将浓硫酸滴到滤纸上,滤纸变黑,是因为浓硫酸具有_______ ;
II.浓H2SO4与Cu反应,体现了浓H2SO4的_______ 。
III.将浓硫酸滴到胆矾上,胆矾变白,是因为浓硫酸具有_______ ;
族 周期 | IA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA |
| 2 | ① | ② | |||||
| 3 | ③ | ④ | ⑤ | ⑥ |
(1)①的元素符号为
(2)②的原子半径
(3)③和⑥两元素形成的化合物的化学式为
(4)④的最高价氧化物对应的水化物的化学式为
(5)⑥的单质与水反应的化学方程式为
(6)⑤的最高价氧化物对应的水化物,其浓溶液具有①酸性;②强氧化性;③吸水性;④脱水性等性质,根据题意填空(填序号):
I.将浓硫酸滴到滤纸上,滤纸变黑,是因为浓硫酸具有
II.浓H2SO4与Cu反应,体现了浓H2SO4的
III.将浓硫酸滴到胆矾上,胆矾变白,是因为浓硫酸具有
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】A、B、C、D、M、N六种短周期主族元素,它们的核电荷数依次增大。A可分别与C、D形成10电子分子,其中B的最外层电子数等于次外层电子数,C原子最外层电子数是次外层电子数的2倍,M的L层电子数为K层和M层电子数之和,D和M同主族。回答下列问题:
(1)元素B的符号和名称分别是________ 、________ ;在周期表中的位置是________ 。
(2)元素C的原子结构示意图为________ 。
(3)元素A分别与C、D形成的10电子分子的稳定性强弱关系为___________ (用化学式表示)。
(4)元素C和M相比,非金属性较强的是________ (用元素符号表示)。
(1)元素B的符号和名称分别是
(2)元素C的原子结构示意图为
(3)元素A分别与C、D形成的10电子分子的稳定性强弱关系为
(4)元素C和M相比,非金属性较强的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐2】元素周期律的发现和元素周期表的诞生,开创了化学科学的新纪元。有关短周期主族元素A、B、C、D、E的相关信息如下表所示。
(1)A的元素符号为___________ ,其原子结构示意图为___________ 。
(2)B在周期表中位于第3周期第___________ 族。
(3)B形成的碱性氧化物的化学式为___________ ,该化合物属于___________ (填“离子”或“共价”)化合物。
(4)依据C、D在周期表中的位置判断:C和D的得电子能力较强的是___________ (填元素符号)。
(5)B、D、E的最高价氧化物对应水化物相互之间均能反应,
①E与B二者的最高价氧化物对应水化物反应的化学方程式为___________ 。
②E与D二者的最高价氧化物对应水化物反应的离子方程式为___________ 。
| 序号 | 相关信息 |
| A | 单质为双原子分子,1个分子中含有14个电子 |
| B | 短周期主族元素中原子半径最大 |
| C | 最高正价与最低负价的绝对值相差6 |
| D | 单质为黄色或淡黄色固体,易溶于 |
| E | M层比K层多1个电子 |
(2)B在周期表中位于第3周期第
(3)B形成的碱性氧化物的化学式为
(4)依据C、D在周期表中的位置判断:C和D的得电子能力较强的是
(5)B、D、E的最高价氧化物对应水化物相互之间均能反应,
①E与B二者的最高价氧化物对应水化物反应的化学方程式为
②E与D二者的最高价氧化物对应水化物反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐3】现有部分短周期元素的性质或原子结构如下表:
(1)写出元素X离子的电子轨道表示式 ___________ 。
(2)写出Y元素最高价氧化物的水化物与NaOH溶液反应的离子方程式___________ 。
(3)写出Z的电子排布式___________ 。
(4)元素T与氯元素相比,非金属性较强的是___________ (用元素符号表示),下列表述中能证明这一事实的是___________ 。
A.气态氢化物的挥发性和稳定性 B.单质分子中的键能
C.两元素单质的氧化性 D.含氧酸的酸性
E.氢化物中X—H键的键长(X代表T和Cl两种元素)
F.两元素在自然界中的存在形式
(5)探寻物质的性质差异性是学习的重要方法之一、T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是___________ (填元素符号),理由是___________ 。
| 元素编号 | 元素性质或原子结构 |
| T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| X | L层p电子数比s电子数多2个 |
| Y | 第三周期元素的简单离子中半径最小 |
| Z | L层有三个未成对电子 |
(2)写出Y元素最高价氧化物的水化物与NaOH溶液反应的离子方程式
(3)写出Z的电子排布式
(4)元素T与氯元素相比,非金属性较强的是
A.气态氢化物的挥发性和稳定性 B.单质分子中的键能
C.两元素单质的氧化性 D.含氧酸的酸性
E.氢化物中X—H键的键长(X代表T和Cl两种元素)
F.两元素在自然界中的存在形式
(5)探寻物质的性质差异性是学习的重要方法之一、T、X、Y、Z四种元素的单质中化学性质明显不同于其他三种单质的是
您最近一年使用:0次



