将19.2g铜粉与一定量的浓硝酸反应,当铜粉完全反应时收集到气体11.2L(标准状况下)。计算:
(1)产生NO、NO2标况下的体积分别是_______ 、_______ 。
(2)所消耗硝酸的物质的量是_______ 。
(1)产生NO、NO2标况下的体积分别是
(2)所消耗硝酸的物质的量是
更新时间:2021-04-12 09:44:03
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】(1)将一定质量的锌粒投入100mL 18.5mol/L的浓硫酸中,待锌粒完全溶解后,测得生成的H2和SO2共33.6L(标准状况),此时溶液中尚余0.1mol H+.计算可知:
①投入锌粒的质量为_____________ g。
②生成的H2和SO2的物质的量之比为_____________ 。
(2)取25.6 g Cu与一定量的某浓度的浓HNO3反应,当铜完全溶解后,收集到产生的NO和NO2混合气体在标准状况下的体积共11.2 L,则:
①消耗硝酸的物质的量为_____________ mol。
②NO的物质的量为_____________ mol,NO2的物质的量为_____________ mol。
③当铜完全溶解时,反应中转移的电子数目为_____________ 。
①投入锌粒的质量为
②生成的H2和SO2的物质的量之比为
(2)取25.6 g Cu与一定量的某浓度的浓HNO3反应,当铜完全溶解后,收集到产生的NO和NO2混合气体在标准状况下的体积共11.2 L,则:
①消耗硝酸的物质的量为
②NO的物质的量为
③当铜完全溶解时,反应中转移的电子数目为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】铜既能与稀硝酸反应,也能与浓硝酸反应,现将32 g Cu投入50 mL 12 mol/L的浓硝酸中,充分反应后,收集到4.48 L(标准状态)NO和NO2的混合气体。(Cu的相对原子质量为64)
(1)被还原硝酸的物质的量是_______ mol。
(2)反应后溶液中有_______ mol NO ,所以,剩余
,所以,剩余_______ (填反应物的化学式),其物质的量是_______ mol。
(3)如果往反应后的体系内再加入100 mL0.4 mol/L的稀硫酸,又会有气体逸出,离子反应方程式为_______ ,产生的气体在标准状况下的体积为_______ mL。
(1)被还原硝酸的物质的量是
(2)反应后溶液中有
 ,所以,剩余
,所以,剩余(3)如果往反应后的体系内再加入100 mL0.4 mol/L的稀硫酸,又会有气体逸出,离子反应方程式为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐1】将1.76g镁铜合金投入20mL一定浓度的硝酸中,合金完全溶解,产生 和
和 混合气体共896mL(不考虑
混合气体共896mL(不考虑 ,体积折算为标准状况下),反应结束后向溶液中加入
,体积折算为标准状况下),反应结束后向溶液中加入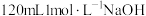 溶液,恰好使溶液中的金属阳离子全部转化为沉淀3.12g。若将盛有896mL该混合气体的容器倒扣在水中,通入一定体积的氧气,恰好可将该混合气体完全转化为
溶液,恰好使溶液中的金属阳离子全部转化为沉淀3.12g。若将盛有896mL该混合气体的容器倒扣在水中,通入一定体积的氧气,恰好可将该混合气体完全转化为 。
。
(1) 和
和 的体积比为
的体积比为______________ ;
(2)原硝酸的浓度为___________  ;
;
(3)通入的 的体积(标准状况下)
的体积(标准状况下)
__________  。
。
 和
和 混合气体共896mL(不考虑
混合气体共896mL(不考虑 ,体积折算为标准状况下),反应结束后向溶液中加入
,体积折算为标准状况下),反应结束后向溶液中加入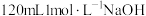 溶液,恰好使溶液中的金属阳离子全部转化为沉淀3.12g。若将盛有896mL该混合气体的容器倒扣在水中,通入一定体积的氧气,恰好可将该混合气体完全转化为
溶液,恰好使溶液中的金属阳离子全部转化为沉淀3.12g。若将盛有896mL该混合气体的容器倒扣在水中,通入一定体积的氧气,恰好可将该混合气体完全转化为 。
。(1)
 和
和 的体积比为
的体积比为(2)原硝酸的浓度为
 ;
;(3)通入的
 的体积(标准状况下)
的体积(标准状况下)
 。
。
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】有硫酸与硝酸的混合液,取出其中10mL,加入足量的BaCl2溶液,将生成的沉淀过滤洗涤,干燥称得质量为4.66g。另取这种溶液10mL与2mol·L-1的NaOH溶液25mL恰好中和。则:
(1)混合液中c(H2SO4)=__ mol·L-1,c(HNO3)=__ mol·L-1
(2)另取10mL的混合液(混合液中的硝酸视为稀硝酸)与0.96g铜粉共热时,产生气体的体积为__ L(标准状况)。
(1)混合液中c(H2SO4)=
(2)另取10mL的混合液(混合液中的硝酸视为稀硝酸)与0.96g铜粉共热时,产生气体的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)合成氨一直是科学家研究的重要课题,已知破坏 有关化学键需要的能量如表所示:
有关化学键需要的能量如表所示:
则反应生成2mol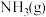 所释放出的热量为
所释放出的热量为___________  。
。
(2)32.0 g Cu 与 100 mL 10.0 mol·L-1的浓硝酸反应,标准状况下测得反应产生的 NO、NO2混合气体 6.72 L,且充分反应后铜仍有剩余。请计算:
①混合气体中 NO 与 NO2的物质的量之比为___________ 。
②向反应后的溶液中滴加稀硫酸可使铜完全溶解,离子方程式为___________ 。若该过程中只有 NO 气体生成,则还能产生 NO 的物质的量为___________ 。
(1)合成氨一直是科学家研究的重要课题,已知破坏
 有关化学键需要的能量如表所示:
有关化学键需要的能量如表所示: |  |  |  |
a | b | c | d |
则反应生成2mol
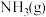 所释放出的热量为
所释放出的热量为 。
。(2)32.0 g Cu 与 100 mL 10.0 mol·L-1的浓硝酸反应,标准状况下测得反应产生的 NO、NO2混合气体 6.72 L,且充分反应后铜仍有剩余。请计算:
①混合气体中 NO 与 NO2的物质的量之比为
②向反应后的溶液中滴加稀硫酸可使铜完全溶解,离子方程式为
您最近一年使用:0次

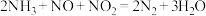 。若反应后得到
。若反应后得到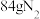 ,理论上需消耗氨气
,理论上需消耗氨气 。
。


