下列说法不正确的是
A. 晶体中存在 晶体中存在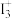 离子, 离子,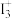 离子的空间构型为V形 离子的空间构型为V形 |
| B.三氯化氮(NCl3)是一种极性分子,NCl3还能再以配位键与Cl-结合 |
| C.PH3和NH3分子中均含有孤电子对,且PH3提供孤电子对的能力强于NH3 |
| D.BeO的晶格能大于MgO,可推测BeCO3的分解温度低于MgCO3 |
更新时间:2021-04-13 11:54:49
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】离子液体是在室温或接近室温时呈液态的盐类物质,应用广泛。1—乙基—3—甲基咪唑四氟硼酸盐离子液体结构如图所示。下列说法错误的是

A.该离子液体中C、N杂化方式均有 和 和 两种 两种 |
| B.阴离子呈正四面体形 |
| C.阳离子中σ键数目是π键数目的10倍 |
| D.该离子液体与水能够形成氢键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列叙述中正确的是
| A.CO、CO2都是极性分子 | B.H2O2、C2H2都是直线型分子 |
| C.CH4、CCl4都是含有极性键的非极性分子 | D.BF3、NCl3都是平面三角形分子 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】短周期主族元素W、X、Y、Z的原子序数依次增大,W、X原子的最外层电子数之比为4∶3,Z原子的核外电子数比X原子多4。下列说法正确的是( )
| A.W、Y、Z的电负性大小顺序一定是Z>Y>W |
| B.Z的氢化物分子间存在氢键 |
| C.Y、Z形成的化合物分子的中心原子可能采取sp3杂化 |
| D.WY2分子中σ键与π键的数目之比一定是2∶1 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】铝离子电池常用离子液体AlCl3/[EMIM]Cl作电解质,其中阴离子有AlCl 、Al2Cl
、Al2Cl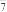 ,阳离子为EMIM+(
,阳离子为EMIM+( ),EMIM+以单个形式存在时可以获得良好的溶解性能。下列说法错误的是
),EMIM+以单个形式存在时可以获得良好的溶解性能。下列说法错误的是
 、Al2Cl
、Al2Cl ,阳离子为EMIM+(
,阳离子为EMIM+( ),EMIM+以单个形式存在时可以获得良好的溶解性能。下列说法错误的是
),EMIM+以单个形式存在时可以获得良好的溶解性能。下列说法错误的是A.EMIM+中存在大π键,表示为π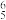 |
B.Al2Cl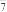 中各原子最外层均达到8电子结构 中各原子最外层均达到8电子结构 |
| C.1mol EMIM+中所含σ键17mol |
| D.为使EMIM+获得良好的溶解性,不能将与N原子相连的-CH3、-C2H5替换为H原子 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】由短周期元素构成的某离子化合物中,一个阳离子和一个阴离子核外电子数之和为20,且阴、阳离子所带电荷相等.下列说法正确的是( )
| A.晶体中阳离子和阴离子数不一定相等 |
| B.晶体中一定只有离子键没有共价键 |
| C.所含元素一定不在同一周期也不在第1周期 |
| D.晶体中阳离子半径一定大于阴离子半径 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
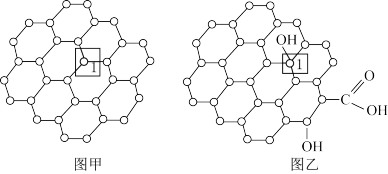
【推荐2】下列对石墨晶体的叙述不正确的是
| A.层状结构,属于混合型晶体 | B.晶体中碳原子个数与C—C键数目比为1:2 |
| C.晶体中的碳原子为sp2杂化 | D.晶体中每个六元环完全占有的碳原子数为2 |
您最近半年使用:0次

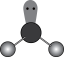
 内部含有极性键、非极性键、配位键和离子键
内部含有极性键、非极性键、配位键和离子键