下列说法错误的是
| A.水汽化和水分解的变化过程中,都需要破坏共价键 |
B. 、 、 晶体中的阴、阳离子个数比分别为 晶体中的阴、阳离子个数比分别为 、 、 |
| C.基态碳原子核外有三种能量不同的电子 |
| D.无水乙醇不可以用于萃取溴水中的溴单质 |
更新时间:2021-04-14 09:36:41
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列各组物质性质的比较中正确的是( )
| A.CH4、CCl4、C60都是含有极性键的非极性分子 |
| B.非金属氢化物的稳定性顺序:H2O>H2S>H2Se,HCl<H2S<PH3 |
| C.弱电解质水溶液导电能力不一定比强电解质水溶液导电能力弱 |
| D.空间利用率:简单立方堆积<体心立方堆积<六方最密堆积<面心立方最密堆积 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知:A、B、C、D、E、F是周期表中前36号元素,A是原子半径最小的元素,B元素基态原子的2p轨道上只有两个电子,C元素的基态原子L层只有2对成对电子,D是元素周期表中电负性最大的元素,E2+的核外电子排布与Ar原子相同,F的核电荷数是D和E的核电荷数之和。
请回答下列问题:
(1)分子式为BC2的立体结构为____ ;F2+的核外电子排布式为____ 。
(2)A分别与B、C形成的最简单化合物的稳定性:B____ C(填“大于”或“小于”);A、C两元素可组成原子个数比为1∶1的化合物,C原子的杂化类型为____ 。
(3)A2C所形成的晶体类型为____ ;F单质形成的晶体类型为____ ,其采用的堆积方式为____ 。
(4)F元素氧化物的熔点比其硫化物的____ (填“高”或“低”),请解释其原因_______ 。
请回答下列问题:
(1)分子式为BC2的立体结构为
(2)A分别与B、C形成的最简单化合物的稳定性:B
(3)A2C所形成的晶体类型为
(4)F元素氧化物的熔点比其硫化物的
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】A、B、C、D、E五种元素的原子序数依次增大。已知A、B、C、D是短周期元素中的四种非金属元素,A元素的原子形成的离子就是一个质子,C、D在元素周期表中处于相邻的位置,它们的单质在常温下均为无色气体,B的一种核素在考古时常用来鉴定一些文物的年代,E是地壳中含量最高的金属元素。下列说法正确的是
| A.A、B、C、D均是非金属元素,所以它们之间只能形成共价化合物 |
| B.化合物BD2是直线型分子,若遇E同周期的金属单质着火均可用BD2灭火 |
| C.用E单质作阳极,石墨电极作阴极电解NaHCO3 溶液,电解一开始就会在阴极区出现白色沉淀 |
| D.A、C两元素可能形成原子个数比(A:C)为3:1、2:1以及1:1的化合物 |
您最近一年使用:0次
【推荐1】下列对分子结构及其性质的解释中,不正确的是
| A.乙烷难溶于水、溴易溶于四氯化碳都可用相似相溶原理解释 |
B.酸性: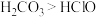 ,是因为 ,是因为 分子中的氢原子数目比HClO多 分子中的氢原子数目比HClO多 |
C.羟基乙酸 不属于手性分子,因其分子中不存在手性碳原子 不属于手性分子,因其分子中不存在手性碳原子 |
D. 的沸点高于 的沸点高于 ,因乙醇分子中含—OH,能形成分子间氢键 ,因乙醇分子中含—OH,能形成分子间氢键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】共价键、离子键、范德华力和氢键都是微观粒子之间的不同作用力,下列物质:①Na2O2②冰 ③金刚石 ④碘单质 ⑤CaCl2⑥白磷,其中只含有两种作用力的组合是
| A.①④⑥ | B.①③⑥ |
| C.②④⑥ | D.①②③⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法中正确的是
| A.干冰气化和碘升华克服的作用力相同 |
| B.甲酸甲酯和乙酸相对分子质量相同,熔点相近 |
| C.氯化钠和氯化氢熔化时,破坏的都是离子键 |
| D.碘化氢的范德华力比溴化氢的大,碘化氢稳定性强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.H2O的沸点比H2S高,因为H2O分子间存在氢键这种化学键 |
| B.晶体氩是由原子直接构成的,属于原子晶体 |
| C.KHCO3固体受热分解生成K2CO3、CO2和H2O,既破坏了离子键,也破坏了共价键 |
| D.HBr比HCl的热稳定性差,说明HBr的分子间作用力比HCl弱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】 和
和 均是化工中重要的化合物。已知
均是化工中重要的化合物。已知 的熔点是
的熔点是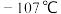 ,
, 的熔点是
的熔点是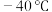 ,则下列说法正确的是
,则下列说法正确的是
 和
和 均是化工中重要的化合物。已知
均是化工中重要的化合物。已知 的熔点是
的熔点是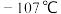 ,
, 的熔点是
的熔点是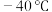 ,则下列说法正确的是
,则下列说法正确的是A. 和 和 均为非极性分子 均为非极性分子 |
B.液态 和 和 气化时克服的微粒间作用力相同 气化时克服的微粒间作用力相同 |
C. 和 和 中每个原子均满足8电子稳定结构 中每个原子均满足8电子稳定结构 |
D. 键能比 键能比 键能大,则 键能大,则 的熔点高于 的熔点高于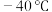 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】当SO3晶体熔化时,下述各项发生变化的是( )
| A.化学键 | B.硫与氧的原子个数之比 | C.分子构型 | D.分子间作用力 |
您最近一年使用:0次

 、
、 、
、 的核外电子排布相同,所以化学性质相同
的核外电子排布相同,所以化学性质相同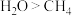 ,是因为水分子间存在氢键
,是因为水分子间存在氢键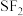 、
、 、
、 的分子中,原子周围都达到了8电子稳定结构
的分子中,原子周围都达到了8电子稳定结构

