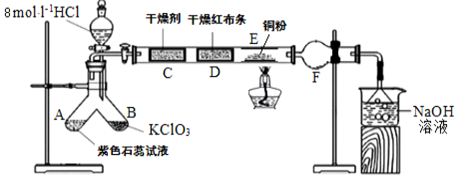
某小组利用氯酸钾与8mol/L盐酸反应制氯气并进行氯气性质的探究,实验装置如图所示:
请回答:
(1)装置F中填充的药品是___________
(2)E中实验现象是___________ ,氢氧化钠溶液中反应的离子方程式为___________
(3)根据相关实验现象就可以证明起漂白作用的不是氯气而是次氯酸,相关现象是___________ 。
(4)写出本实验中制取氯气的离子反应方程式___________ 。
(5)现要配制240ml 8mol/L所需盐酸,请回答下列问题:
①所用的仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要的仪器是___________
②配制过程中有下列实验操作步骤,其正确的顺序为___________ (填序号)

③下列操作会使配制结果偏高的是___________
A.容量瓶洗净后未干燥直接用来配制溶液
B.反复摇匀后发现液面低于刻度线,继续加水至刻度线
C.定容时俯视读数
D.用量筒量取浓盐酸配制所需盐酸时,量筒仰视读数

请回答:
(1)装置F中填充的药品是
(2)E中实验现象是
(3)根据相关实验现象就可以证明起漂白作用的不是氯气而是次氯酸,相关现象是
(4)写出本实验中制取氯气的离子反应方程式
(5)现要配制240ml 8mol/L所需盐酸,请回答下列问题:
①所用的仪器除量筒、烧杯、玻璃棒、胶头滴管外,还需要的仪器是
②配制过程中有下列实验操作步骤,其正确的顺序为

③下列操作会使配制结果偏高的是
A.容量瓶洗净后未干燥直接用来配制溶液
B.反复摇匀后发现液面低于刻度线,继续加水至刻度线
C.定容时俯视读数
D.用量筒量取浓盐酸配制所需盐酸时,量筒仰视读数
更新时间:2021-04-15 00:26:25
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】钠、氯及其化合物有如图转化关系,请按要求填空:

(1)一小块金属钠投入水中其反应的化学方程式是_________ 。
(2)将灼热的细铁丝放入盛有氯气的集气瓶中,观察到_________ 现象,其反应的化学方程式为_________ 。
(3)通常情况下,为了防止污染环境,在做完实验后,多余的氯气应用NaOH溶液吸收,其化学方程式为_________ 。
(4)工业上用氯气和石灰乳反应制漂白粉,其反应的化学方程式为_________ 。漂白粉的有效成分是_________ 。

(1)一小块金属钠投入水中其反应的化学方程式是
(2)将灼热的细铁丝放入盛有氯气的集气瓶中,观察到
(3)通常情况下,为了防止污染环境,在做完实验后,多余的氯气应用NaOH溶液吸收,其化学方程式为
(4)工业上用氯气和石灰乳反应制漂白粉,其反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
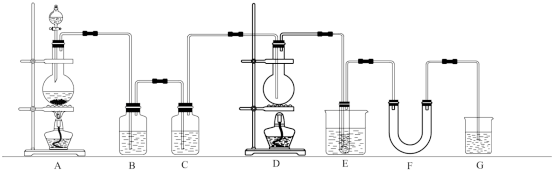
【推荐2】SnCl4是无色液体,沸点114.1℃,遇潮湿空气水解而生成SnO2和氯化氢。实验室利用下列装置可以制备无水SnCl4:
回答下列问题:
(1)本试验中检查制气装置A气密性的方法是_______ 。
(2)装置A中用浓盐酸的原因是①增强 的氧化性②增强
的氧化性②增强 的还原性,在发应后的固液混合物中加入
的还原性,在发应后的固液混合物中加入_______ 有氯气产生,证明①正确的,在发应后固液的混合物中加入_______ 有氯气产生,证明②正确的。
(3)实验过程中若发现B、C装置少量漏气,可采取的措施是_______ 。
(4)C的作用是_______ 。
(5)F中可装的试剂可以是_______ 。
a. b.
b. c.浓硫酸 d.
c.浓硫酸 d.
(6)制备反应停止熄灭酒精灯后,将G中导管移出溶液并使导管口靠近液面,装置冷却,之后的操作是_______ ,清洗仪器,摆放整齐,擦干净桌面。

回答下列问题:
(1)本试验中检查制气装置A气密性的方法是
(2)装置A中用浓盐酸的原因是①增强
 的氧化性②增强
的氧化性②增强 的还原性,在发应后的固液混合物中加入
的还原性,在发应后的固液混合物中加入(3)实验过程中若发现B、C装置少量漏气,可采取的措施是
(4)C的作用是
(5)F中可装的试剂可以是
a.
 b.
b. c.浓硫酸 d.
c.浓硫酸 d.
(6)制备反应停止熄灭酒精灯后,将G中导管移出溶液并使导管口靠近液面,装置冷却,之后的操作是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】无水氯化铁在空气中易潮解,加热易升华,冷却后易凝华。如图是两名同学设计的用氯气与铁反应制备无水氯化铁的实验装置。左边的反应装置相同,而右边有Ⅰ、Ⅱ两种产品收集装置。请回答下列问题:

(1)仪器A的名称是____________ 。
(2)装置B中发生反应的离子方程式为_____________________ ,其中浓盐酸表现出__________ 性。
(3)气体通过装置D的目的是_____________________ 。
(4)装置E中的反应开始前,需进行的操作是__________ ,应采取的方法是____________________ 。
(5)装置E中发生反应的化学方程式为_____________________ 。
(6)装置Ⅰ的主要缺点是_________________________ 。
(7)装置Ⅱ的G中发生反应的化学方程式为_________________________ 。如果选用装置Ⅱ来完成实验,则必须采取的改进措施是________________________________________________________________ 。

(1)仪器A的名称是
(2)装置B中发生反应的离子方程式为
(3)气体通过装置D的目的是
(4)装置E中的反应开始前,需进行的操作是
(5)装置E中发生反应的化学方程式为
(6)装置Ⅰ的主要缺点是
(7)装置Ⅱ的G中发生反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验室要配制450ml 0.2mol·L-1 Na2CO3溶液.请回答下列问题。
(1)托盘天平天平称取无水碳酸钠固体的质量为__________ g。
(2)需要使用的主要玻璃仪器有烧杯、玻璃棒、胶头滴管和_____________ 。
(3)试分析下列操作对所配溶液的浓度有何影响(填“偏高”,“偏低”或“无影响”)。
① 未洗涤烧杯和玻璃棒,使所配溶液浓度_________ ;
② 定容时俯视刻度线,使所配溶液浓度___________ ;
③ 摇匀后,发现液面低于刻度线,又滴加蒸馏水,使所配溶液浓度________ 。
(1)托盘天平天平称取无水碳酸钠固体的质量为
(2)需要使用的主要玻璃仪器有烧杯、玻璃棒、胶头滴管和
(3)试分析下列操作对所配溶液的浓度有何影响(填“偏高”,“偏低”或“无影响”)。
① 未洗涤烧杯和玻璃棒,使所配溶液浓度
② 定容时俯视刻度线,使所配溶液浓度
③ 摇匀后,发现液面低于刻度线,又滴加蒸馏水,使所配溶液浓度
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】二氧化氯消毒剂是国际公认的高效消毒灭菌剂。二氧化氯漂白液中常含有 ClO2和 Cl2两种主要成分。化学兴趣小组同学为测定某二氧化氯漂白液中 ClO2的浓度,进行如下实验:
【实验Ⅰ】配制250mL0.10mol/L的Na2S2O3溶液,步骤如下:
①用天平准确称取一定质量的 Na2S2O3·5H2O 固体,放入烧杯,用适量蒸馏水溶解;
②将烧杯中的溶液小心的注入 250mL 容量瓶中;
③用蒸馏水洗涤烧杯内壁和玻璃棒 2~3 次,并将每次洗涤的溶液转入容量瓶中,振荡;
④继续向容量瓶中加水至距刻度线 1~2cm 处,改用胶头滴管加水至刻度线;
⑤将容量瓶塞盖好,充分摇匀。
回答下列问题:
(1)容量瓶在使用前必须进行的操作是_______ ;
(2)配制溶液过程中需称量 Na2S2O3·5H2O 固体的质量为_______ ;
(3)配制溶液过程中,若未进行步骤③操作,则配制的溶液浓度_______ (填“偏高”、“偏低” 或“无影响”);
【实验Ⅱ】测定二氧化氯漂白液中ClO2浓度,步骤如下:
①量取 5mL 二氧化氯漂白液于锥形瓶中,加蒸馏水稀释到 25mL,再向其中加入过量 KI 溶液,二氧化氯漂白液中的两种成分分别发生反应: 2ClO2 + 2KI = 2KClO2 + I2、Cl2 + 2KI = 2KCl + I2
②加入淀粉作指示剂,向其中逐滴加入 0.10mol/L 的 Na2S2O3溶液至反应恰好完全进行,过程中发生的反应为: 2Na2S2O3 + I2 = Na2S4O6 + 2NaI
③加入稀硫酸调节溶液 pH=3,发生反应: KClO2 + 4KI + 2H2SO4 = KCl + 2K2SO4 + 2I2 +2H2O
④再逐滴加入 0.10mol/L 的 Na2S2O3溶液,反应恰好完全进行时,该步消耗 Na2S2O3溶液 20mL。
回答下列问题:
(4)用双线桥标出反应中电子转移的方向和数目:2ClO2 + 2KI = 2KClO2 + I2,______________ ;
(5)该二氧化氯漂白液中 ClO2的物质的量浓度为_______ 。
【实验Ⅰ】配制250mL0.10mol/L的Na2S2O3溶液,步骤如下:
①用天平准确称取一定质量的 Na2S2O3·5H2O 固体,放入烧杯,用适量蒸馏水溶解;
②将烧杯中的溶液小心的注入 250mL 容量瓶中;
③用蒸馏水洗涤烧杯内壁和玻璃棒 2~3 次,并将每次洗涤的溶液转入容量瓶中,振荡;
④继续向容量瓶中加水至距刻度线 1~2cm 处,改用胶头滴管加水至刻度线;
⑤将容量瓶塞盖好,充分摇匀。
回答下列问题:
(1)容量瓶在使用前必须进行的操作是
(2)配制溶液过程中需称量 Na2S2O3·5H2O 固体的质量为
(3)配制溶液过程中,若未进行步骤③操作,则配制的溶液浓度
【实验Ⅱ】测定二氧化氯漂白液中ClO2浓度,步骤如下:
①量取 5mL 二氧化氯漂白液于锥形瓶中,加蒸馏水稀释到 25mL,再向其中加入过量 KI 溶液,二氧化氯漂白液中的两种成分分别发生反应: 2ClO2 + 2KI = 2KClO2 + I2、Cl2 + 2KI = 2KCl + I2
②加入淀粉作指示剂,向其中逐滴加入 0.10mol/L 的 Na2S2O3溶液至反应恰好完全进行,过程中发生的反应为: 2Na2S2O3 + I2 = Na2S4O6 + 2NaI
③加入稀硫酸调节溶液 pH=3,发生反应: KClO2 + 4KI + 2H2SO4 = KCl + 2K2SO4 + 2I2 +2H2O
④再逐滴加入 0.10mol/L 的 Na2S2O3溶液,反应恰好完全进行时,该步消耗 Na2S2O3溶液 20mL。
回答下列问题:
(4)用双线桥标出反应中电子转移的方向和数目:2ClO2 + 2KI = 2KClO2 + I2,
(5)该二氧化氯漂白液中 ClO2的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】利用课堂上学到的知识来解决生活中的问题是我们学习的重要目的。
(1)某化学实验兴趣小组自行购置了鸡蛋、食醋等生活用品,进行了如下探究。
①甲同学测出从超市购买的食醋中醋酸(CH3COOH)含量为0.75mol/L,则食醋中醋酸含量为_______ g/100mL,属于_______ 醋(填“酿造”或“配制”,已知:酿造醋的国家标准为醋酸含量必须大于3.50g/100mL,而配制醋仅为1.50g~3.50g/100mL)。
②乙同学将鸡蛋壳(主要成分为CaCO3)泡进食醋中,发现有气泡产生,请写出该反应的离子方程式_______ ;
(2)下图是化学实验室浓盐酸试剂标签上的部分内容。
丁同学计划用该浓盐酸配制470mL1mol·L-1的稀盐酸,可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤玻璃棒 ⑥试剂瓶。请回答下列问题:
①经计算,配制1mol·L-1的稀盐酸需要量取上述浓盐酸的体积为_______ mL(结果保留1位小数)。
②配制稀盐酸时,还缺少的仪器有_______ 。
③测定所配制的稀盐酸,发现其浓度大于1mol·L-1,引起误差的原因可能是_______ 。
A.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入烧杯
B.定容时俯视容量瓶刻度线
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
(1)某化学实验兴趣小组自行购置了鸡蛋、食醋等生活用品,进行了如下探究。
①甲同学测出从超市购买的食醋中醋酸(CH3COOH)含量为0.75mol/L,则食醋中醋酸含量为
②乙同学将鸡蛋壳(主要成分为CaCO3)泡进食醋中,发现有气泡产生,请写出该反应的离子方程式
(2)下图是化学实验室浓盐酸试剂标签上的部分内容。
| 盐酸 分子式:HC1 相对分子质量:36.5 密度约1.18g.cm-3 HCl的质量分数:36.5% |
①经计算,配制1mol·L-1的稀盐酸需要量取上述浓盐酸的体积为
②配制稀盐酸时,还缺少的仪器有
③测定所配制的稀盐酸,发现其浓度大于1mol·L-1,引起误差的原因可能是
A.将量取的浓盐酸倒入烧杯后,洗涤量筒,洗涤液也注入烧杯
B.定容时俯视容量瓶刻度线
C.转移溶液后,未洗涤烧杯和玻璃棒
D.定容摇匀后发现液面低于容量瓶的刻度线,再加水至刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室用碳酸钠晶体(Na2CO3·10H2O)配制480mL0.2mol/LNa2CO3溶液,回答下列问题:
(1)所用的仪器除托盘天平、药匙、烧杯、玻璃棒外,还需要的玻璃仪器是:_______ 。
(2)配制过程中有下列实验操作步骤,其正确的顺序为:_______ 。

(3)下列操作,会使配制的溶液浓度偏小的是_______ (填写编号);
A.称量时碳酸钠晶体与砝码的位置颠倒
B.使用容量瓶配制溶液时,俯视液面定容后所得溶液的浓度
C.没有用蒸馏水洗烧杯2~3次,并将洗液移入容量瓶中
D.容量瓶刚用蒸馏水洗净,没有烘干
E.定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切
(4)用配制的Na2CO3溶液做以下实验,下列叙述不正确的是_______ (填写编号)
A.取2mL该Na2CO3溶液于试管中,滴加几滴酚酞,溶液变红
B.将一块沾有油污的铜片浸入加热过的该Na2CO3溶液中,静置约几分钟。再用镊子将铜片从溶液中取出后,用水冲洗干净,可观察到铜片表面变得洁净光亮
C.将该Na2CO3溶液分别滴入澄清石灰水、氯化钙溶液中,有相同的实验现象;其反应的离子方程式也相同
D.将该Na2CO3溶液逐滴加入稀硫酸中与稀硫酸逐滴加入Na2CO3溶液中,开始时有相同的实验现象,其反应的离子方程式也相同
(1)所用的仪器除托盘天平、药匙、烧杯、玻璃棒外,还需要的玻璃仪器是:
(2)配制过程中有下列实验操作步骤,其正确的顺序为:

(3)下列操作,会使配制的溶液浓度偏小的是
A.称量时碳酸钠晶体与砝码的位置颠倒
B.使用容量瓶配制溶液时,俯视液面定容后所得溶液的浓度
C.没有用蒸馏水洗烧杯2~3次,并将洗液移入容量瓶中
D.容量瓶刚用蒸馏水洗净,没有烘干
E.定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切
(4)用配制的Na2CO3溶液做以下实验,下列叙述不正确的是
A.取2mL该Na2CO3溶液于试管中,滴加几滴酚酞,溶液变红
B.将一块沾有油污的铜片浸入加热过的该Na2CO3溶液中,静置约几分钟。再用镊子将铜片从溶液中取出后,用水冲洗干净,可观察到铜片表面变得洁净光亮
C.将该Na2CO3溶液分别滴入澄清石灰水、氯化钙溶液中,有相同的实验现象;其反应的离子方程式也相同
D.将该Na2CO3溶液逐滴加入稀硫酸中与稀硫酸逐滴加入Na2CO3溶液中,开始时有相同的实验现象,其反应的离子方程式也相同
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】在KNO3固体样品中含有少量的KCl、BaCl2杂质,为了提纯KNO3并分离得到BaCl2,进行如下实验操作:

(1)加入过量K2CO3所发生反应的离子方程式为____ ;
(2)结合图中各物质的溶解度曲线可知操作③的名称是____ ;

(3)有人认为操作③之前无需加入过量的酸b,也能达到实验目的,你认为该观点是否正确?并做出解释___ 。
(4)用制得的KNO3固体配制200mL0.2mol/LKNO3溶液。
①本实验用到的仪器有天平、药匙、玻璃棒、烧杯、量筒、还有___ 、___ ;
②下列情况会使所配制的KNO3 溶液的浓度偏高的是____ (填字母)。
A.没有洗涤烧杯和玻璃棒
B.容量瓶不干燥,含有少量蒸馏水
C.定容时仰视刻度线
D.定容时俯视刻度线
E.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线

(1)加入过量K2CO3所发生反应的离子方程式为
(2)结合图中各物质的溶解度曲线可知操作③的名称是

(3)有人认为操作③之前无需加入过量的酸b,也能达到实验目的,你认为该观点是否正确?并做出解释
(4)用制得的KNO3固体配制200mL0.2mol/LKNO3溶液。
①本实验用到的仪器有天平、药匙、玻璃棒、烧杯、量筒、还有
②下列情况会使所配制的KNO3 溶液的浓度偏高的是
A.没有洗涤烧杯和玻璃棒
B.容量瓶不干燥,含有少量蒸馏水
C.定容时仰视刻度线
D.定容时俯视刻度线
E.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ.如图是一种“纳米药物分子运输车”,该技术可提高肿瘤的治疗效果。回答下列问题:
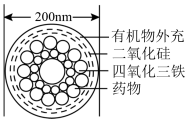
(1)“纳米药物分子运输车”分散于水中所得的分散系_______ (填“属于”或“不属于”)胶体。
(2)“纳米药物分子运输车”的外壳属于有机物。酒精、蔗糖、醋酸这三种有机物中,属于电解质的是_______ 。
(3)从元素组成的角度分析,CO2和Fe3O4可归为同一类物质,其类别属于化合物中的_______ 。
(4)纳米级的Fe3O4是一种非常重要的磁性材料。
①Fe3O4溶于稀盐酸生成FeCl3、_______ 和H2O。
②铁在氧气中燃烧生成Fe3O4,反应中每生成1 mol Fe3O4转移_______ mol电子。
Ⅱ.配制480 mL0.5 mol/L的NaOH溶液用于洗涤器物。
(5)配制时,应用天平称取NaOH的质量为_______ 。
某操作步骤如图所示:

该操作应放在如图所示的_______ (填序号)操作之间。

(6)下列说法错误的是_______(填字母)。

(1)“纳米药物分子运输车”分散于水中所得的分散系
(2)“纳米药物分子运输车”的外壳属于有机物。酒精、蔗糖、醋酸这三种有机物中,属于电解质的是
(3)从元素组成的角度分析,CO2和Fe3O4可归为同一类物质,其类别属于化合物中的
(4)纳米级的Fe3O4是一种非常重要的磁性材料。
①Fe3O4溶于稀盐酸生成FeCl3、
②铁在氧气中燃烧生成Fe3O4,反应中每生成1 mol Fe3O4转移
Ⅱ.配制480 mL0.5 mol/L的NaOH溶液用于洗涤器物。
(5)配制时,应用天平称取NaOH的质量为
某操作步骤如图所示:

该操作应放在如图所示的

(6)下列说法错误的是_______(填字母)。
| A.称量NaOH固体的时间不宜过长 |
| B.待烧杯中溶液冷却至室温才进行转移 |
| C.定容时,仰视容量瓶刻度线会使配制的NaOH溶液浓度偏高 |
| D.容量瓶可存放配好的NaOH溶液 |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室用浓硫酸和乙醇反应制备乙稀,若温度过高或加热时间过长,制得的乙稀往往混有CO2、SO2、H2O(气体少量)。请回答下列问题:
(1)试分析CO2和SO2是怎么样产生的?_____ (用一句话说明)。
(2)试用下图所示的装置设计一个实验,验证制得的气体中确实含有CO2和SO2、H2O(g) ,按气流的方向,各装置的连接顺序是:__________ 。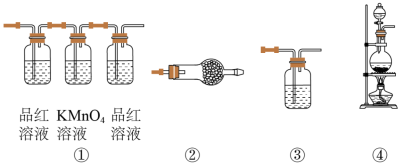
(3)实验时若观察到:①中A瓶中溶液褪色,B瓶中深水颜色逐渐变浅,C瓶中溶液不褪色,则A瓶的作用是___________ ,B瓶的作用是________ , C瓶的作用是____________ 。
(4)装置②中所加的试剂名称是__________ ,它可以验证的气体是__________ ,简述确定装置②在整套装置中的位置的理由是______________ 。
(5)装置③中所盛溶液的名称是__________ ,它可以用来验证的气体是__________ 。
(1)试分析CO2和SO2是怎么样产生的?
(2)试用下图所示的装置设计一个实验,验证制得的气体中确实含有CO2和SO2、H2O(g) ,按气流的方向,各装置的连接顺序是:

(3)实验时若观察到:①中A瓶中溶液褪色,B瓶中深水颜色逐渐变浅,C瓶中溶液不褪色,则A瓶的作用是
(4)装置②中所加的试剂名称是
(5)装置③中所盛溶液的名称是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】草酸钴可用于指示剂和催化剂的制备。用水钴矿(主要成分为Co2O3,含少量Fe2O3、A12O3、MnO、MgO、CaO、SiO2等)制取CoC2O4·2H2O工艺流程如下

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
(1)CoC2O4·2H2O中C的化合价是____________________________ 。
(2)写出浸出过程中Na2SO3与Co2O3发生反应的离子方程式:______________ 。
(3)浸出液中加入NaClO3的目的是____________________________ 。
(4)加Na2CO3能使浸出液中某些金属离子转化成氢氧化物沉淀,沉淀除Al(OH)3外,还有的成分是______________ (填化学式),试用离子方程式和必要的文字简述其原理:____________________________ 。
(5)萃取剂对金属离子的萃取率与pH的关系如图,萃取剂的作用是______________ ;其使用的适宜pH范围是______________ 。

A. 2.0〜2.5
B. 3.0〜3.5
C. 4.0〜4.5
(6)滤液I“除钙、镁”是将其转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10,当加入过量NaF后,所得滤液c(Mg2+)/c(Ca2+) =______________ 。
(7)用m1kg水钴矿(含Co2O360%)制备CoC2O4·2H2O,最终得到产品m2kg,产率(实际产量/理论产量×100%)为____________________________ 。(已知:M(Co2O3)=166,M(CoC2O4·2H2O)=183,仅需列出数字计算式)。

已知:①浸出液含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Ca2+、Mg2+、Al3+等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:
| 沉淀物 | Fe(OH)3 | Al(OH)3 | Co(OH)2 | Fe(OH)2 | Mn(OH)2 |
| 完全沉淀的pH | 3.7 | 5.2 | 9.2 | 9.6 | 9.8 |
(1)CoC2O4·2H2O中C的化合价是
(2)写出浸出过程中Na2SO3与Co2O3发生反应的离子方程式:
(3)浸出液中加入NaClO3的目的是
(4)加Na2CO3能使浸出液中某些金属离子转化成氢氧化物沉淀,沉淀除Al(OH)3外,还有的成分是
(5)萃取剂对金属离子的萃取率与pH的关系如图,萃取剂的作用是

A. 2.0〜2.5
B. 3.0〜3.5
C. 4.0〜4.5
(6)滤液I“除钙、镁”是将其转化为MgF2、CaF2沉淀。已知Ksp(MgF2)=7.35×10-11、Ksp(CaF2)=1.05×10-10,当加入过量NaF后,所得滤液c(Mg2+)/c(Ca2+) =
(7)用m1kg水钴矿(含Co2O360%)制备CoC2O4·2H2O,最终得到产品m2kg,产率(实际产量/理论产量×100%)为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】如图是在实验室进行二氧化硫制备与性质实验的组合装置,部分固定装置未画出。
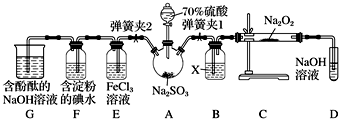
(1)在组装好装置后,若要检验A~D装置的气密性,其操作是首先__________ ,然后往D中装入水,然后微热A,观察到D中有气泡冒出,移开酒精灯或松开双手,D中导管有水柱形成且高度保持不变,说明装置气密性良好。
(2)装置D中盛放NaOH溶液的作用是___________ 。
(3)关闭弹簧夹1后,打开弹簧夹2,残余气体进入E、F、G中,能说明I-还原性弱于SO2的现象为_____ ;发生反应的离子方程式是________________ 。
(4)为了验证E中SO2与FeCl3发生了氧化还原反应,设计了如下实验:取E中的溶液,往溶液中加入用稀硝酸酸化的BaCl2溶液,产生白色沉淀,说明SO2与FeCl3发生了氧化还原反应。
上述方案是否合理?________ (填“合理”或“不合理”),原因是_____________ 。
(5)实验过程中G中含酚酞的NaOH溶液逐渐褪色,此实验证明SO2具有漂白性还是其溶于水显酸性?请设计实验验证:______________________ 。

(1)在组装好装置后,若要检验A~D装置的气密性,其操作是首先
(2)装置D中盛放NaOH溶液的作用是
(3)关闭弹簧夹1后,打开弹簧夹2,残余气体进入E、F、G中,能说明I-还原性弱于SO2的现象为
(4)为了验证E中SO2与FeCl3发生了氧化还原反应,设计了如下实验:取E中的溶液,往溶液中加入用稀硝酸酸化的BaCl2溶液,产生白色沉淀,说明SO2与FeCl3发生了氧化还原反应。
上述方案是否合理?
(5)实验过程中G中含酚酞的NaOH溶液逐渐褪色,此实验证明SO2具有漂白性还是其溶于水显酸性?请设计实验验证:
您最近一年使用:0次



