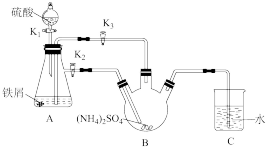
莫尔盐[(NH4)2Fe(SO4)2·6H2O,Mr=392]是一种重要的还原剂,在空气中比一般的亚铁盐稳定。某学习小组设计如下实验制备少量的莫尔盐。
回答下列问题:
Ⅰ.制取莫尔盐
(1)连接装置,检查装置气密性。将0.1mol(NH4)2SO4晶体置于玻璃仪器___________ (填仪器名称)中,将6.0g洁净铁屑加入锥形瓶中。
(2)①打开分液漏斗瓶塞,关闭活塞K3,打开K2、K1,加完55.0mL2mol·L-1稀硫酸后关闭K1,A装置中反应的离子方程式为___________ 。
②待大部分铁粉溶解后,打开K3、关闭K2,此时可以看到的现象为___________ ,原因是___________ 。
③关闭活塞K2、K3,采用100℃水浴蒸发B中水分,液面产生晶膜时,停止加热,冷却结晶、___________ 、用无水乙醇洗涤晶体。装置A中的反应,硫酸需过量,保持溶液的pH在1~2之间,其目的为___________ 。
④装置C的作用为___________ ,装置C存在的缺点是___________ 。

回答下列问题:
Ⅰ.制取莫尔盐
(1)连接装置,检查装置气密性。将0.1mol(NH4)2SO4晶体置于玻璃仪器
(2)①打开分液漏斗瓶塞,关闭活塞K3,打开K2、K1,加完55.0mL2mol·L-1稀硫酸后关闭K1,A装置中反应的离子方程式为
②待大部分铁粉溶解后,打开K3、关闭K2,此时可以看到的现象为
③关闭活塞K2、K3,采用100℃水浴蒸发B中水分,液面产生晶膜时,停止加热,冷却结晶、
④装置C的作用为
2021·西藏拉萨·一模 查看更多[2]
更新时间:2021-04-27 14:58:29
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】某混合溶液中,可能大量含阳离子: 、
、 、
、 、
、 、
、 ;阴离子:
;阴离子: 、
、 、
、 。为探究其成分,某同学将
。为探究其成分,某同学将 逐渐加入到上述混合溶液中并微热,产生沉淀和气体的物质的量与加入
逐渐加入到上述混合溶液中并微热,产生沉淀和气体的物质的量与加入 的物质的量的关系分别如图所示:
的物质的量的关系分别如图所示:
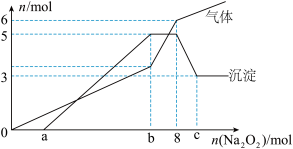
(1)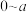 段无沉淀生成,说明一定含有
段无沉淀生成,说明一定含有___________ ,一定不含有___________ ;通过图像推理溶液中一定还存在___________ (以上均填离子符号);
(2)加入过氧化钠物质的量为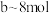 时生成的气体为
时生成的气体为___________ ;
(3)写出沉淀减少的化学方程式:___________ 、___________ ;
(4)溶液中一定存在的阳离子物质的量之比为___________ (注意离子符号与比值相对应)。
 、
、 、
、 、
、 、
、 ;阴离子:
;阴离子: 、
、 、
、 。为探究其成分,某同学将
。为探究其成分,某同学将 逐渐加入到上述混合溶液中并微热,产生沉淀和气体的物质的量与加入
逐渐加入到上述混合溶液中并微热,产生沉淀和气体的物质的量与加入 的物质的量的关系分别如图所示:
的物质的量的关系分别如图所示:
(1)
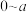 段无沉淀生成,说明一定含有
段无沉淀生成,说明一定含有(2)加入过氧化钠物质的量为
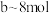 时生成的气体为
时生成的气体为(3)写出沉淀减少的化学方程式:
(4)溶液中一定存在的阳离子物质的量之比为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A+、B+、C-、D、E5种微粒(分子或离子),它们分别含10个电子,已知它们有如下转化关系:①A++C-=D+E;②B++C-=2D。据此,回答下列问题:
(1)上述含10电子的四核阳离子为___________ ,含10电子的阴离子为_______ 。
(2)A+和B+的电子式A+____________ 、B+____________ 。
(3)C-、D、E3种粒子结合质子H+的能力由强到弱的顺序是(用粒子的化学式表示)____________________ ;这一顺序可用以下离子方程式加以说明:
①_____________________________________________ ;
②_____________________________________________ 。
(1)上述含10电子的四核阳离子为
(2)A+和B+的电子式A+
(3)C-、D、E3种粒子结合质子H+的能力由强到弱的顺序是(用粒子的化学式表示)
①
②
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】摩尔盐的成分为(NH4)2Fe(SO4)2·6H2O(M=392g·mol-1),常作氧化还原滴定剂。学校购买了一批摩尔盐样品(假设杂质不参与反应),某学习小组拟设计实验方案测定其纯度:
方案1:沉淀法。甲同学准确称量一定质量样品溶于适量的蒸馏水,滴加适量BaCl2溶液至S042-完全沉淀,经过滤、洗涤、干燥,称得BaSO4质量。
(1)检验SO42-是否完全沉淀的操作是____________________________________________ 。
方案2:滴定法。乙同学准确称取mg摩尔盐样品溶于蒸馏水配制成250mL溶液,量取25.00mL所配制溶液于锥形瓶中,滴加适量的稀硫酸,用cmol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液的体积为VmL。
(2)用KMnO4溶液滴定时应选用___ (填“酸式”或“碱式”)滴定管,写出滴定反应的离子方程式:_________ 。
(3)该样品的纯度为_________________________________ 。
(4)若用待测液润洗锥形瓶,测得结果___________ (填“偏高”“偏低”或“无影响”)。
方案3:量气法。丙同学准确称量4.0g样品按下图所示装置进行实验。
(5)①橡胶管L的作用是______________________ 。
②B中液体可以是___________ (填字母)。
a.饱和食盐水 b四氯化碳 c.煤油 d饱和氯化铵溶液
③当A中样品完全反应后,待装置冷却至室温,测得NH3的体积为448mL(已折合成标准状况)。根据上述数据计算,该产品的纯度为____________ 。
方案1:沉淀法。甲同学准确称量一定质量样品溶于适量的蒸馏水,滴加适量BaCl2溶液至S042-完全沉淀,经过滤、洗涤、干燥,称得BaSO4质量。
(1)检验SO42-是否完全沉淀的操作是
方案2:滴定法。乙同学准确称取mg摩尔盐样品溶于蒸馏水配制成250mL溶液,量取25.00mL所配制溶液于锥形瓶中,滴加适量的稀硫酸,用cmol·L-1KMnO4溶液滴定至终点,消耗KMnO4溶液的体积为VmL。
(2)用KMnO4溶液滴定时应选用
(3)该样品的纯度为
(4)若用待测液润洗锥形瓶,测得结果
方案3:量气法。丙同学准确称量4.0g样品按下图所示装置进行实验。
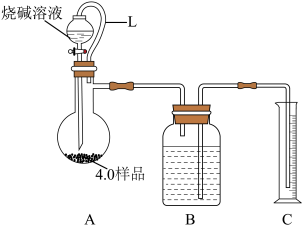
(5)①橡胶管L的作用是
②B中液体可以是
a.饱和食盐水 b四氯化碳 c.煤油 d饱和氯化铵溶液
③当A中样品完全反应后,待装置冷却至室温,测得NH3的体积为448mL(已折合成标准状况)。根据上述数据计算,该产品的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某学习小组欲利用如下装置制备SO2,并检验SO2的性质和制取食品抗氧化剂焦亚硫酸钠(Na2S2O5)。
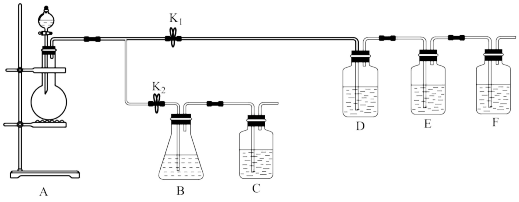
(1)检查A装置气密性的方法是___________ 。
(2)用A装置制备SO2,最适宜的试剂为___________ (填序号)。
a.10%硫酸、Na2SO3固体 b.98%浓硫酸、铜片
c.70%浓硫酸、Na2SO3固体 d.60%浓硝酸、Na2SO3固体
(3)加好药品,打开K1、关闭K2。已知:E装置中盛放FeCl3和BaCl2的混合溶液。
①若D装置的作用是检验SO2的漂白性,则D装置中通常盛放的试剂是___________ 。
②用离子方程式表示E装置中发生的反应:___________ 。
③C装置的作用是___________ 。F装置中可选用的试剂是___________ (填序号)。
a.浓硫酸 b.氢氧化钠溶液 c.酸性高锰酸钾溶液
(4)B装置中盛放的是Na2SO3饱和溶液。打开K2、关闭K1一段时间后B装置中有Na2S2O5晶体析出,B装置中发生反应的化学方程式为___________ 。

(1)检查A装置气密性的方法是
(2)用A装置制备SO2,最适宜的试剂为
a.10%硫酸、Na2SO3固体 b.98%浓硫酸、铜片
c.70%浓硫酸、Na2SO3固体 d.60%浓硝酸、Na2SO3固体
(3)加好药品,打开K1、关闭K2。已知:E装置中盛放FeCl3和BaCl2的混合溶液。
①若D装置的作用是检验SO2的漂白性,则D装置中通常盛放的试剂是
②用离子方程式表示E装置中发生的反应:
③C装置的作用是
a.浓硫酸 b.氢氧化钠溶液 c.酸性高锰酸钾溶液
(4)B装置中盛放的是Na2SO3饱和溶液。打开K2、关闭K1一段时间后B装置中有Na2S2O5晶体析出,B装置中发生反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】在生活中亚硝酸钠( )应用十分广泛,它是一种白色固体,外观与NaCl极其相似。少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长;还可用于治疗氰化物中毒等。
)应用十分广泛,它是一种白色固体,外观与NaCl极其相似。少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长;还可用于治疗氰化物中毒等。
(1)人体正常的血红蛋白含有 ,若误食亚硝酸钠会把
,若误食亚硝酸钠会把 转换为
转换为 而中毒,应立即注射美蓝溶液进行治疗。上述过程中,亚硝酸钠作
而中毒,应立即注射美蓝溶液进行治疗。上述过程中,亚硝酸钠作_______ (填“氧化”或“还原”下同)剂,美蓝溶液被_______ 。
(2)某腌制品中亚硝酸钠含量随时间变化如图所示,若要保证在亚硝酸钠含量低于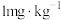 时食用,则三种条件下保存时间最长的是
时食用,则三种条件下保存时间最长的是_______ (填序号)。
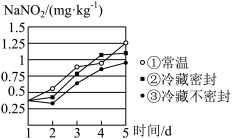
(3)某化学兴趣小组查阅资料得知 ,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)
,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)
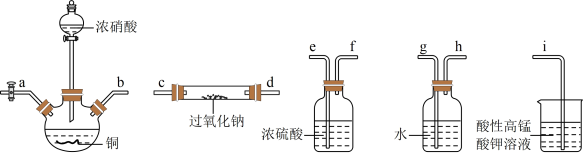
已知: 易被空气氧化,NO能被酸性高锰酸钾溶液氧化为
易被空气氧化,NO能被酸性高锰酸钾溶液氧化为 ,但不能被浓硫酸氧化;酸性高锰酸钾溶液可将
,但不能被浓硫酸氧化;酸性高锰酸钾溶液可将 氧化成
氧化成
①盛装浓硝酸的仪器名称为_______ ,仪器按气流方向连接顺序为b→g_______ (装置可重复使用)。
②反应开始前打开止水夹a,通入过量氮气的目的是排除装置中的空气,若不排除装置中的空气,可能产生的后果是_______ ;反应结束后打开止水夹a,通入过量氮气的目的是_______ 。
③盛水的洗气瓶的作用是_______ 。
④判断 已被NO反应完全的现象是
已被NO反应完全的现象是_______ 。
(4)某工厂以硝酸为原料生产亚硝酸钠,其工艺流程如下:
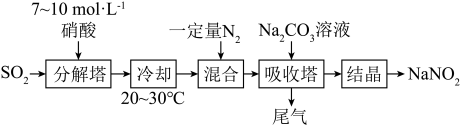
已知: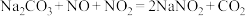 。按一定计量比在“分解塔”中通
。按一定计量比在“分解塔”中通 和喷入硝酸,若反应后生成的NO与
和喷入硝酸,若反应后生成的NO与 的物质的量之比恰好为1:1,则“分解塔”中发生反应的化学方程式:
的物质的量之比恰好为1:1,则“分解塔”中发生反应的化学方程式:_______ 。
 )应用十分广泛,它是一种白色固体,外观与NaCl极其相似。少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长;还可用于治疗氰化物中毒等。
)应用十分广泛,它是一种白色固体,外观与NaCl极其相似。少量可做食品的护色剂,可防止肉毒杆菌在肉类食品中生长;还可用于治疗氰化物中毒等。(1)人体正常的血红蛋白含有
 ,若误食亚硝酸钠会把
,若误食亚硝酸钠会把 转换为
转换为 而中毒,应立即注射美蓝溶液进行治疗。上述过程中,亚硝酸钠作
而中毒,应立即注射美蓝溶液进行治疗。上述过程中,亚硝酸钠作(2)某腌制品中亚硝酸钠含量随时间变化如图所示,若要保证在亚硝酸钠含量低于
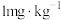 时食用,则三种条件下保存时间最长的是
时食用,则三种条件下保存时间最长的是
(3)某化学兴趣小组查阅资料得知
 ,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)
,该学习小组利用下列装置制备干燥的亚硝酸钠(夹持及加热装置略去,部分仪器可重复使用)
已知:
 易被空气氧化,NO能被酸性高锰酸钾溶液氧化为
易被空气氧化,NO能被酸性高锰酸钾溶液氧化为 ,但不能被浓硫酸氧化;酸性高锰酸钾溶液可将
,但不能被浓硫酸氧化;酸性高锰酸钾溶液可将 氧化成
氧化成
①盛装浓硝酸的仪器名称为
②反应开始前打开止水夹a,通入过量氮气的目的是排除装置中的空气,若不排除装置中的空气,可能产生的后果是
③盛水的洗气瓶的作用是
④判断
 已被NO反应完全的现象是
已被NO反应完全的现象是(4)某工厂以硝酸为原料生产亚硝酸钠,其工艺流程如下:

已知:
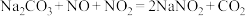 。按一定计量比在“分解塔”中通
。按一定计量比在“分解塔”中通 和喷入硝酸,若反应后生成的NO与
和喷入硝酸,若反应后生成的NO与 的物质的量之比恰好为1:1,则“分解塔”中发生反应的化学方程式:
的物质的量之比恰好为1:1,则“分解塔”中发生反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】某课外研究性学习小组用下图所示装置制备少量溴苯并验证溴与苯的反应是取代反应。
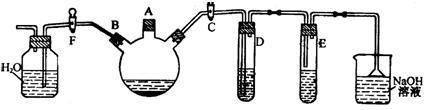
实验时,关闭F活塞,打开C活塞,在装有少量苯的三口烧瓶中由A口加入少量液溴,再加入少量铁屑,塞住A口。
回答下列问题:
(1)D试管内装的是______________ ,其作用是_____________________ 。
(2)E试管内装的是______________ 。
(3)除去溴苯中混有的Br2杂质的试剂是____________ ,操作方法为____________ 。
(4)三口烧瓶中发生反应的化学方程式为:_________________________________
(5)根据什么现象可证明验证溴与苯的反应是取代反应?__________________ 。

实验时,关闭F活塞,打开C活塞,在装有少量苯的三口烧瓶中由A口加入少量液溴,再加入少量铁屑,塞住A口。
回答下列问题:
(1)D试管内装的是
(2)E试管内装的是
(3)除去溴苯中混有的Br2杂质的试剂是
(4)三口烧瓶中发生反应的化学方程式为:
(5)根据什么现象可证明验证溴与苯的反应是取代反应?
您最近一年使用:0次



