将足量的AgCl分别放入下列物质中,AgCl的溶解度由大到小排列的顺序是
①20 mL 0.01 mol·L-1NH4Cl溶液
②30 mL 0.02 mol·L-1 CaCl2溶液
③40 mL 0.03 mol·L-1盐酸
④10 mL蒸馏水
⑤50 mL 0.05 mol·L-1AgNO3溶液
①20 mL 0.01 mol·L-1NH4Cl溶液
②30 mL 0.02 mol·L-1 CaCl2溶液
③40 mL 0.03 mol·L-1盐酸
④10 mL蒸馏水
⑤50 mL 0.05 mol·L-1AgNO3溶液
| A.①②③④⑤ | B.④①③②⑤ | C.⑤④②①③ | D.④③⑤②① |
18-19高二下·福建莆田·期中 查看更多[3]
(已下线)3.4.1 沉淀溶解平衡-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)3.4.1 沉淀溶解平衡原理-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)福建省莆田第十五中学2018-2019学年高二下学期期中测试化学试题
更新时间:2021-04-23 09:56:49
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】下列叙述中,不正确的是
| A.AgCl在水溶液中的沉淀溶解平衡方程式是AgCl(s)⇌Ag+(aq)+Cl-(aq) |
| B.HCl在水溶液中的电离方程式是HCl=H++Cl- |
| C.反应aA(g)⇌bB(g)+cC(g)达到平衡以后,增大A的物质的量浓度,A的转化率一定减小 |
| D.钢铁发生电化学腐蚀时负极反应式为Fe-2e-=Fe2+ |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】对“AgCl(s)  Ag+(aq)+Cl-(aq)”的理解正确的是
Ag+(aq)+Cl-(aq)”的理解正确的是
①说明AgCl没有完全电离,AgCl是弱电解质
②说明溶解的AgCl已完全电离,是强电解质
③说明Cl-与Ag+的反应不能完全进行到底
④说明Cl-与Ag+的反应可以完全进行到底
 Ag+(aq)+Cl-(aq)”的理解正确的是
Ag+(aq)+Cl-(aq)”的理解正确的是①说明AgCl没有完全电离,AgCl是弱电解质
②说明溶解的AgCl已完全电离,是强电解质
③说明Cl-与Ag+的反应不能完全进行到底
④说明Cl-与Ag+的反应可以完全进行到底
| A.③④ | B.②③ | C.①③ | D.②④ |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】把Ca(OH)2溶入蒸馏水中,一定时间后达到以下平衡:Ca(OH)2(s) Ca2+ +2OH–,加入以下物质,可使Ca(OH)2(s)减少的是
Ca2+ +2OH–,加入以下物质,可使Ca(OH)2(s)减少的是
 Ca2+ +2OH–,加入以下物质,可使Ca(OH)2(s)减少的是
Ca2+ +2OH–,加入以下物质,可使Ca(OH)2(s)减少的是| A.CaO | B.AlCl3 | C.NaOH | D.CaCl2 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】在NaCl饱和溶液中通入HCl(g)时,NaCl(s)能沉淀析出的原因是
| A.HCl水溶液是强酸,任何强酸都导致有沉淀析出 |
| B.Cl-浓度增大,使平衡向生成氯化钠的方向移动,生成NaCl(s) |
| C.酸的存在降低了Ksp(NaCl)的数值 |
| D.Ksp(NaCl)不受酸的影响,但增加Cl-浓度,能使Ksp(NaCl)减小 |
您最近一年使用:0次

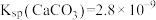 ,现将
,现将 溶液与
溶液与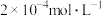 的
的 溶液等体积混合,若要产生沉淀,则原
溶液等体积混合,若要产生沉淀,则原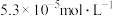
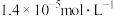
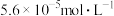
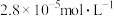
 Mg2+(aq)+2OH-(aq),为使Mg(OH)2固体的量减少,可加入少量的
Mg2+(aq)+2OH-(aq),为使Mg(OH)2固体的量减少,可加入少量的

