(1)COCl2分子中所有原子均满足8电子构型,COCl2分子中σ键和π键的个数比为_______ ,中心原子的杂化方式为_______ 。
(2)AlH 中,Al原子的轨道杂化方式为
中,Al原子的轨道杂化方式为_______ ;列举与AlH 空间构型相同的一种粒子:
空间构型相同的一种粒子:_______ 。
(3)用价层电子对互斥理论推断SnBr2分子中,Sn原子的轨道杂化方式为_______ ,SnBr2分子中Br-Sn-Br的键角_______ 120°(填“>”“<”或“=”)。
(2)AlH
 中,Al原子的轨道杂化方式为
中,Al原子的轨道杂化方式为 空间构型相同的一种粒子:
空间构型相同的一种粒子:(3)用价层电子对互斥理论推断SnBr2分子中,Sn原子的轨道杂化方式为
20-21高二下·黑龙江牡丹江·阶段练习 查看更多[2]
(已下线)第2.2.2讲 杂化轨道理论-2021-2022学年高二化学链接教材精准变式练(人教版2019选择性必修2)黑龙江省牡丹江市海林市朝鲜族中学2020-2021学年高二下学期4月份月考化学试题
更新时间:2021-05-08 12:57:19
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】在 分子中,键角∠HCO
分子中,键角∠HCO___________ (填“>”“<”或“=”)∠HCH,理由是___________ 。
 分子中,键角∠HCO
分子中,键角∠HCO
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】O3分子的立体构型为________ 。根据表中数据判断氧原子之间的共价键最稳定的粒子是______ 。
| 粒子 | O2 | O | O3 |
| 键长/pm | 121 | 126 | 128 |
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】氮及其化合物与人类生产、生活息息相关。
(1)在现代化学中,常利用________ 上的特征谱线来鉴定元素,称为光谱分析。
(2)基态N原子的价电子占据的能量最高的能级是________ ,价电子在该能级上的排布遵循的原则是________ 。
(3)化肥(NH4)2SO4中会含有N4H4(SO4)2,该物质在水中电离出SO42-和N4H44-,N4H44-遇到碱性溶液会生成一种形似白磷(P4)的N4分子。 N、O、S中第一电离能由大到小排序为________ ,N4比P4的沸点________ ,原因为________ 。
(4)在稀氨水中,丁二酮肟(CH3C=N-OH)2与Ni2+反应可生成鲜红色沉淀丁二酮肟镍(结构如右图),常用于检验Ni2+。
①在丁二酮肟镍中,存在的作用力有________
A.配位键 B.离子键 C. σ键 D. π键 E.金属键 F.氢键
②在丁二酮肟镍中,碳原子的杂化轨道类型有________ 。
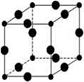
(5)Cu3N具有良好的电学和光学性能,其晶胞结构如右图,Cu+半径为a pm,N3-半径为b pm,则N3-的配位数为________ ,Cu3N 的密度为________ g·cm-3。
(1)在现代化学中,常利用
(2)基态N原子的价电子占据的能量最高的能级是
(3)化肥(NH4)2SO4中会含有N4H4(SO4)2,该物质在水中电离出SO42-和N4H44-,N4H44-遇到碱性溶液会生成一种形似白磷(P4)的N4分子。 N、O、S中第一电离能由大到小排序为
(4)在稀氨水中,丁二酮肟(CH3C=N-OH)2与Ni2+反应可生成鲜红色沉淀丁二酮肟镍(结构如右图),常用于检验Ni2+。
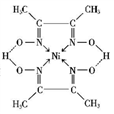
①在丁二酮肟镍中,存在的作用力有
A.配位键 B.离子键 C. σ键 D. π键 E.金属键 F.氢键
②在丁二酮肟镍中,碳原子的杂化轨道类型有
(5)Cu3N具有良好的电学和光学性能,其晶胞结构如右图,Cu+半径为a pm,N3-半径为b pm,则N3-的配位数为
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】20世纪50年代科学家提出价层电子对互斥模型(简称VSEPR模型),用于预测简单分子的空间结构。其要点可以概括为:
Ⅰ、用AXnEm表示只含一个中心原子的分子组成,A为中心原子,X为与中心原子相结合的原子,E为中心原子价层未参与成键的电子对(称为孤电子对), 称为价层电子对数。分子中的价层电子对总是互相排斥,均匀地分布在中心原子周围的空间。
称为价层电子对数。分子中的价层电子对总是互相排斥,均匀地分布在中心原子周围的空间。
Ⅱ、分子的空间结构是指分子中的原子在空间的排布,不包括中心原子未成键的孤电子对。
Ⅲ、分子中价层电子对之间的斥力的主要顺序为:
i、孤电子对之间的斥力>孤电子对与共用电子对之间的斥力>共用电子对之间的斥力;
ii、双键与双键之间的斥力>双键与单键之间的斥力>单键与单键之间的斥力;
iii、X原子得电子能力越弱,A—X形成的共用电子对之间的斥力越强;
iv、其他。
请仔细阅读上述材料,回答下列问题:
(1)由 的
的 模型填写下表:
模型填写下表:
(2)请用 模型解释
模型解释 为直线形分子的原因:
为直线形分子的原因:___________ 。
(3) 分子的空间结构为
分子的空间结构为___________ ,请你预测水分子中 的大小范围并解释原因:
的大小范围并解释原因:___________ 。
(4) 和
和 都属于
都属于 型分子,S、O之间以双键结合,S与
型分子,S、O之间以双键结合,S与 、S与F之间以单键结合。请你预测
、S与F之间以单键结合。请你预测 和
和 分子的空间结构:
分子的空间结构:___________ 。 分子中
分子中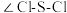
___________ (填“<”“>”或“=”) 分子中
分子中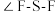 。
。
Ⅰ、用AXnEm表示只含一个中心原子的分子组成,A为中心原子,X为与中心原子相结合的原子,E为中心原子价层未参与成键的电子对(称为孤电子对),
 称为价层电子对数。分子中的价层电子对总是互相排斥,均匀地分布在中心原子周围的空间。
称为价层电子对数。分子中的价层电子对总是互相排斥,均匀地分布在中心原子周围的空间。Ⅱ、分子的空间结构是指分子中的原子在空间的排布,不包括中心原子未成键的孤电子对。
Ⅲ、分子中价层电子对之间的斥力的主要顺序为:
i、孤电子对之间的斥力>孤电子对与共用电子对之间的斥力>共用电子对之间的斥力;
ii、双键与双键之间的斥力>双键与单键之间的斥力>单键与单键之间的斥力;
iii、X原子得电子能力越弱,A—X形成的共用电子对之间的斥力越强;
iv、其他。
请仔细阅读上述材料,回答下列问题:
(1)由
 的
的 模型填写下表:
模型填写下表: | 2 | ① |
| VSEPR模型 | ② | 四面体形 |
| 价层电子对之间的键角 | ③ |  |
 模型解释
模型解释 为直线形分子的原因:
为直线形分子的原因:(3)
 分子的空间结构为
分子的空间结构为 的大小范围并解释原因:
的大小范围并解释原因:(4)
 和
和 都属于
都属于 型分子,S、O之间以双键结合,S与
型分子,S、O之间以双键结合,S与 、S与F之间以单键结合。请你预测
、S与F之间以单键结合。请你预测 和
和 分子的空间结构:
分子的空间结构: 分子中
分子中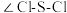
 分子中
分子中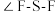 。
。
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】向盛有硫酸铜水溶液的试管里加入氨水,首先形成蓝色沉淀,继续添加氨水,沉淀溶解病得到深蓝色的透明液体;若向试管中加入一定量乙醇,析出深蓝色晶体。结合有关知识,回答下列问题:
(1)Cu、N、O、S元素第一电离能由大到小的顺序是_______ (填元素符号);蓝色沉淀溶解时发生反应的离子方程式是________________ 。
(2)请解释加入乙醇后析出晶体的原因______________ 。
(3)SO42-的空间构型是_____________ ,其中S原子的杂化轨道类型是___________ 。
(4)NH3、H2O分子中,键角的大小顺序为_______ (用分子式表示);NH3极易溶于H2O的原因,除了两种分子都是极性分子外,还因为_______________ 。
(5)Cu和O能形成一种化合物,其晶胞结构如图所示,则R所表示微粒的价电子排布式为_____ ;若相邻的两不同微粒间的距离为a cm,设阿伏伽德罗常数的数值为NA,则该晶体的密度为_______ (用含a、NA的代数式表示)g/cm3。
(1)Cu、N、O、S元素第一电离能由大到小的顺序是
(2)请解释加入乙醇后析出晶体的原因
(3)SO42-的空间构型是
(4)NH3、H2O分子中,键角的大小顺序为
(5)Cu和O能形成一种化合物,其晶胞结构如图所示,则R所表示微粒的价电子排布式为

您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)某元素原子的价电子构型为4s24p1,该元素的符号为________ 。
(2)某元素+3价离子的3d轨道半充满,该元素的符号为________ 。
(3)A元素的负二价离子和B元素的正二价离子的电子层结构都与氩相同,A的离子结构示意图为________ ,B的元素名称为________ 。
(4)如图,第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量。如图是部分元素原子的第一电离能I1随原子序数变化的曲线(其中12~17号元素的有关数据缺失)。
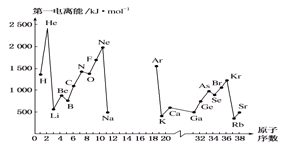
①认真分析图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围为________ <Al<________ ;(填元素符号)。
②图中第一电离能最小的元素在周期表中的位置是第________ 周期________ 族。
(2)某元素+3价离子的3d轨道半充满,该元素的符号为
(3)A元素的负二价离子和B元素的正二价离子的电子层结构都与氩相同,A的离子结构示意图为
(4)如图,第一电离能I1是指气态原子X(g)处于基态时,失去一个电子成为气态阳离子X+(g)所需的能量。如图是部分元素原子的第一电离能I1随原子序数变化的曲线(其中12~17号元素的有关数据缺失)。

①认真分析图中同周期元素第一电离能的变化规律,推断Na~Ar元素中,Al的第一电离能的大小范围为
②图中第一电离能最小的元素在周期表中的位置是第
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)如图为某原子3d能级的电子排布情况.

该排布情况违反了________ 原理
(2)s电子的原子轨道呈_________ 形,每个s能级有_________ 个原子轨道;p电子的原子轨道_________ 形,每个p能级有_________ 个原子轨道。
(3)填表

该排布情况违反了
(2)s电子的原子轨道呈
(3)填表
| 分子或离子 | CO2 | H2O | SO3 | NH4+ | N2O |
| VSEPR模型名称 | |||||
| 中心原子杂化轨道类型 | |||||
| 分子或离子立体构型 |
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】回答下列问题。
(1)在H-S、H-Cl两种共价键中,键的极性较强的是_______ ,键长较长的是_______ 。在四种酸①HClO4;②H2SO4;③HNO2;④HClO中,酸性由弱到强的顺序为_______ 。(用序号表示)
(2)下列气态分子①BeCl2;②BCl3;③CCl4;④H2O中,其键角由大到小的顺序为_______ 。(用序号表示)
(3)SO2与CO2在相同条件下两者在水中的溶解度较大的是____ (写分子式),理由是_____ 。
(1)在H-S、H-Cl两种共价键中,键的极性较强的是
(2)下列气态分子①BeCl2;②BCl3;③CCl4;④H2O中,其键角由大到小的顺序为
(3)SO2与CO2在相同条件下两者在水中的溶解度较大的是
您最近半年使用:0次



