二氧化碳的综合利用是环保领域研究的热点课题。
Ⅰ. 经过催化氢化合成低碳烯烃。
经过催化氢化合成低碳烯烃。
合成乙烯的反应为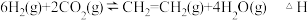
(1)已知几种化学键键能如下表所示:
则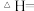
___________ (用含字母的代数式表示)。
(2)反应温度、投料比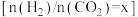 对
对 平衡转化率的影响如图1。
平衡转化率的影响如图1。
①
___________ 3(填“>”“<”或“=”,下同); 、
、 两点反应的平衡常数
两点反应的平衡常数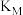
___________  。
。
②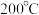 时,往
时,往 刚性密闭容器中加入
刚性密闭容器中加入 、
、 ,反应
,反应 达到平衡,则反应开始和平衡时的总压强比为
达到平衡,则反应开始和平衡时的总压强比为___________ 。
(3)某新型催化剂对 合成低碳烯烃在不同反应温度下的催化性能如图2。
合成低碳烯烃在不同反应温度下的催化性能如图2。
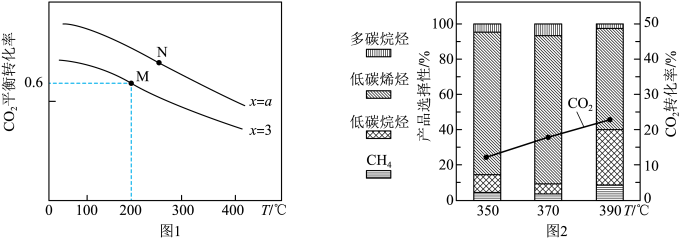
由图2可知,该反应最适宜的温度为___________ ,理由为___________ 。
Ⅱ. 经过电解转化为化工原料
经过电解转化为化工原料 。
。
(4)图3所示固体氧化物电解池利用具有优良催化活性的电极共电解 。
。
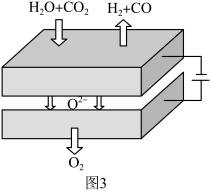
①阴极生成氢气的电极反应式为___________ 。
②电解过程中还伴随着积碳反应 。以下说法正确的是
。以下说法正确的是___________ (填标号)。
a.生成的碳覆盖在电极表面,影响电极的催化活性
b.生成的碳使电解效率降低
c.生成的碳会和电解产生的氧气反应
Ⅰ.
 经过催化氢化合成低碳烯烃。
经过催化氢化合成低碳烯烃。合成乙烯的反应为
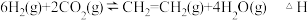
(1)已知几种化学键键能如下表所示:
| 物质 |  |  |  |  |  |
能量 |  |  |  |  |  |
则
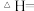
(2)反应温度、投料比
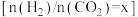 对
对 平衡转化率的影响如图1。
平衡转化率的影响如图1。①

 、
、 两点反应的平衡常数
两点反应的平衡常数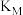
 。
。②
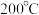 时,往
时,往 刚性密闭容器中加入
刚性密闭容器中加入 、
、 ,反应
,反应 达到平衡,则反应开始和平衡时的总压强比为
达到平衡,则反应开始和平衡时的总压强比为(3)某新型催化剂对
 合成低碳烯烃在不同反应温度下的催化性能如图2。
合成低碳烯烃在不同反应温度下的催化性能如图2。
由图2可知,该反应最适宜的温度为
Ⅱ.
 经过电解转化为化工原料
经过电解转化为化工原料 。
。(4)图3所示固体氧化物电解池利用具有优良催化活性的电极共电解
 。
。
①阴极生成氢气的电极反应式为
②电解过程中还伴随着积碳反应
 。以下说法正确的是
。以下说法正确的是a.生成的碳覆盖在电极表面,影响电极的催化活性
b.生成的碳使电解效率降低
c.生成的碳会和电解产生的氧气反应
更新时间:2021-05-15 10:35:45
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】氢能源是最具前景的应用能源之一,氢气的制备和应用是目前的研究热点。回答下列问题:
(1)氨气中氢含量高,可通过氨热分解法制氢气。一定温度下,利用催化剂将 分解为
分解为 和
和 ,反应过程中的能量变化如图所示。
,反应过程中的能量变化如图所示。
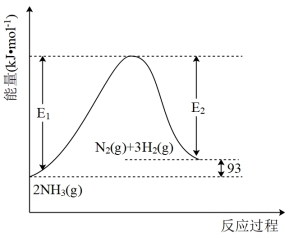
写出该反应的热化学方程式_______ 。
(2)已知断开(或形成) 键、
键、 键分别需要吸收(或放出)
键分别需要吸收(或放出)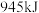 、
、 的热量,则断开
的热量,则断开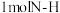 吸收的热量为
吸收的热量为_______  。利用该反应制备标况下
。利用该反应制备标况下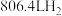 时,吸收的热量为
时,吸收的热量为_______ 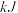 。
。
(3)《Science》杂志报道了我国研究团队发明的用 和
和 制取
制取 的绿色方法,原理如图所示。
的绿色方法,原理如图所示。
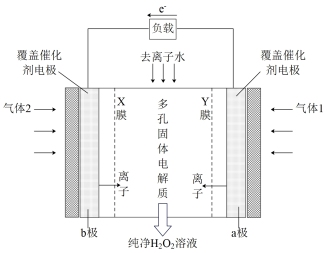
①a极上的电极反应式为_______ ,当生成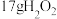 ,理论上需消耗标况下
,理论上需消耗标况下_______ L气体2。
②Y膜是选择性_______ (填“阳”或“阴”)离子交换膜。
(1)氨气中氢含量高,可通过氨热分解法制氢气。一定温度下,利用催化剂将
 分解为
分解为 和
和 ,反应过程中的能量变化如图所示。
,反应过程中的能量变化如图所示。
写出该反应的热化学方程式
(2)已知断开(或形成)
 键、
键、 键分别需要吸收(或放出)
键分别需要吸收(或放出)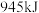 、
、 的热量,则断开
的热量,则断开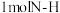 吸收的热量为
吸收的热量为 。利用该反应制备标况下
。利用该反应制备标况下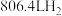 时,吸收的热量为
时,吸收的热量为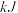 。
。(3)《Science》杂志报道了我国研究团队发明的用
 和
和 制取
制取 的绿色方法,原理如图所示。
的绿色方法,原理如图所示。
①a极上的电极反应式为
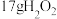 ,理论上需消耗标况下
,理论上需消耗标况下②Y膜是选择性
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】氮和硫的化合物在工农业生产、生活中具有重要应用。请回答下列问题:
(1)航天领域中常用肼 作为火箭发射的助燃剂。
作为火箭发射的助燃剂。
①已知各共价键键能如下表:
 ;
;
_______  。
。
② 与氨气相似,是一种碱性气体,易溶于水,生成弱碱
与氨气相似,是一种碱性气体,易溶于水,生成弱碱 。用电离方程式表示
。用电离方程式表示 显碱性的原因
显碱性的原因_______ 。
(2)查阅资料可知,常温下,部分弱电解质的电离平衡常数如表:
① 的电离平衡常数的表达式
的电离平衡常数的表达式
_______ ;
②常温下,等浓度的下列溶液a. 溶液;b.
溶液;b. 溶液;c.
溶液;c. 溶液,其
溶液,其 由大到小的顺序是
由大到小的顺序是_______ (用字母表示)。
(3)某同学设计一个肼 燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中
燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中 为阳离子交换膜。
为阳离子交换膜。_______ (填“正极”或“负极”),负极的电极反应式为_______ 。
②若甲中有 氧气(标准状况下)参加反应,乙中通过离子交换膜的阳离子个数为
氧气(标准状况下)参加反应,乙中通过离子交换膜的阳离子个数为____ ,丙中硫酸铜溶液的浓度_______ (填“变大”、“变小”或“不变”)。
(1)航天领域中常用肼
 作为火箭发射的助燃剂。
作为火箭发射的助燃剂。①已知各共价键键能如下表:
 |  |  |  |  | |
键能 | 946 | 497 | 193 | 391 | 463 |
 的结构如图
的结构如图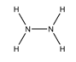
 ;
;
 。
。②
 与氨气相似,是一种碱性气体,易溶于水,生成弱碱
与氨气相似,是一种碱性气体,易溶于水,生成弱碱 。用电离方程式表示
。用电离方程式表示 显碱性的原因
显碱性的原因(2)查阅资料可知,常温下,部分弱电解质的电离平衡常数如表:
| 弱电解质 |  |  |  |
电离平衡常数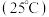 |  | 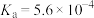 | 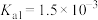 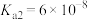 |
 的电离平衡常数的表达式
的电离平衡常数的表达式
②常温下,等浓度的下列溶液a.
 溶液;b.
溶液;b. 溶液;c.
溶液;c. 溶液,其
溶液,其 由大到小的顺序是
由大到小的顺序是(3)某同学设计一个肼
 燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中
燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中 为阳离子交换膜。
为阳离子交换膜。
②若甲中有
 氧气(标准状况下)参加反应,乙中通过离子交换膜的阳离子个数为
氧气(标准状况下)参加反应,乙中通过离子交换膜的阳离子个数为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】完成下列问题。
(1)下列变化中,属于放热反应的是___________ ,属于吸热反应的是___________ (填标号)
①酸碱中和反应;② 通过炽热的炭发生的反应;③石灰石在高温下的分解反应;④生石灰与水反应;⑤干冰升华;⑥
通过炽热的炭发生的反应;③石灰石在高温下的分解反应;④生石灰与水反应;⑤干冰升华;⑥ 与
与 的反应;⑦食物因氧化而腐败发生的反应;⑧苛性钠固体溶于水
的反应;⑦食物因氧化而腐败发生的反应;⑧苛性钠固体溶于水
(2)甲烷可消除 的污染,反应为
的污染,反应为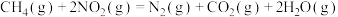 ,在
,在 密闭容器中,控制不同温度,分别加入
密闭容器中,控制不同温度,分别加入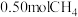 和
和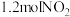 ,测得
,测得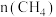 随时间变化的有关实验数据见表。
随时间变化的有关实验数据见表。
①组别A中,反应开始至 ,
,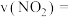
___________ mol∙L-1∙min-1。
②由实验数据可知实验控制的温度:
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
③一定条件下,能说明该反应进行到最大限度的是___________ (填序号)。
a.容器内 的物质的量分数不再随时间而发生变化
的物质的量分数不再随时间而发生变化
b. 的浓度为0
的浓度为0
c.体系内物质的平均相对分子质量保持不变
d.体系内气体的密度保持不变
(3)甲烷还是一种清洁燃料,也是一种重要的化工原料,已知部分共价键的键能如表所示:
则由 和
和 合成
合成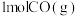 和
和 ,吸收的热量为
,吸收的热量为___________  。
。
(4)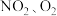 和熔融
和熔融 可制作燃料电池,其原理如图。
可制作燃料电池,其原理如图。

该电池在使用过程中石墨I电极上生成氧化物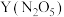 ,则石墨II电极是
,则石墨II电极是___________ (填“正极”或“负极”),石墨I电极反应式为:___________ 。
(1)下列变化中,属于放热反应的是
①酸碱中和反应;②
 通过炽热的炭发生的反应;③石灰石在高温下的分解反应;④生石灰与水反应;⑤干冰升华;⑥
通过炽热的炭发生的反应;③石灰石在高温下的分解反应;④生石灰与水反应;⑤干冰升华;⑥ 与
与 的反应;⑦食物因氧化而腐败发生的反应;⑧苛性钠固体溶于水
的反应;⑦食物因氧化而腐败发生的反应;⑧苛性钠固体溶于水(2)甲烷可消除
 的污染,反应为
的污染,反应为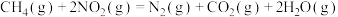 ,在
,在 密闭容器中,控制不同温度,分别加入
密闭容器中,控制不同温度,分别加入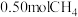 和
和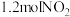 ,测得
,测得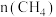 随时间变化的有关实验数据见表。
随时间变化的有关实验数据见表。| 组别 | 温度 | 时间/ 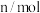 | 0 | 10 | 20 | 40 | 50 |
| A |  | 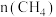 | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| B |  | 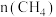 | 0.50 | 0.30 | 0.18 | 0.15 | 0.15 |
 ,
,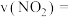
②由实验数据可知实验控制的温度:

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。③一定条件下,能说明该反应进行到最大限度的是
a.容器内
 的物质的量分数不再随时间而发生变化
的物质的量分数不再随时间而发生变化b.
 的浓度为0
的浓度为0c.体系内物质的平均相对分子质量保持不变
d.体系内气体的密度保持不变
(3)甲烷还是一种清洁燃料,也是一种重要的化工原料,已知部分共价键的键能如表所示:
| 化学键 |  |  |  |  |
键能 | 415 | 463 | 1076 | 436 |
 和
和 合成
合成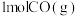 和
和 ,吸收的热量为
,吸收的热量为 。
。(4)
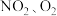 和熔融
和熔融 可制作燃料电池,其原理如图。
可制作燃料电池,其原理如图。
该电池在使用过程中石墨I电极上生成氧化物
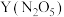 ,则石墨II电极是
,则石墨II电极是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】I.“嫦娥”五号预计在海南文昌发射中心发射,火箭的第一、二级发动机中,所用的燃料为偏二甲肼和四氧化二氮,偏二甲肼可用肼来制备。用肼(N2H4)作燃料,四氧化二氮作氧化剂,二者反应生成氮气和气态水。已知:
①N2(g)+2O2(g)=N2O4(g) ΔH=+10.7 kJ·mol-1
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1
(1)写出气态肼和N2O4反应的热化学方程式:_______ 。
II.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)⇌CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:
回答下列问题:
(2)该反应的化学平衡常数表达式为K=_______ 。
(3)该反应为_______ 反应(填“吸热”或“放热”)。
(4)某温度下,各物质的平衡浓度符合下式:3c(CO2)·c(H2)=5c(CO)·c(H2O),试判断此时的温度为_______ 。
(5)若830 ℃时,向容器中充入1 mol CO、5 mol H2O,反应达到平衡后,其化学平衡常数K_______ 1.0(填“大于”“小于”或“等于”)。
(6)830 ℃时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的体积。平衡_______ 移动(填“向正反应方向”“向逆反应方向”或“不”)。
①N2(g)+2O2(g)=N2O4(g) ΔH=+10.7 kJ·mol-1
②N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-543 kJ·mol-1
(1)写出气态肼和N2O4反应的热化学方程式:
II.在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)⇌CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:
| t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(2)该反应的化学平衡常数表达式为K=
(3)该反应为
(4)某温度下,各物质的平衡浓度符合下式:3c(CO2)·c(H2)=5c(CO)·c(H2O),试判断此时的温度为
(5)若830 ℃时,向容器中充入1 mol CO、5 mol H2O,反应达到平衡后,其化学平衡常数K
(6)830 ℃时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的体积。平衡
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】在某一容积为5L的体积不变的密闭容器内,加入0.3mol的CO和0.3mol的 ,在催化剂存在和800℃的条件下,发生反应:
,在催化剂存在和800℃的条件下,发生反应:
 ,
, 的浓度随时间变化情况如图:
的浓度随时间变化情况如图:

(1)可以说明该反应已达平衡的是_______ (填序号)。
①体系内压强不再改变 ② 的浓度不再改变
的浓度不再改变
③容器内气体的密度不再改变 ④
⑤
(2)根据图上数据,该温度(800℃)下的平衡常数
_______ 。若保持温度和容器的体积不变,在上述平衡体系中,再充入0.3 mol的水蒸气,重新达到平衡后, 的转化率
的转化率_______ (填升高、降低或不变)。
(3)在体积不变的条件下,改变下列条件能增大平衡常数K的有_______ (填字母)。
A.升高温度 B.降低温度 C.增大压强 D.加入一氧化碳气体 E.加入催化剂
(4)在800℃下,改变其他条件,测得在某一时刻
 mol⋅L-1;
mol⋅L-1;
 mol⋅L-1,则此时正、逆反应速率的大小:
mol⋅L-1,则此时正、逆反应速率的大小:
_______ (填“>”“<”或“=”) 。
。
 ,在催化剂存在和800℃的条件下,发生反应:
,在催化剂存在和800℃的条件下,发生反应:
 ,
, 的浓度随时间变化情况如图:
的浓度随时间变化情况如图:
(1)可以说明该反应已达平衡的是
①体系内压强不再改变 ②
 的浓度不再改变
的浓度不再改变③容器内气体的密度不再改变 ④

⑤

(2)根据图上数据,该温度(800℃)下的平衡常数

 的转化率
的转化率(3)在体积不变的条件下,改变下列条件能增大平衡常数K的有
A.升高温度 B.降低温度 C.增大压强 D.加入一氧化碳气体 E.加入催化剂
(4)在800℃下,改变其他条件,测得在某一时刻
 mol⋅L-1;
mol⋅L-1; mol⋅L-1,则此时正、逆反应速率的大小:
mol⋅L-1,则此时正、逆反应速率的大小:
 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】CO2是地球上取之不尽用之不竭的碳源,将CO2应用于生产中实现其综合利用是目前的研究热点。
(1)CO2加氢制备甲酸(HCOOH,熔点8.4℃沸点100.8℃)是利用化学载体进行H2储存的关键步骤。
已知:H2(g)+CO2(g) HCOOH(l) △H1=-30.0kJ•mol-1
HCOOH(l) △H1=-30.0kJ•mol-1
2H2(g)+O2(g)=2H2O(1) △H2=-571.6kJ•mol-1
则表示HCOOH燃烧热的热化学方程式为___ 。
(2)在催化作用下由CO2和CH4转化为CH3COOH的反应历程示意图如图。

①在合成CH3COOH的反应历程中,下列有关说法正确的是___ 。填(字母)
a.该催化剂使反应的平衡常数增大
b.CH4→CH3COOH过程中,有C—H键发生断裂
c.由X→Y过程中放出能量并形成了C—C键
②该条件下由CO2和CH4合成CH3COOH的化学方程式为___ 。
(3)CO2与H2在一定条件下反应可生成甲醇:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H<0。改变温度时,该反应中的所有物质都为气态,起始温度、容积均相同(T1℃、2L密闭容器)。实验过程中的部分数据见下表:
CH3OH(g)+H2O(g) △H<0。改变温度时,该反应中的所有物质都为气态,起始温度、容积均相同(T1℃、2L密闭容器)。实验过程中的部分数据见下表:
①实验I,前10min内的平均反应速率υ(CH3OH)=___ 。
②平衡时CH3OH的浓度:c(实验I)___ c(实验II)(填“>”、“<”或“=”,下同)。实验I中当其他条件不变时,若30min后只改变温度为T2℃,再次平衡时n(H2)=3.2mol,则T1___ T2。
③已知某温度下该反应的平衡常数K=160,开始时在密闭容器中只加入CO2和H2,反应10min时测得各组分的浓度如下表,则此时υ正___ υ逆。
(1)CO2加氢制备甲酸(HCOOH,熔点8.4℃沸点100.8℃)是利用化学载体进行H2储存的关键步骤。
已知:H2(g)+CO2(g)
 HCOOH(l) △H1=-30.0kJ•mol-1
HCOOH(l) △H1=-30.0kJ•mol-12H2(g)+O2(g)=2H2O(1) △H2=-571.6kJ•mol-1
则表示HCOOH燃烧热的热化学方程式为
(2)在催化作用下由CO2和CH4转化为CH3COOH的反应历程示意图如图。

①在合成CH3COOH的反应历程中,下列有关说法正确的是
a.该催化剂使反应的平衡常数增大
b.CH4→CH3COOH过程中,有C—H键发生断裂
c.由X→Y过程中放出能量并形成了C—C键
②该条件下由CO2和CH4合成CH3COOH的化学方程式为
(3)CO2与H2在一定条件下反应可生成甲醇:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H<0。改变温度时,该反应中的所有物质都为气态,起始温度、容积均相同(T1℃、2L密闭容器)。实验过程中的部分数据见下表:
CH3OH(g)+H2O(g) △H<0。改变温度时,该反应中的所有物质都为气态,起始温度、容积均相同(T1℃、2L密闭容器)。实验过程中的部分数据见下表:| 反应时间 | n(CO2)/mol | n(H2)/mol | n(CH3OH)/mol | n(H2O)/mol | |
| 实验I恒温恒容 | 0min | 2 | 6 | 0 | 0 |
| 10min | 4.5 | ||||
| 20min | 1 | ||||
| 30min | 1 | ||||
| 实验II绝热恒容 | 0min | 0 | 0 | 2 | 2 |
①实验I,前10min内的平均反应速率υ(CH3OH)=
②平衡时CH3OH的浓度:c(实验I)
③已知某温度下该反应的平衡常数K=160,开始时在密闭容器中只加入CO2和H2,反应10min时测得各组分的浓度如下表,则此时υ正
| 物质 | H2 | CO2 | CH3OH | H2O |
| 浓度/(mol·L-1) | 0.2 | 0.2 | 0.4 | 0.4 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】从废旧磷酸铁理电池的正极材料(含LiFePO4、石墨粉和铝箔等)中综合回收锂、铁和磷等的工艺流程如图所示:
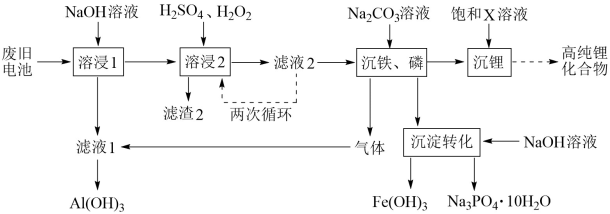
回答下列问题:
(1)“溶浸1”中铝溶解的化学方程式为________ 。
(2)完成“溶浸2”反应的离子方程式:____LiFePO4+___H2O2+____=_____Li++____+_____ +____H2O
+____H2O
__________
(3)“滤渣2”的主要成分是__________ 。
(4) “滤渣2”循环两次的目的是_______ 。
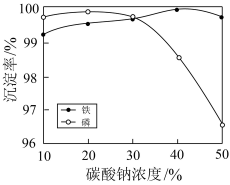
(5)“沉铁、磷”时,析出FePO4沉淀,反应的离子方程式为_______ 。实验中,铁、磷的沉淀率结果如图所示。碳酸钠浓度大于30%后,铁沉淀率仍然升高,磷沉淀率明显降低,其可能原因是_________ 。
(6)为了充分沉淀,“沉锂”时所用的X和适宜温度是_______ (填标号)。
A. NaOH 20-40℃ B. NaOH 80-100℃ C. Na2CO3 20-40℃ D. Na2CO3 60-80℃

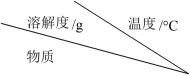 | 0 | 20 | 40 | 60 | 80 | 100 |
| LiOH | 11.9 | 12.4 | 13.2 | 14.6 | 16.6 | 19.1 |
| Li2CO3 | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
回答下列问题:
(1)“溶浸1”中铝溶解的化学方程式为
(2)完成“溶浸2”反应的离子方程式:____LiFePO4+___H2O2+____=_____Li++____+_____
 +____H2O
+____H2O(3)“滤渣2”的主要成分是
(4) “滤渣2”循环两次的目的是
(5)“沉铁、磷”时,析出FePO4沉淀,反应的离子方程式为

(6)为了充分沉淀,“沉锂”时所用的X和适宜温度是
A. NaOH 20-40℃ B. NaOH 80-100℃ C. Na2CO3 20-40℃ D. Na2CO3 60-80℃
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】氨是最重要的氮肥,是产量最大的化工产品之一,传统的工业合成氨技术是德国人哈伯(FritzHaber)在1905年发明的,因此也被称为哈伯法合成氨。哈伯本人也因此获得了1918年度诺贝尔化学奖。哈伯法合成氨需要20~50MPa的高压和500℃的高温,并用铁作催化剂。氢气和氮气在催化剂、高温、高压下合成氨,近一个世纪,全世界都这样生产氨。
(1)哈伯法制氨气的化学反应方程式为___ 。
(2)从结构角度分析植物难以利用氮气作为氮源的原因是___ 。
最近,韩国蔚山国家科学技术研究所(UNIST)与吉林大学、加拿大卡尔加里大学的研究人员合作,提出一种基于机械化学在温和条件下由氮气合成氨的新方案“球磨法”是在温和的条件下(45℃和1bar,1bar=100kPa)合成氨,氨的最终体积分数可高达82.5%。
该法分为两个步骤(如图):第一步,铁粉在球磨过程中被反复剧烈碰撞而活化,产生高密度的缺陷,氮分子被吸附在这些缺陷上([Fe(N*)]),有助于氮分子的解离。第二步,N*发生加氢反应得到NHx(x=1~3),剧烈碰撞中,NHx从催化剂表面脱附得到产物氨。

(3)“球磨法”与“哈伯法”相比较,下列说法中正确的是___ 。
A.催化剂(Fe)缺陷密度越高,N2的吸附率越高
B.“哈伯法”采用高温主要用于解离氮氮三键,而“球磨法”不用解离氮氮三键
C.“球磨法”中“剧烈碰撞”仅仅为了产生“活化缺陷”
D.“球磨法”不采用高压,是因为低压产率已经较高,加压会增大成本
(4)机械碰撞有助于催化剂缺陷的形成,而摩擦生热会使体系温度升高。图甲是N2吸附量、体系温度随球磨转速变化曲线,则应选择的最佳转速约___ 转/min;若选择500转/min的转速,N2的吸附量降低的原因是___ 。

(1)哈伯法制氨气的化学反应方程式为
(2)从结构角度分析植物难以利用氮气作为氮源的原因是
最近,韩国蔚山国家科学技术研究所(UNIST)与吉林大学、加拿大卡尔加里大学的研究人员合作,提出一种基于机械化学在温和条件下由氮气合成氨的新方案“球磨法”是在温和的条件下(45℃和1bar,1bar=100kPa)合成氨,氨的最终体积分数可高达82.5%。
该法分为两个步骤(如图):第一步,铁粉在球磨过程中被反复剧烈碰撞而活化,产生高密度的缺陷,氮分子被吸附在这些缺陷上([Fe(N*)]),有助于氮分子的解离。第二步,N*发生加氢反应得到NHx(x=1~3),剧烈碰撞中,NHx从催化剂表面脱附得到产物氨。

(3)“球磨法”与“哈伯法”相比较,下列说法中正确的是
A.催化剂(Fe)缺陷密度越高,N2的吸附率越高
B.“哈伯法”采用高温主要用于解离氮氮三键,而“球磨法”不用解离氮氮三键
C.“球磨法”中“剧烈碰撞”仅仅为了产生“活化缺陷”
D.“球磨法”不采用高压,是因为低压产率已经较高,加压会增大成本
(4)机械碰撞有助于催化剂缺陷的形成,而摩擦生热会使体系温度升高。图甲是N2吸附量、体系温度随球磨转速变化曲线,则应选择的最佳转速约

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】二氧化碳是主要的温室气体,也是一种工业原料。将其固定及利用,有利于缓解温室效应带来的环境问题。
(1)用二氧化碳合成甲醇。
已知:2H2(g)+O2(g)=2H2O(g) ∆H=-484kJ/mol
2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g) ∆H=-1348kJ/mol
在催化剂作用下,CO2(g)和H2(g)反应生成CH3OH(g)和H2O(g),该反应的热化学方程式是___________ 。
(2)用二氧化碳与环氧丙烷(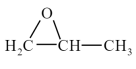 )反应合成可降解塑料PPC,同时也能生成副产物CPC,其化学反应过程中的能量变化如下图所示:在不同温度和压强下,PPC的选择性(产物中PPC的质量与产物总质量的比值)和总产率(产物总质量与反应物投料总质量的比值)如下表所示。
)反应合成可降解塑料PPC,同时也能生成副产物CPC,其化学反应过程中的能量变化如下图所示:在不同温度和压强下,PPC的选择性(产物中PPC的质量与产物总质量的比值)和总产率(产物总质量与反应物投料总质量的比值)如下表所示。
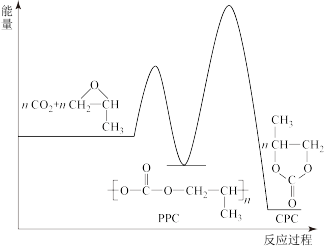
①通过表中数据ⅰ、ⅱ、ⅲ可以得出的结论是___________ 。在25℃时,实际生产中反应压强为1.5MPa,而不是2.0MPa,理由是___________ 。
②通过表中数据ⅱ、ⅳ、ⅴ可知温度升高会使PPC的选择性下降,结合上图说明其原因可能是___________ 。
(1)用二氧化碳合成甲醇。
已知:2H2(g)+O2(g)=2H2O(g) ∆H=-484kJ/mol
2CH3OH(g)+3O2(g)=2CO2(g)+4H2O(g) ∆H=-1348kJ/mol
在催化剂作用下,CO2(g)和H2(g)反应生成CH3OH(g)和H2O(g),该反应的热化学方程式是
(2)用二氧化碳与环氧丙烷(
 )反应合成可降解塑料PPC,同时也能生成副产物CPC,其化学反应过程中的能量变化如下图所示:在不同温度和压强下,PPC的选择性(产物中PPC的质量与产物总质量的比值)和总产率(产物总质量与反应物投料总质量的比值)如下表所示。
)反应合成可降解塑料PPC,同时也能生成副产物CPC,其化学反应过程中的能量变化如下图所示:在不同温度和压强下,PPC的选择性(产物中PPC的质量与产物总质量的比值)和总产率(产物总质量与反应物投料总质量的比值)如下表所示。
| 序号 | 温度/℃ | 压强/MPa | 总产率/% | PPC的选择性/% |
| ⅰ | 25 | 0.5 | 90 | 92.1 |
| ⅱ | 25 | 1.5 | 94.9 | >99 |
| ⅲ | 25 | 2.0 | 95.4 | >99 |
| ⅳ | 40 | 1.5 | 95.6 | 96.2 |
| ⅴ | 60 | 1.5 | 99 | 76 |
②通过表中数据ⅱ、ⅳ、ⅴ可知温度升高会使PPC的选择性下降,结合上图说明其原因可能是
您最近一年使用:0次
【推荐1】 对人类有着重要的作用。请回答下列问题:
对人类有着重要的作用。请回答下列问题:
(1)甲醇是一种绿色可再生能源,已知热化学方程式:
ⅰ.
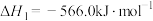
ⅱ.
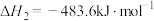
ⅲ.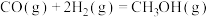

则计算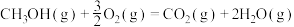 的
的
_______  。
。
(2)合成硝酸工艺中涉及到反应: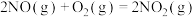 、
、 。
。 时,在恒容密闭容器中以投料比
时,在恒容密闭容器中以投料比 进行投料,容器内总压强p的变化如下表:
进行投料,容器内总压强p的变化如下表:
已知:a. 可认为迅速达到平衡状态。
可认为迅速达到平衡状态。
b.时间 时,NO(g)完全反应。
时,NO(g)完全反应。
①已知时间为 时,测得容器内
时,测得容器内 分压
分压 ,则此时NO的分压
,则此时NO的分压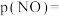
_______  。
。
② 时,可逆反应
时,可逆反应 的平衡常数
的平衡常数
_______  (用平衡分压代替平衡浓度计算,分压=总压×体积分数,写出计算式即可),
(用平衡分压代替平衡浓度计算,分压=总压×体积分数,写出计算式即可), 的平衡转化率为
的平衡转化率为_______ %(保留2位有效数字)。
③若将上述反应容器内温度升高至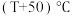 ,达到平衡时,容器内混合气体的平均相对分子质量减小,则
,达到平衡时,容器内混合气体的平均相对分子质量减小,则

_______ 0(填“>”或“<”)。)
(3)人体内化学反应时刻需要 参与,如广泛存在于肌肉中的肌红蛋白(Mb),具有结合
参与,如广泛存在于肌肉中的肌红蛋白(Mb),具有结合 的能力,可表示为
的能力,可表示为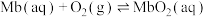 。肌红蛋白的结合度(即转化率α)与平衡时的氧气分压
。肌红蛋白的结合度(即转化率α)与平衡时的氧气分压 密切相关,其变化曲线如图1,37℃时,测得平衡常数
密切相关,其变化曲线如图1,37℃时,测得平衡常数 (气体和溶液中的溶质分别用分压和物质的量浓度表达)。
(气体和溶液中的溶质分别用分压和物质的量浓度表达)。
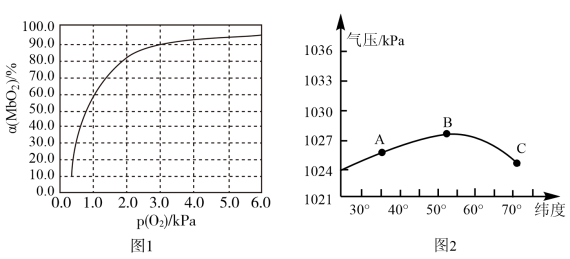
①平衡时,平衡常数表达式
_______ [用含α和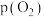 的代数式表示];37℃时,测得人正常呼吸时α的最大值为97.7%,则空气中氧气分压
的代数式表示];37℃时,测得人正常呼吸时α的最大值为97.7%,则空气中氧气分压
_______ kPa(保留3位有效数字)。
②某天不同纬度的大气压变化曲线如图2所术,某运动员处于A、B、C不同位置时,其体内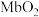 的浓度最大位置为
的浓度最大位置为_______ (填“A”“B”或“C”)。
(4)某碱性甲醇燃料电池原理如图所示。
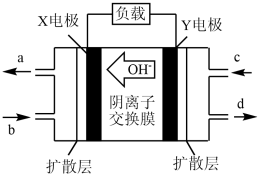
①Y电极区发生反应的电极反应式为_______ 。
②用上述电池做电源,电解饱和食盐水(电极均为惰性电极)。假设溶液体积300mL,当溶液的pH值由7变为13时(在常温下测定),理论上消耗甲醇的质量为_______ (忽略溶液体积变化)
 对人类有着重要的作用。请回答下列问题:
对人类有着重要的作用。请回答下列问题:(1)甲醇是一种绿色可再生能源,已知热化学方程式:
ⅰ.

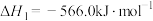
ⅱ.

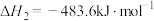
ⅲ.
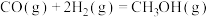

则计算
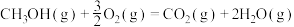 的
的
 。
。(2)合成硝酸工艺中涉及到反应:
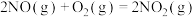 、
、 。
。 时,在恒容密闭容器中以投料比
时,在恒容密闭容器中以投料比 进行投料,容器内总压强p的变化如下表:
进行投料,容器内总压强p的变化如下表: | 0 | 40 | 80 | 160 | 260 | 700 | ∞ |
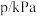 | 33.2 | 28.6 | 27.1 | 26.3 | 25.9 | 25.2 | 22.3 |
已知:a.
 可认为迅速达到平衡状态。
可认为迅速达到平衡状态。b.时间
 时,NO(g)完全反应。
时,NO(g)完全反应。①已知时间为
 时,测得容器内
时,测得容器内 分压
分压 ,则此时NO的分压
,则此时NO的分压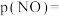
 。
。②
 时,可逆反应
时,可逆反应 的平衡常数
的平衡常数
 (用平衡分压代替平衡浓度计算,分压=总压×体积分数,写出计算式即可),
(用平衡分压代替平衡浓度计算,分压=总压×体积分数,写出计算式即可), 的平衡转化率为
的平衡转化率为③若将上述反应容器内温度升高至
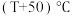 ,达到平衡时,容器内混合气体的平均相对分子质量减小,则
,达到平衡时,容器内混合气体的平均相对分子质量减小,则

(3)人体内化学反应时刻需要
 参与,如广泛存在于肌肉中的肌红蛋白(Mb),具有结合
参与,如广泛存在于肌肉中的肌红蛋白(Mb),具有结合 的能力,可表示为
的能力,可表示为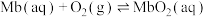 。肌红蛋白的结合度(即转化率α)与平衡时的氧气分压
。肌红蛋白的结合度(即转化率α)与平衡时的氧气分压 密切相关,其变化曲线如图1,37℃时,测得平衡常数
密切相关,其变化曲线如图1,37℃时,测得平衡常数 (气体和溶液中的溶质分别用分压和物质的量浓度表达)。
(气体和溶液中的溶质分别用分压和物质的量浓度表达)。
①平衡时,平衡常数表达式

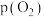 的代数式表示];37℃时,测得人正常呼吸时α的最大值为97.7%,则空气中氧气分压
的代数式表示];37℃时,测得人正常呼吸时α的最大值为97.7%,则空气中氧气分压
②某天不同纬度的大气压变化曲线如图2所术,某运动员处于A、B、C不同位置时,其体内
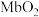 的浓度最大位置为
的浓度最大位置为(4)某碱性甲醇燃料电池原理如图所示。

①Y电极区发生反应的电极反应式为
②用上述电池做电源,电解饱和食盐水(电极均为惰性电极)。假设溶液体积300mL,当溶液的pH值由7变为13时(在常温下测定),理论上消耗甲醇的质量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上用电解 溶液生成的氯气为原料,生产溴酸钾
溶液生成的氯气为原料,生产溴酸钾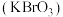 的工艺流程如下:
的工艺流程如下:
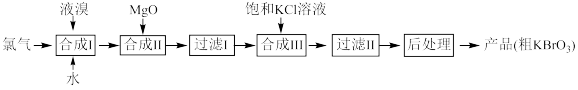
回答下列问题:
(1)惰性电极电解 溶液产生氯气总反应的离子方程式为
溶液产生氯气总反应的离子方程式为______________ 。
(2)“合成I”中得到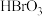 ,该反应的还原剂是
,该反应的还原剂是______________ ;“合成II”中加入 的目的是
的目的是____________ 。
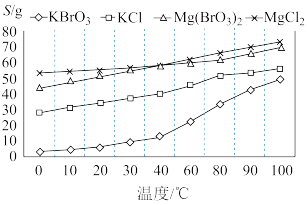
(3)结合溶解度曲线分析,“合成Ⅲ”为复分解反应,该反应能发生的原因是____________ ;若向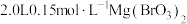 溶液中加入
溶液中加入______________  粉末,可使溶液中的
粉末,可使溶液中的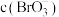 降为
降为 [假设溶液体积不变,已知该温度下
[假设溶液体积不变,已知该温度下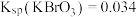 ]。“合成III”实际中用饱和
]。“合成III”实际中用饱和 溶液而不用
溶液而不用 粉末的优点是
粉末的优点是______________ (写一条)。
(4)为了从过滤II后的滤液中获得氯化镁结晶,依次要经过________ 、___________ 操作。
(5)另一种产生溴酸盐的方法是用 溶液吸收
溶液吸收 ,同时生成
,同时生成 气体。写出相应的化学方程式
气体。写出相应的化学方程式______________ ; 原子经济性更高的是
原子经济性更高的是______________ (填“ 吸收法”或“氯气氧化法”)。
吸收法”或“氯气氧化法”)。
 溶液生成的氯气为原料,生产溴酸钾
溶液生成的氯气为原料,生产溴酸钾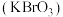 的工艺流程如下:
的工艺流程如下:
回答下列问题:
(1)惰性电极电解
 溶液产生氯气总反应的离子方程式为
溶液产生氯气总反应的离子方程式为(2)“合成I”中得到
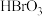 ,该反应的还原剂是
,该反应的还原剂是 的目的是
的目的是(3)结合溶解度曲线分析,“合成Ⅲ”为复分解反应,该反应能发生的原因是
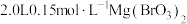 溶液中加入
溶液中加入 粉末,可使溶液中的
粉末,可使溶液中的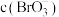 降为
降为 [假设溶液体积不变,已知该温度下
[假设溶液体积不变,已知该温度下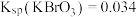 ]。“合成III”实际中用饱和
]。“合成III”实际中用饱和 溶液而不用
溶液而不用 粉末的优点是
粉末的优点是(4)为了从过滤II后的滤液中获得氯化镁结晶,依次要经过
(5)另一种产生溴酸盐的方法是用
 溶液吸收
溶液吸收 ,同时生成
,同时生成 气体。写出相应的化学方程式
气体。写出相应的化学方程式 原子经济性更高的是
原子经济性更高的是 吸收法”或“氯气氧化法”)。
吸收法”或“氯气氧化法”)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】铬及其化合物在催化、金属防腐等方面具有重要应用。回答下列问题:
(1) 属于
属于___________ 区元素。
(2) 催化丙烷脱氢过程中,部分反应历程如图,
催化丙烷脱氢过程中,部分反应历程如图, 过程的焓变为
过程的焓变为___________ (列式表示)。

(3) 溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
(i)

(ii)
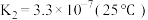
①下列有关 溶液的说法正确的有
溶液的说法正确的有___________ (填字母)。
a.加入少量硫酸溶液,溶液的pH不变
B.加入少量水稀释,溶液中所有离子的浓度均减小
C.加入少量硫酸溶液,反应(ⅰ)的平衡逆向移动
D.加入少量 固体,平衡时
固体,平衡时 与
与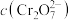 的比值保持不变
的比值保持不变
②25℃时, 溶液中,设
溶液中,设 、
、 与
与 的平衡浓度分别为x、y、
的平衡浓度分别为x、y、 ,则x、y、z之间的关系式为
,则x、y、z之间的关系式为___________ 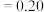
③电解铬酸钾溶液制备重铬酸钾的装置示意图如图所示,请写出该制备过程总反应的化学方程式为___________ 。

(1)
 属于
属于(2)
 催化丙烷脱氢过程中,部分反应历程如图,
催化丙烷脱氢过程中,部分反应历程如图, 过程的焓变为
过程的焓变为
(3)
 溶液中存在多个平衡。本题条件下仅需考虑如下平衡:
溶液中存在多个平衡。本题条件下仅需考虑如下平衡:(i)


(ii)

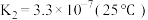
①下列有关
 溶液的说法正确的有
溶液的说法正确的有a.加入少量硫酸溶液,溶液的pH不变
B.加入少量水稀释,溶液中所有离子的浓度均减小
C.加入少量硫酸溶液,反应(ⅰ)的平衡逆向移动
D.加入少量
 固体,平衡时
固体,平衡时 与
与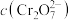 的比值保持不变
的比值保持不变②25℃时,
 溶液中,设
溶液中,设 、
、 与
与 的平衡浓度分别为x、y、
的平衡浓度分别为x、y、 ,则x、y、z之间的关系式为
,则x、y、z之间的关系式为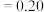
③电解铬酸钾溶液制备重铬酸钾的装置示意图如图所示,请写出该制备过程总反应的化学方程式为

您最近一年使用:0次




