下列关于化学键的说法,认识错误的是
① 键与
键与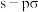 键的对称性不同
键的对称性不同
② 键不能单独存在,一定要和
键不能单独存在,一定要和 键共存
键共存
③含有 键的化合物与只含
键的化合物与只含 键的化合物的化学性质不同
键的化合物的化学性质不同
④两个非金属元素的原子之间形成的化学键都是共价键
⑤分子中含有共价键,则一定只含有一个 键
键
⑥成键的原子间原子轨道重叠越多,共价键越牢固
⑦1个N原子最多只能与3个H原子结合形成NH3分子,是由共价键的饱和性决定的
①
 键与
键与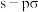 键的对称性不同
键的对称性不同②
 键不能单独存在,一定要和
键不能单独存在,一定要和 键共存
键共存③含有
 键的化合物与只含
键的化合物与只含 键的化合物的化学性质不同
键的化合物的化学性质不同④两个非金属元素的原子之间形成的化学键都是共价键
⑤分子中含有共价键,则一定只含有一个
 键
键⑥成键的原子间原子轨道重叠越多,共价键越牢固
⑦1个N原子最多只能与3个H原子结合形成NH3分子,是由共价键的饱和性决定的
| A.①⑤ | B.②⑥ | C.③⑦ | D.②④ |
更新时间:2021-05-11 16:59:44
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】设NA为阿伏加德罗常数的值。下列说法错误的是
A.1mol 中配位键数为2NA 中配位键数为2NA |
| B.31g白磷分子中孤电子对数为NA |
C.标况下,11.2L 中σ键数为NA 中σ键数为NA |
D.常温下,1molNO与0.5mol 混合后分子数为NA 混合后分子数为NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】固体A的化学式为NH5 , 它的所有原子的电子层结构都跟该原子同周期的稀有气体原子一样,NH5能跟水反应,化学方程式为:NH5+H2O=NH3•H2O+H2↑.则下列说法中,不正确的是( )
| A.NH5跟水的反应中,H2既是氧化产物又是还原产物 |
| B.NH5中既有共价键,又有离子键,属于离子化合物 |
| C.NH5跟水的反应是氧化还原反应 |
| D.1molNH5中有5NA个N﹣H键(NA为阿伏伽德罗常数的值) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】硝基胍的结构简式如图所示(“→”是一种特殊的共价单键,属于σ键)。下列说法正确的是

| A.硝基胍分子中只含极性键,不含非极性键 | B.N原子间只能形成σ键 |
C.硝基胍分子中σ键与π键的个数比是 | D.10.4g硝基胍中含有 个原子 个原子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】由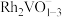 簇介导的光辅助水蒸气重整甲烷的两个连续催化循环机理如图所示(“UV”代表紫外线)。下列说法错误的是
簇介导的光辅助水蒸气重整甲烷的两个连续催化循环机理如图所示(“UV”代表紫外线)。下列说法错误的是
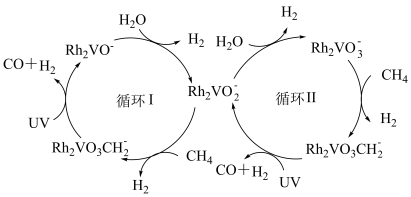
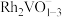 簇介导的光辅助水蒸气重整甲烷的两个连续催化循环机理如图所示(“UV”代表紫外线)。下列说法错误的是
簇介导的光辅助水蒸气重整甲烷的两个连续催化循环机理如图所示(“UV”代表紫外线)。下列说法错误的是
| A.反应过程中有极性键的断裂和生成 |
B.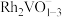 都有可能在循环中作催化剂 都有可能在循环中作催化剂 |
| C.反应过程中金属元素Rh、V的价态均不变 |
D.该循环的总反应为: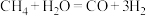 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列关于物质的结构或性质以及解释均正确的是
| 选项 | 物质的结构与性质 | 解释 |
| A | 键角: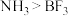 |  中 中 的孤电子对数比 的孤电子对数比 中 中 的孤电子对数多 的孤电子对数多 |
| B | 酸性: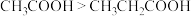 | 烃基(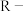 )越长推电子效应越大,使羧基中羟基的极性越小,羧酸的酸性越弱 )越长推电子效应越大,使羧基中羟基的极性越小,羧酸的酸性越弱 |
 |  的熔点比干冰高 的熔点比干冰高 |  比 比 相对分子量大,分子间作用力大 相对分子量大,分子间作用力大 |
 | 稳定性: |  分子间存在氢键 分子间存在氢键 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】键能的大小可以衡量化学键的强弱。下列说法中错误的是
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能/kJ·mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
| A.C-C的键能大于Si-Si |
| B.HCl的稳定性比HI稳定性高 |
| C.SiCl4的熔点比SiC熔点低 |
| D.拆开1 mol四氯化硅中的化学键所吸收的能量为360 kJ |
您最近一年使用:0次

 的电子式为
的电子式为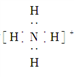 ,离子呈平面正方形结构
,离子呈平面正方形结构 、MgO的熔点由低到高
、MgO的熔点由低到高 分子内键角依次减小
分子内键角依次减小

