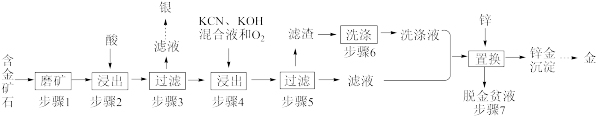
金、银是生活中常见的贵金属,用途非常广泛。工业上常利用氰化法从一种含金矿石(成分为Au、Ag、Fe2O3和其它不溶性杂质)中提取金。工艺流程如下:
已知:① Zn + O2 + H2O = Zn(OH)2
O2 + H2O = Zn(OH)2
②Zn2+(aq)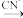 Zn(CN)2(s)
Zn(CN)2(s) 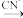 Zn(CN)
Zn(CN) (aq)
(aq)
(1)步骤1中“磨矿”的目的是___________ 。
(2)步骤2中浸出应选用___________ (填盐酸、硫酸或硝酸)。
(3)步骤4浸出的目的是将单质Au转化为Au(CN) 进入溶液,该反应的离子方程式为
进入溶液,该反应的离子方程式为___________ 。
(4)步骤4中为提高金的浸出速率可适当升高温度,但温度过高浸出速率反而会降低,原因是___________ 。
(5)步骤6的目的是___________ 。
(6)步骤7置换的总反应为:2Au(CN) +3Zn+4CN-+2H2O=2Au +2Zn(CN)
+3Zn+4CN-+2H2O=2Au +2Zn(CN) +ZnO
+ZnO +2H2↑,该过程中,为防止生成Zn(CN)2沉淀影响置换速率,可采取的措施是
+2H2↑,该过程中,为防止生成Zn(CN)2沉淀影响置换速率,可采取的措施是___________ 。
(7)脱金贫液(主要含有CN-)会破坏环境,可通过化学方法转化为无毒废水净化排放。碱性条件下,用NaClO将贫液中的CN- 氧化成无毒的CO 和N2,该反应的离子方程式为
和N2,该反应的离子方程式为___________ 。

已知:① Zn +
 O2 + H2O = Zn(OH)2
O2 + H2O = Zn(OH)2②Zn2+(aq)
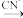 Zn(CN)2(s)
Zn(CN)2(s)  Zn(CN)
Zn(CN) (aq)
(aq)(1)步骤1中“磨矿”的目的是
(2)步骤2中浸出应选用
(3)步骤4浸出的目的是将单质Au转化为Au(CN)
 进入溶液,该反应的离子方程式为
进入溶液,该反应的离子方程式为(4)步骤4中为提高金的浸出速率可适当升高温度,但温度过高浸出速率反而会降低,原因是
(5)步骤6的目的是
(6)步骤7置换的总反应为:2Au(CN)
 +3Zn+4CN-+2H2O=2Au +2Zn(CN)
+3Zn+4CN-+2H2O=2Au +2Zn(CN) +ZnO
+ZnO +2H2↑,该过程中,为防止生成Zn(CN)2沉淀影响置换速率,可采取的措施是
+2H2↑,该过程中,为防止生成Zn(CN)2沉淀影响置换速率,可采取的措施是(7)脱金贫液(主要含有CN-)会破坏环境,可通过化学方法转化为无毒废水净化排放。碱性条件下,用NaClO将贫液中的CN- 氧化成无毒的CO
 和N2,该反应的离子方程式为
和N2,该反应的离子方程式为
更新时间:2021-05-24 21:13:38
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】碱式碳酸钴用作催化剂及制钴盐原料,陶瓷工业着色剂,电子、磁性材料的添加剂。利用以下装置测定碱式碳酸钴[Cox(OH)y(CO3)z•H2O]的化学组成。
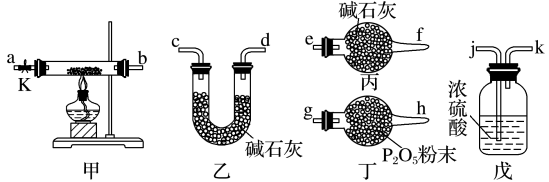
已知:碱式碳酸钴中钴为+2价,受热时可分解生成三种氧化物。
请回答下列问题:
(1)选用以上部分装置组装测定碱式碳酸钴[Cox(OH)y(CO3)z•H2O]的化学组成,其中戊的作用____ 。
(2)样品分解完,打开止水夹K,缓缓通入氮气数分钟,通入氮气的目的是____ 。
(3)取碱式碳酸钴样品34.9g,通过实验测得分解生成的水和二氧化碳的质量分别为3.6g、8.8g,则该碱式碳酸钴的化学式为____ 。
(4)某兴趣小组以含钴废料(含少量Fe、Al等杂质)制取CoCl2•6H2O的一种实验设计流程如图:

已知:25℃时
①操作I用到的玻璃仪器主要有_____ 。
②加盐酸酸浸后,继续加盐酸调pH为2~3的目的是____ 。
③操作II的过程为____ 、过滤、洗涤、干燥。

已知:碱式碳酸钴中钴为+2价,受热时可分解生成三种氧化物。
请回答下列问题:
(1)选用以上部分装置组装测定碱式碳酸钴[Cox(OH)y(CO3)z•H2O]的化学组成,其中戊的作用
(2)样品分解完,打开止水夹K,缓缓通入氮气数分钟,通入氮气的目的是
(3)取碱式碳酸钴样品34.9g,通过实验测得分解生成的水和二氧化碳的质量分别为3.6g、8.8g,则该碱式碳酸钴的化学式为
(4)某兴趣小组以含钴废料(含少量Fe、Al等杂质)制取CoCl2•6H2O的一种实验设计流程如图:

已知:25℃时
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 |
| 开始沉淀pH | 1.9 | 7.0 | 7.6 | 3.4 |
| 完全沉淀pH | 3.2 | 9.0 | 9.2 | 4.7 |
②加盐酸酸浸后,继续加盐酸调pH为2~3的目的是
③操作II的过程为
您最近一年使用:0次
【推荐2】亚氯酸钠( )是一种高效氧化剂、漂白剂。
)是一种高效氧化剂、漂白剂。 的一种生产工艺如图所示。
的一种生产工艺如图所示。

(1)一种方法是:在一定条件下,将 通入填充有固体
通入填充有固体 的反应柱内将其氧化为
的反应柱内将其氧化为 ,该反应的化学方程式为
,该反应的化学方程式为_______ 。
(2)“吸收”反应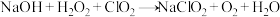 (未配平)中,氧化剂与还原剂的质量之比为
(未配平)中,氧化剂与还原剂的质量之比为_______ 。
(3)图中生产工艺制得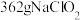 ,理论上需要消耗
,理论上需要消耗 的质量为
的质量为_______ 。
(4)已知:ⅰ. 在高于60℃时不稳定,易分解生成
在高于60℃时不稳定,易分解生成 和
和 。
。
ⅱ. 的溶解度曲线如图所示。
的溶解度曲线如图所示。

①写出 分解反应的化学方程式:
分解反应的化学方程式:_______ 。
②结合题中数据分析,从 溶液中获得
溶液中获得 固体的具体操作为:先将
固体的具体操作为:先将 溶液
溶液_______ ,最后过滤、洗涤、晾干,得到 固体。
固体。
 )是一种高效氧化剂、漂白剂。
)是一种高效氧化剂、漂白剂。 的一种生产工艺如图所示。
的一种生产工艺如图所示。
(1)一种方法是:在一定条件下,将
 通入填充有固体
通入填充有固体 的反应柱内将其氧化为
的反应柱内将其氧化为 ,该反应的化学方程式为
,该反应的化学方程式为(2)“吸收”反应
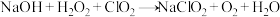 (未配平)中,氧化剂与还原剂的质量之比为
(未配平)中,氧化剂与还原剂的质量之比为(3)图中生产工艺制得
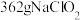 ,理论上需要消耗
,理论上需要消耗 的质量为
的质量为(4)已知:ⅰ.
 在高于60℃时不稳定,易分解生成
在高于60℃时不稳定,易分解生成 和
和 。
。ⅱ.
 的溶解度曲线如图所示。
的溶解度曲线如图所示。
①写出
 分解反应的化学方程式:
分解反应的化学方程式:②结合题中数据分析,从
 溶液中获得
溶液中获得 固体的具体操作为:先将
固体的具体操作为:先将 溶液
溶液 固体。
固体。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】硫酸铜是一种应用极其广泛的化工原料;以下是某工厂用含铁废铜为原料生产胆矾(CuSO4·5H2 O)和副产物石膏(CaSO4·2H2O)的生产流程示意图:
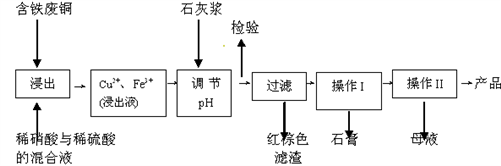
胆矾和石膏在不同温度下的溶解度(g/100g水)见下表。
请回答下列问题:
(1)红棕色滤渣的主要成分是__________________ 。
(2)写出浸出过程中生成铜离子的离子方程式________________________________________ 。
(3)操作I包括蒸发浓缩、__________ 等操作,温度应该控制在_____  左右;
左右;
(4)从溶液中分离出硫酸铜晶体操作Ⅱ应采用_______ 结晶;晶体用无水乙醇作洗涤液而不用蒸馏水的原因是_______________________________________ ;干燥时采用晾干,不用加热烘干的原因是_________________________ 。

胆矾和石膏在不同温度下的溶解度(g/100g水)见下表。
温度( ) ) | 20 | 40 | 60 | 80 | 100 |
| 石膏(g) | 0.32 | 0.26 | 0.15 | 0.11 | 0.07 |
| 胆矾(g) | 32 | 44.6 | 61.8 | 83.8 | 114 |
请回答下列问题:
(1)红棕色滤渣的主要成分是
(2)写出浸出过程中生成铜离子的离子方程式
(3)操作I包括蒸发浓缩、
 左右;
左右;(4)从溶液中分离出硫酸铜晶体操作Ⅱ应采用
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】对牙膏的探究要用到许多化学知识。
(1)下表列出了两种牙膏中的摩擦剂,请在表中填写两种摩擦剂所属的物质类别。
(2)根据你的推测,牙膏摩擦剂的溶解性是___ (填“易溶”或“难溶”)。
(3)牙膏中的摩擦剂碳酸钙可以用石灰石来制备。甲同学设计了一种实验室制备碳酸钙的实验方案,其流程图为:

请写出上述方案中步骤3的化学方程式:___ 。
(4)乙同学的实验方案如图,其优点为___ 。

(1)下表列出了两种牙膏中的摩擦剂,请在表中填写两种摩擦剂所属的物质类别。
| 牙膏 | A牙膏 | B牙膏 |
| 摩擦剂 | 碳酸钙 | 二氧化硅 |
| 摩擦剂的物质类别 |
(3)牙膏中的摩擦剂碳酸钙可以用石灰石来制备。甲同学设计了一种实验室制备碳酸钙的实验方案,其流程图为:

请写出上述方案中步骤3的化学方程式:
(4)乙同学的实验方案如图,其优点为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】重晶石矿的主要成分为硫酸钡,纯净的硫酸钡才能供医用作“钡餐”。硫化钡是可溶于水的盐。讨论用重晶石矿制硫酸钡,设计流程如图:
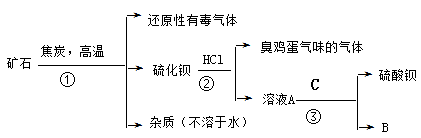
(1)写出步骤①的化学反应方程式_______ ,该反应产生的气体具有_______ 、_______ 等用途。
(2)为进行反应②先要分离出硫化钡,采用的方法是_______ 。反应前要在溶液中滴入少量Ba(OH)2溶液,其作用是:_______ 。
(3)若B物质在该生产过程中可循环使用,则反应③的化学方程式是:_______ 。
(4)有人提出反应②产生了有臭鸡蛋气味的有毒气体,可采用改变反应物的方法避免产生该气体,则反应②的化学方程式是:_______ 。此时若要B物质还能循环使用,则C为_______ (写化学式)。BaSO4是因为具有_______ 、_______ 等性质而可用作“钡餐”。

(1)写出步骤①的化学反应方程式
(2)为进行反应②先要分离出硫化钡,采用的方法是
(3)若B物质在该生产过程中可循环使用,则反应③的化学方程式是:
(4)有人提出反应②产生了有臭鸡蛋气味的有毒气体,可采用改变反应物的方法避免产生该气体,则反应②的化学方程式是:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】工业生产中会产生大量的废铁屑,可将其“变废为宝”制成化工原料氯化铁。实验室中利用下图所示装置探究由废铁屑制备FeCl3·6H2O晶体的原理并测定铁屑中铁单质的质量分数(杂质不溶于水且不与酸反应)。

(1)装置A的名称为____________________ 。
(2)检验该装置气密性的具体操作如下:
①关闭_____________ ;打开弹簧夹K1;
②向水准管中加水,使水准管液面高于量气管液面;
③_________________ 。
取m g废铁屑加入B装置中,在A中加入足量的盐酸后进行下列操作:
Ⅰ.打开弹簧夹K1,关闭活塞b,打开活塞a,缓慢滴加盐酸。
Ⅱ.当装置D的量气管一侧液面不再下降时,关闭弹簧夹K1,打开活塞b,当A中溶液完全进入烧杯后关闭活塞a、b。
Ⅲ.将烧杯中的溶液经过一系列操作后得到FeCl3·6H2O晶体。
请回答:
(3)用离子方程式表示烧杯中足量的H2O2溶液的作用:____________________ 。
(4)实验结束后,量气管和水准管内液面高度如上图所示,为了使两者液面相平,应将水准管_____ (填“上移”或“下移”)。
(5)由FeCl3溶液制得FeCl3•6H2O晶体的操作过程中不需要使用的仪器有_____ (填选项序号)。
a.蒸发皿
b.烧杯
c.酒精灯
d.分液漏斗
e.坩埚
f.玻璃棒
g.漏斗
(6)实验结束后,若量气管内共收集到VmL气体(已换算成标准状况),则此废铁屑中铁单质的质量分数为_________________ 。

(1)装置A的名称为
(2)检验该装置气密性的具体操作如下:
①关闭
②向水准管中加水,使水准管液面高于量气管液面;
③
取m g废铁屑加入B装置中,在A中加入足量的盐酸后进行下列操作:
Ⅰ.打开弹簧夹K1,关闭活塞b,打开活塞a,缓慢滴加盐酸。
Ⅱ.当装置D的量气管一侧液面不再下降时,关闭弹簧夹K1,打开活塞b,当A中溶液完全进入烧杯后关闭活塞a、b。
Ⅲ.将烧杯中的溶液经过一系列操作后得到FeCl3·6H2O晶体。
请回答:
(3)用离子方程式表示烧杯中足量的H2O2溶液的作用:
(4)实验结束后,量气管和水准管内液面高度如上图所示,为了使两者液面相平,应将水准管
(5)由FeCl3溶液制得FeCl3•6H2O晶体的操作过程中不需要使用的仪器有
a.蒸发皿
b.烧杯
c.酒精灯
d.分液漏斗
e.坩埚
f.玻璃棒
g.漏斗
(6)实验结束后,若量气管内共收集到VmL气体(已换算成标准状况),则此废铁屑中铁单质的质量分数为
您最近一年使用:0次



