宁夏银川市第六中学2021届高三第五次模拟考试理综化学试卷
宁夏
高三
模拟预测
2021-06-06
453次
整体难度:
适中
考查范围:
认识化学科学、有机化学基础、物质结构与性质、常见无机物及其应用、化学实验基础、化学反应原理
宁夏银川市第六中学2021届高三第五次模拟考试理综化学试卷
宁夏
高三
模拟预测
2021-06-06
453次
整体难度:
适中
考查范围:
认识化学科学、有机化学基础、物质结构与性质、常见无机物及其应用、化学实验基础、化学反应原理
一、单选题 添加题型下试题
单选题
|
容易(0.94)
名校
解题方法
1. 《黄帝内经》说:“五谷为养,五果为助,五畜为益,五菜为充”,以上食物中富含糖类、油脂、蛋白质等营养物质。下列说法正确的是
| A.“五谷”富含淀粉,淀粉是天然高分子化合物 |
| B.“五果”富含糖类,其中的葡萄糖、蔗糖和纤维素互为同系物 |
| C.“五畜”富含油脂和蛋白质,它们的组成元素相同 |
| D.“五菜”富含维生素,其中维生素C具有较强氧化性,常用做抗氧化剂 |
【知识点】 氧化还原反应的几组概念解读 糖类综合 蛋白质组成结构
您最近一年使用:0次
2021-04-09更新
|
625次组卷
|
5卷引用:吉林省长春市普通高中2021届高三4月质量监测(三)理综化学试卷题
单选题
|
适中(0.65)
名校
2. 羟甲香豆素(MSDS)又称利胆通,是一种新型利胆药物,常用作医药中间体,有关MSDS下列说法正确的是
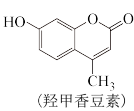

| A.该物质属于芳香烃 |
| B.可发生氧化反应 |
| C.不能使酸性高锰酸钾溶液褪色 |
| D.1mol该物质最多能与3molH2发生加成反应 |
您最近一年使用:0次
2021-03-03更新
|
730次组卷
|
4卷引用:广东省珠海市2021届高三第一次学业质量监测化学试题
广东省珠海市2021届高三第一次学业质量监测化学试题(已下线)2021年高考化学押题预测卷(新课标Ⅱ卷)(02)(含考试版、答题卡、参考答案、全解全析)宁夏银川市第六中学2021届高三第五次模拟考试理综化学试卷黑龙江省哈尔滨市第六中学2020-2021学年高二6月月考化学试题
单选题
|
较易(0.85)
名校
解题方法
3. 原子序数依次增大的短周期元素 X、Y、Z、R,含 0.9%YR的水溶液称为生理盐水,X、Y、Z三种元素组成两种化合物 A、B 的性质如图,Z的质子数是X质子数的2 倍。下列说法正确的是


| A.简单氢化物沸点 Z>X |
| B.简单离子半径 X<Y<Z<R |
| C.Y与X形成的一种化合物含有离子键和非极性键 |
| D.化合物 A 和 B的水溶液皆呈中性 |
您最近一年使用:0次
2021-03-03更新
|
535次组卷
|
4卷引用:广东省珠海市2021届高三第一次学业质量监测化学试题
广东省珠海市2021届高三第一次学业质量监测化学试题(已下线)小题15 元素周期表、律(根据物质性质角度的元素推断)——备战2021年高考化学经典小题考前必刷(全国通用)宁夏银川市第六中学2021届高三第五次模拟考试理综化学试卷湖南省湘潭市湘潭县第一中学2021-2022学年高三下学期5月月考化学试题
单选题
|
较易(0.85)
名校
解题方法
4. 根据下列实验操作和现象所得出的结论正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向3mLKI溶液中滴加几滴溴水,振荡,再滴加1mL淀粉溶液,溶液显蓝色 | Br2的氧化性比I2的强 |
| B | 向蛋白质溶液中分别加入甲醛和 饱和溶液,均有固体析出 饱和溶液,均有固体析出 | 蛋白质均发生了变性 |
| C | 向苯酚浊液中滴加Na2CO3溶液,浊液变清 | 苯酚的酸性强于碳酸的酸性 |
| D | 向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀 | 气体X具有强氧化性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-03-03更新
|
669次组卷
|
5卷引用:广东省珠海市2021届高三第一次学业质量监测化学试题
广东省珠海市2021届高三第一次学业质量监测化学试题宁夏银川市第六中学2021届高三第五次模拟考试理综化学试卷(已下线)考点32 化学实验方案设计与评价-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点35 化学实验方案的设计与评价-备战2022年高考化学一轮复习考点帮(浙江专用)广东省佛山市第一中学2021-2022学年高三上学期第二次段考化学试题
单选题
|
适中(0.65)
名校
5. 碳酸二甲酯(DMC)具有优良的化学反应性能。在众多研究方向中,CO2和甲醇直接合成DMC的方法受到了较多的关注,M2O(OH)催化该反应的一种反应机理如图所示。下列叙述正确的是


| A.M2O(OH)是反应的催化剂,H2O是反应中间体 |
| B.DMC中所有原子可能共面 |
| C.DMC的同分异构体中同时含有羧基和羟基两种官能团的物质有2种(不考虑立体异构) |
| D.反应①②③均为取代反应 |
您最近一年使用:0次
2021-04-09更新
|
421次组卷
|
3卷引用:吉林省长春市普通高中2021届高三4月质量监测(三)理综化学试卷题
单选题
|
较难(0.4)
名校
6. 一种新型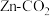 水介质电池,为解决环境和能源问题提供了一种新途径,其工作示意图如图所示,下列说法
水介质电池,为解决环境和能源问题提供了一种新途径,其工作示意图如图所示,下列说法不正确 的是

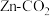 水介质电池,为解决环境和能源问题提供了一种新途径,其工作示意图如图所示,下列说法
水介质电池,为解决环境和能源问题提供了一种新途径,其工作示意图如图所示,下列说法
| A.放电时,金属锌为负极 |
B.放电时,温室气体 被转化为储氢物质HCOOH 被转化为储氢物质HCOOH |
C.充电时,电池总反应为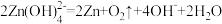 |
D.充电时,双极隔膜产生的 向右侧正极室移动 向右侧正极室移动 |
【知识点】 原电池、电解池综合考查解读
您最近一年使用:0次
2021-04-10更新
|
912次组卷
|
5卷引用:北京市房山区2021届高三一模化学试题
北京市房山区2021届高三一模化学试题(已下线)难点4 电化学原理及其应用-2021年高考化学【热点·重点·难点】专练(山东专用)宁夏银川市第六中学2021届高三第五次模拟考试理综化学试卷(已下线)专题06 电化学原理应用—2022年高考化学二轮复习讲练测(全国版)-测试北京市西城区第一六一中学2022届高三考前热身测试化学试题
单选题
|
适中(0.65)
名校
7. 甲酸甲酯是重要的有机化工原料,制备反应为 ,相同时间内,在容积固定的密闭容器中,使反应在不同温度下进行(起始投料比
,相同时间内,在容积固定的密闭容器中,使反应在不同温度下进行(起始投料比 均为1),测得CO的转化率随温度变化的曲线如图所示。下列说法中,
均为1),测得CO的转化率随温度变化的曲线如图所示。下列说法中,不正确 的是

 ,相同时间内,在容积固定的密闭容器中,使反应在不同温度下进行(起始投料比
,相同时间内,在容积固定的密闭容器中,使反应在不同温度下进行(起始投料比 均为1),测得CO的转化率随温度变化的曲线如图所示。下列说法中,
均为1),测得CO的转化率随温度变化的曲线如图所示。下列说法中,
A.a点对应的CO的转化率与 的转化率相同 的转化率相同 |
B.b点和e点的平衡常数: |
| C.70~80℃,CO转化率随温度升高而增大,其原因是升高温度反应速率增大 |
| D.85~90℃,CO转化率随温度升高而降低,其原因可能是升高温度平衡逆向移动 |
您最近一年使用:0次
2021-04-10更新
|
419次组卷
|
6卷引用:北京市房山区2021届高三一模化学试题
北京市房山区2021届高三一模化学试题(已下线)难点5 化学反应速率与化学平衡图表分析-2021年高考化学【热点·重点·难点】专练(山东专用)(已下线)押山东卷第14题 化学反应速率和平衡-备战2021年高考化学临考题号押题(山东卷)宁夏银川市第六中学2021届高三第五次模拟考试理综化学试卷湖南省湘潭市湘潭县第一中学2021-2022学年高三下学期5月月考化学试题浙江省余姚中学2023-2024学年高二上学期第一次月考化学试题
二、解答题 添加题型下试题
解答题-工业流程题
|
适中(0.65)
名校
解题方法
8. 金、银是生活中常见的贵金属,用途非常广泛。工业上常利用氰化法从一种含金矿石(成分为Au、Ag、Fe2O3和其它不溶性杂质)中提取金。工艺流程如下:
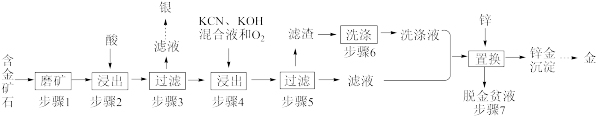
已知:① Zn + O2 + H2O = Zn(OH)2
O2 + H2O = Zn(OH)2
②Zn2+(aq)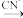 Zn(CN)2(s)
Zn(CN)2(s) 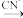 Zn(CN)
Zn(CN) (aq)
(aq)
(1)步骤1中“磨矿”的目的是___________ 。
(2)步骤2中浸出应选用___________ (填盐酸、硫酸或硝酸)。
(3)步骤4浸出的目的是将单质Au转化为Au(CN) 进入溶液,该反应的离子方程式为
进入溶液,该反应的离子方程式为___________ 。
(4)步骤4中为提高金的浸出速率可适当升高温度,但温度过高浸出速率反而会降低,原因是___________ 。
(5)步骤6的目的是___________ 。
(6)步骤7置换的总反应为:2Au(CN) +3Zn+4CN-+2H2O=2Au +2Zn(CN)
+3Zn+4CN-+2H2O=2Au +2Zn(CN) +ZnO
+ZnO +2H2↑,该过程中,为防止生成Zn(CN)2沉淀影响置换速率,可采取的措施是
+2H2↑,该过程中,为防止生成Zn(CN)2沉淀影响置换速率,可采取的措施是___________ 。
(7)脱金贫液(主要含有CN-)会破坏环境,可通过化学方法转化为无毒废水净化排放。碱性条件下,用NaClO将贫液中的CN- 氧化成无毒的CO 和N2,该反应的离子方程式为
和N2,该反应的离子方程式为___________ 。

已知:① Zn +
 O2 + H2O = Zn(OH)2
O2 + H2O = Zn(OH)2②Zn2+(aq)
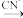 Zn(CN)2(s)
Zn(CN)2(s) 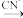 Zn(CN)
Zn(CN) (aq)
(aq)(1)步骤1中“磨矿”的目的是
(2)步骤2中浸出应选用
(3)步骤4浸出的目的是将单质Au转化为Au(CN)
 进入溶液,该反应的离子方程式为
进入溶液,该反应的离子方程式为(4)步骤4中为提高金的浸出速率可适当升高温度,但温度过高浸出速率反而会降低,原因是
(5)步骤6的目的是
(6)步骤7置换的总反应为:2Au(CN)
 +3Zn+4CN-+2H2O=2Au +2Zn(CN)
+3Zn+4CN-+2H2O=2Au +2Zn(CN) +ZnO
+ZnO +2H2↑,该过程中,为防止生成Zn(CN)2沉淀影响置换速率,可采取的措施是
+2H2↑,该过程中,为防止生成Zn(CN)2沉淀影响置换速率,可采取的措施是(7)脱金贫液(主要含有CN-)会破坏环境,可通过化学方法转化为无毒废水净化排放。碱性条件下,用NaClO将贫液中的CN- 氧化成无毒的CO
 和N2,该反应的离子方程式为
和N2,该反应的离子方程式为【知识点】 物质分离、提纯综合应用解读 常见无机物的制备解读
您最近一年使用:0次
2021-05-24更新
|
286次组卷
|
2卷引用:宁夏银川市第六中学2021届高三第五次模拟考试理综化学试卷
解答题-实验探究题
|
适中(0.65)
名校
解题方法
9. 氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。某化学兴趣小组在实验室制取氯水和氯酸钾,并进行相关实验。
Ⅰ.用图所示实验装置制取氯水和氯酸钾
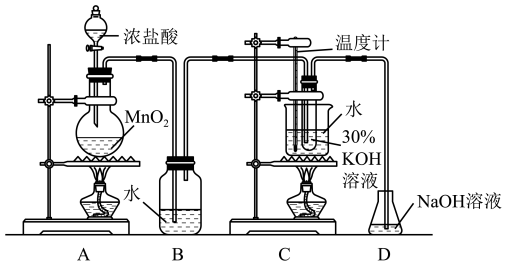
(1)图中标注装有浓盐酸的仪器名称为_______ ,A装置圆底烧瓶中发生反应的化学方程式为_______ 。
(2)在确保KOH溶液完全反应的的条件下,若对调B和C装置的位置,C中氯酸钾的产率会_______ (填“增大”、“减小”或“不变”),原因是 _______ 。
II.测定从装置C试管中分离得到的粗产品中KClO3的质量分数(粗产品中混有的杂质是KClO和KCl);碱性条件下,ClO 氧化性较弱,不能氧化H2O2。测定粗产品中KClO3的纯度的实验过程如下:
氧化性较弱,不能氧化H2O2。测定粗产品中KClO3的纯度的实验过程如下:
步骤 1:取3.00g 样品溶于水配成250mL溶液。
步骤 2:取 25.00mL 溶液于锥形瓶中,加KOH溶液调节pH,然后滴加过量H2O2溶液充分振荡以除尽ClO-。然后煮沸溶液1~2 分钟,冷却。
步骤3:将溶液转移到碘量瓶中(如图),加H2SO4将溶液调至弱酸性,加过量的20%的KI溶液,加盖水封,于暗处放置5min。
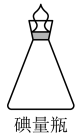
步骤 4:以淀粉为指示剂,用0.1500mol·L-1Na2S2O3标准溶液滴定碘量瓶中的溶液至终点,平行操作三次,平均消耗Na2S2O3溶液20.00mL。相关反应为:
(3)步骤2中,煮沸溶液1~2分钟的目的是_______ 。
(4)步骤3发生反应的离子方程式为:_______ 。
(5)使用碘量瓶时,加盖水封的目的是_______ ,Na2S2O3标准溶液应装入_______ 式滴定管中(填“酸”或“碱”)。
(6)粗产品中KClO3的质量分数为_______ (保留三位有效数字)。
Ⅰ.用图所示实验装置制取氯水和氯酸钾

(1)图中标注装有浓盐酸的仪器名称为
(2)在确保KOH溶液完全反应的的条件下,若对调B和C装置的位置,C中氯酸钾的产率会
II.测定从装置C试管中分离得到的粗产品中KClO3的质量分数(粗产品中混有的杂质是KClO和KCl);碱性条件下,ClO
 氧化性较弱,不能氧化H2O2。测定粗产品中KClO3的纯度的实验过程如下:
氧化性较弱,不能氧化H2O2。测定粗产品中KClO3的纯度的实验过程如下:步骤 1:取3.00g 样品溶于水配成250mL溶液。
步骤 2:取 25.00mL 溶液于锥形瓶中,加KOH溶液调节pH,然后滴加过量H2O2溶液充分振荡以除尽ClO-。然后煮沸溶液1~2 分钟,冷却。
步骤3:将溶液转移到碘量瓶中(如图),加H2SO4将溶液调至弱酸性,加过量的20%的KI溶液,加盖水封,于暗处放置5min。

步骤 4:以淀粉为指示剂,用0.1500mol·L-1Na2S2O3标准溶液滴定碘量瓶中的溶液至终点,平行操作三次,平均消耗Na2S2O3溶液20.00mL。相关反应为:

(3)步骤2中,煮沸溶液1~2分钟的目的是
(4)步骤3发生反应的离子方程式为:
(5)使用碘量瓶时,加盖水封的目的是
(6)粗产品中KClO3的质量分数为
您最近一年使用:0次
2021-04-09更新
|
395次组卷
|
3卷引用:吉林省长春市普通高中2021届高三4月质量监测(三)理综化学试卷题
解答题-原理综合题
|
适中(0.65)
解题方法
10. 碳、氮、硫是重要的非金属元素,在工农业生产中有广泛的应用。
(1)用于发射“天宫一号”的长征二号火箭的燃料是液态偏二甲肼 ,氧化剂是液态N2O4.二者在反应过程中放出大量能量,同时生成无毒、无污染的气体。已知室温下,1g燃料完全燃烧释放出的能量为
,氧化剂是液态N2O4.二者在反应过程中放出大量能量,同时生成无毒、无污染的气体。已知室温下,1g燃料完全燃烧释放出的能量为 ,请写出该反应的热化学方程式
,请写出该反应的热化学方程式___________ 。
(2)298K时,在2L的密闭容器中,发生可逆反应 kJ·mol-1,(a>0) N2O4的物质的量浓度随时间变化如图1,平衡时,
kJ·mol-1,(a>0) N2O4的物质的量浓度随时间变化如图1,平衡时, 的浓度为
的浓度为 的2倍,回答下列问题。
的2倍,回答下列问题。
① 0-20s内用N2O4表示的平均反应速率为___________ 。
②298K时,该反应的平衡常数为___________ (保留两位小数)。
③ 在温度为T1、T2时,平衡体系中 的体积分数随压强变化曲线如图2所示。下列说法正确的是
的体积分数随压强变化曲线如图2所示。下列说法正确的是 ___________ 。

a.A、C两点的反应速率:A>C
b.B、C两点的气体的平均相对分子质量:B﹤C
c.A、C两点气体的颜色:A深,C浅
d.由状态B到状态A,可以用加热的方法
④ 若反应在398K进行,某时刻测得上述容器中
 ,则此时V(正)
,则此时V(正) ___________ V(逆)( 填>、﹤、=)”。
(3) 在分析试剂、医药、电子工业中用途广泛。现向100mL
在分析试剂、医药、电子工业中用途广泛。现向100mL 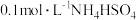 溶液中滴加
溶液中滴加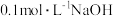 溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图3所示,试分析图中a、b、c、d、e五个点,并填空。
溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图3所示,试分析图中a、b、c、d、e五个点,并填空。
① 水的电离程度最大的是___________ 点 ;
② 其溶液中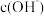 的数值最接近
的数值最接近 的电离常数K数值的是
的电离常数K数值的是 ___________ 点。
(1)用于发射“天宫一号”的长征二号火箭的燃料是液态偏二甲肼
 ,氧化剂是液态N2O4.二者在反应过程中放出大量能量,同时生成无毒、无污染的气体。已知室温下,1g燃料完全燃烧释放出的能量为
,氧化剂是液态N2O4.二者在反应过程中放出大量能量,同时生成无毒、无污染的气体。已知室温下,1g燃料完全燃烧释放出的能量为 ,请写出该反应的热化学方程式
,请写出该反应的热化学方程式(2)298K时,在2L的密闭容器中,发生可逆反应
 kJ·mol-1,(a>0) N2O4的物质的量浓度随时间变化如图1,平衡时,
kJ·mol-1,(a>0) N2O4的物质的量浓度随时间变化如图1,平衡时, 的浓度为
的浓度为 的2倍,回答下列问题。
的2倍,回答下列问题。① 0-20s内用N2O4表示的平均反应速率为
②298K时,该反应的平衡常数为
③ 在温度为T1、T2时,平衡体系中
 的体积分数随压强变化曲线如图2所示。下列说法正确的是
的体积分数随压强变化曲线如图2所示。下列说法正确的是 
a.A、C两点的反应速率:A>C
b.B、C两点的气体的平均相对分子质量:B﹤C
c.A、C两点气体的颜色:A深,C浅
d.由状态B到状态A,可以用加热的方法
④ 若反应在398K进行,某时刻测得上述容器中

 ,则此时V(正)
,则此时V(正) (3)
 在分析试剂、医药、电子工业中用途广泛。现向100mL
在分析试剂、医药、电子工业中用途广泛。现向100mL 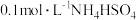 溶液中滴加
溶液中滴加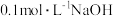 溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图3所示,试分析图中a、b、c、d、e五个点,并填空。
溶液,得到的溶液pH与NaOH溶液体积的关系曲线如图3所示,试分析图中a、b、c、d、e五个点,并填空。① 水的电离程度最大的是
② 其溶液中
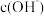 的数值最接近
的数值最接近 的电离常数K数值的是
的电离常数K数值的是
您最近一年使用:0次
解答题-结构与性质
|
适中(0.65)
解题方法
11. A、B、C、D、E代表五种常见元素,它们的核电荷数依次增大。A的基态原子中有2个未成对电子,B的基态原子中共有3对成对电子,C是短周期中最活泼的金属元素。C的液态单质可用作核反应堆的传热介质,D与C可形成CD型离子化合物,元素E的基态3d轨道上未成对电子数是成对电子数的2倍。请回答下列问题:
(1)E的基态原子价层电子排布式为___________ 。
(2)化合物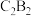 属于
属于___________ 化合物(填“离子”或“共价”),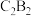 的电子式为
的电子式为___________ 。
(3)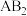 分子中A的杂化类型是
分子中A的杂化类型是___________ ,与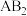 互为等电子体的分子有
互为等电子体的分子有___________ 写一种,下同,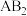 形成的晶体的熔点
形成的晶体的熔点___________ 填(“高于”、“低于”或“无法判断”)CD形成的晶体的熔点,原因是___________ 。
(4)由化合物CD组成的晶体中,阴、阳离子都具有或近似具有球形对称结构,它们都可以看作刚性圆球,并彼此“相切”。如图所示为C、D形成化合物的晶胞结构图以及晶胞的剖面图:

在该晶体中阴离子的配位数为___________ ;若 m,则该晶体的密度为
m,则该晶体的密度为___________ 
(1)E的基态原子价层电子排布式为
(2)化合物
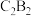 属于
属于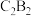 的电子式为
的电子式为(3)
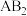 分子中A的杂化类型是
分子中A的杂化类型是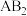 互为等电子体的分子有
互为等电子体的分子有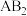 形成的晶体的熔点
形成的晶体的熔点(4)由化合物CD组成的晶体中,阴、阳离子都具有或近似具有球形对称结构,它们都可以看作刚性圆球,并彼此“相切”。如图所示为C、D形成化合物的晶胞结构图以及晶胞的剖面图:

在该晶体中阴离子的配位数为
 m,则该晶体的密度为
m,则该晶体的密度为
您最近一年使用:0次
解答题-有机推断题
|
适中(0.65)
12. 聚戊二酸丙二醇酯(PPG)是一种可降解的聚酯类高分子材料,在材料的生物相容性方面有很好的应用前景。PPG的一种合成路线如图:
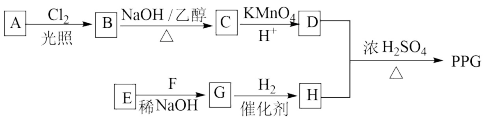
已知:(1)烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢;
(2)化合物B为单氯代烃:化合物C的分子式为C5H8;
(3)E、F为相对分子质量差14的同系物,F是福尔马林的溶质;
(4)R1CHO+R2CH2CHO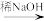
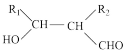
回答下列问题:
(1)A的结构简式为___________ 。
(2)由B生成C的化学方程式为___________ 。
(3)由E和F生成G的反应类型为___________ ,G的化学名称为___________ 。
(4)由D和H生成PPG的化学方程式为___________ 。
(5)D的同分异构体中能同时满足下列条件的共有___________ 种不含立体异构:
①能与饱和NaHCO3溶液反应产生气体
②既能发生银镜反应,又能发生碱性条件下的水解
其中核磁共振氢谱显示为3组峰,且峰面积比为6:1:1的是写结构简式___________ ;D的所有同分异构体在下列一种表征仪器中显示的信号或数据完全相同,该仪器是___________ 。
a.核磁共振仪b.红外光谱仪c.元素分析仪
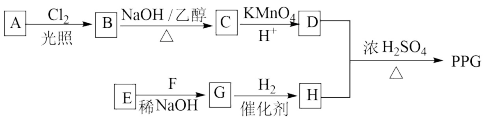
已知:(1)烃A的相对分子质量为70,核磁共振氢谱显示只有一种化学环境的氢;
(2)化合物B为单氯代烃:化合物C的分子式为C5H8;
(3)E、F为相对分子质量差14的同系物,F是福尔马林的溶质;
(4)R1CHO+R2CH2CHO
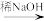
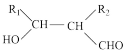
回答下列问题:
(1)A的结构简式为
(2)由B生成C的化学方程式为
(3)由E和F生成G的反应类型为
(4)由D和H生成PPG的化学方程式为
(5)D的同分异构体中能同时满足下列条件的共有
①能与饱和NaHCO3溶液反应产生气体
②既能发生银镜反应,又能发生碱性条件下的水解
其中核磁共振氢谱显示为3组峰,且峰面积比为6:1:1的是写结构简式
a.核磁共振仪b.红外光谱仪c.元素分析仪
您最近一年使用:0次
试卷分析
整体难度:适中
考查范围:认识化学科学、有机化学基础、物质结构与性质、常见无机物及其应用、化学实验基础、化学反应原理
试卷题型(共 12题)
题型
数量
单选题
7
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 氧化还原反应的几组概念 糖类综合 蛋白质组成结构 | |
| 2 | 0.65 | 有机官能团的性质及结构 含有酚羟基的物质性质的推断 多官能团有机物的结构与性质 | |
| 3 | 0.85 | 元素周期律的应用 根据原子结构进行元素种类推断 根据物质性质进行元素种类推断 “位构性”关系理解及应用 | |
| 4 | 0.85 | 氨的碱性 苯酚的弱酸性 蛋白质的盐析 化学实验方案的设计与评价 | |
| 5 | 0.65 | 根据要求书写同分异构体 取代反应 有机分子中原子共面的判断 | |
| 6 | 0.4 | 原电池、电解池综合考查 | |
| 7 | 0.65 | 化学平衡常数的影响因素及应用 化学平衡题中基于图表数据的相关计算 | |
| 二、解答题 | |||
| 8 | 0.65 | 物质分离、提纯综合应用 常见无机物的制备 | 工业流程题 |
| 9 | 0.65 | 氯气的实验室制法 酸碱中和滴定实验相关仪器 酸碱中和滴定原理的应用 物质制备的探究 | 实验探究题 |
| 10 | 0.65 | 热化学方程式书写及正误判断 化学平衡的移动及其影响因素 化学平衡常数的有关计算 水溶液中水的电离程度及的计算 | 原理综合题 |
| 11 | 0.65 | 物质结构与性质综合考查 根据原子结构进行元素种类推断 电子排布式 晶胞的有关计算 | 结构与性质 |
| 12 | 0.65 | 有机反应类型 同分异构体的数目的确定 羧酸酯化反应 有机物的推断 | 有机推断题 |



