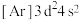下列描述中正确的是
| A.价电子排布为4s24p3的元素位于第四周期第ⅤA族 |
| B.2p和3p轨道形状均为哑铃形,能量也相等 |
| C.所有非金属元素都分布在p区 |
| D.钠原子由1s22s22p63s1→1s22s22p63p1时,原子释放能量,由基态转化成激发态 |
更新时间:2021-05-24 23:45:30
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列叙述中正确的有
①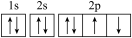 该原子的电子排布图,最外层违背了洪特规则
该原子的电子排布图,最外层违背了洪特规则
②处于最低能量状态原子叫基态原子, 过程中形成的是发射光谱
过程中形成的是发射光谱
③运用价层电子对互斥理论, 离子的空间构型为三角锥型
离子的空间构型为三角锥型
④具有相同核外电子排布的粒子,化学性质相同
⑤NCl3中 N-Cl 键的键长比 CCl4中 C-Cl 键的键长短
①
 该原子的电子排布图,最外层违背了洪特规则
该原子的电子排布图,最外层违背了洪特规则②处于最低能量状态原子叫基态原子,
 过程中形成的是发射光谱
过程中形成的是发射光谱③运用价层电子对互斥理论,
 离子的空间构型为三角锥型
离子的空间构型为三角锥型④具有相同核外电子排布的粒子,化学性质相同
⑤NCl3中 N-Cl 键的键长比 CCl4中 C-Cl 键的键长短
| A.1 个 | B.2 个 | C.3 个 | D.4 个 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】关于原子核外电子排布的说法中正确的是
| A.当K层为最外层时,最多容纳的电子数是8 |
| B.K层距离原子核最近,能量最高 |
| C.当M层为次外层时,最多容纳的电子数是18 |
| D.当N层为最外层时,最多容纳的电子数是32 |
您最近半年使用:0次
【推荐1】新型光催化剂Zn2GeO4具有较高的催化活性。下列有关其组成元素的说法正确的是
| A.Zn处于元素周期表中的d区 |
| B.Ge的价层电子排布式为3d104s24p4 |
| C.基态O原子中成对电子数是未成对电子数的2倍 |
| D.三种元素电负性由大到小的顺序:O>Ge>Zn |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于物质结构的选项中,正确的是
| A.CH3COOH分子中碳原子的杂化类型有sp2和sp3两种 |
| B.元素Ge位于周期表第四周期VIA族,核外电子排布式为[Ar]3d104s24p2,属于p区 |
| C.HF沸点高于HCl,是因为HCl共价键键能小于HF |
| D.可燃冰中甲烷分子与水分子之间存在氢键 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列关于原子结构的说法正确的是
| A.原于光谱上的特征谱线不能用于元素鉴定 |
| B.同一原子中,3s、3p、3d轨道上的电子具有的能量相同 |
| C.日常生活中的焰火、LED灯光都与原子核外电子跃迁释放能量有关 |
D.电于排布式为 的基态原子对应元素位于周期表第五周期 的基态原子对应元素位于周期表第五周期 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列各项叙述中,正确的是
| A.所有原子任一能层的s电子云轮廓图都是球形,但球的半径大小不同 |
| B.镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 |
| C.24Cr原子的电子排布式是1s22s22p63s23p63d44s2 |
| D.价电子排布为5s25p1的元素位于第五周期第ⅠA族,是s区元素 |
您最近半年使用:0次

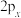 、
、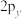 、
、 轨道相互垂直,能量不相等
轨道相互垂直,能量不相等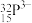 中有15种电子运动状态,占据了9个原子轨道
中有15种电子运动状态,占据了9个原子轨道 键
键