四氧化钌( )是金黄色针状晶体,微溶于水,有强氧化性,能氧化浓盐酸生成
)是金黄色针状晶体,微溶于水,有强氧化性,能氧化浓盐酸生成 和
和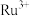 。酸性介质中固体
。酸性介质中固体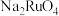 与
与 溶液或
溶液或 溶液反应均可制得
溶液反应均可制得 。下列说法正确的是
。下列说法正确的是
 )是金黄色针状晶体,微溶于水,有强氧化性,能氧化浓盐酸生成
)是金黄色针状晶体,微溶于水,有强氧化性,能氧化浓盐酸生成 和
和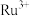 。酸性介质中固体
。酸性介质中固体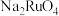 与
与 溶液或
溶液或 溶液反应均可制得
溶液反应均可制得 。下列说法正确的是
。下列说法正确的是A.若 与 与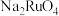 物质的量之比 物质的量之比 ,则还原产物为 ,则还原产物为 |
B. 与浓盐酸反应生成 与浓盐酸反应生成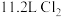 转移电子数为 转移电子数为 |
C.酸性介质中氧化性: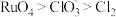 |
D.在稀硫酸环境中,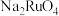 与 与 反应制备 反应制备 的化学方程式为 的化学方程式为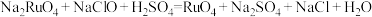 |
更新时间:2021-06-25 08:16:21
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列有关Na2O2的说法不正确的是( )
| A.向包有Na2O2粉末的脱脂棉上滴加几滴水,脱脂棉剧烈燃烧起来,说明Na2O2与H2O反应放热且有氧气生成 |
| B.Na2O2与CO2反应时有单质O2生成,该反应属于置换反应 |
| C.Na2O2在空气中久置变白,涉及的氧化还原反应中,Na2O2既是氧化剂,又是还原剂 |
| D.Na2O2粉末加入Ca(HCO3)2溶液中,会产生气体和浑浊 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.工业制硅时1mol碳高温下与足量的二氧化硅反应转移电子为2mol |
B.工业制硫酸时1mol S与足量的氧气和水反应,理论上可制得1mol  |
C.工业制硝酸时尾气吸收的反应原理为 |
D.汽车尾气处理的化学反应原理 属于置换反应 属于置换反应 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】高铁酸钠(Na2FeO4)是一种绿色净水剂。
①实验室制备原理是 ;
;
②在酸性介质中高铁酸钠不稳定,发生反应: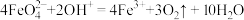 ,在碱性介质中能稳定存在;
,在碱性介质中能稳定存在;
③已知氧化剂的电势是衡量其氧化性强度的主要参数,电势越高,对应条件下氧化剂的氧化性越强,酸性条件下,电势:FeO >Cl2。
>Cl2。
下列叙述错误的是
①实验室制备原理是
 ;
;②在酸性介质中高铁酸钠不稳定,发生反应:
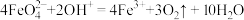 ,在碱性介质中能稳定存在;
,在碱性介质中能稳定存在;③已知氧化剂的电势是衡量其氧化性强度的主要参数,电势越高,对应条件下氧化剂的氧化性越强,酸性条件下,电势:FeO
 >Cl2。
>Cl2。下列叙述错误的是
| A.配制Na2FeO4溶液时添加少量NaOH溶液 |
| B.由反应①知,氧化性:NaClO>Na2FeO4 |
| C.由反应②知,产生11.2LO2时转移2mol电子 |
| D.向Na2FeO4溶液中滴加浓盐酸产生的气体不只一种 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】设NA为阿伏加德罗常数的值,下列说法正确的是
| A.22.4L Cl2和CO的混合气体中含有的原子数为2NA |
| B.1mol O2作氧化剂时转移电子数一定为4NA |
| C.在Na2O2与CO2的反应中,每生成1mol Na2CO3,转移电子数为2NA |
D. 23g Na与O2充分反应生成Na2O和Na2O2的混合物,混合物中阴离子数为0.5NA 23g Na与O2充分反应生成Na2O和Na2O2的混合物,混合物中阴离子数为0.5NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】漂粉精同浓盐酸作用产生氯气:Ca(ClO)2+4HCl(浓)= 2C12↑+CaCl2+2H2O。下列说法错误的是
| A.该反应中HCl作还原剂,Ca(ClO)2作氧化剂 |
| B.每消耗1mol Ca(ClO)2,有4molHCl被氧化 |
| C.已知漂白粉样品mg,反应结束后测得Cl2在标准状况下的体积为VmL,则该漂白粉中有效成分的含量为143v/448m% |
| D.依据该反应产生的氯气中,除含水蒸气外,还含有HCl气体 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】从干海带中提取碘的实验流程如下:
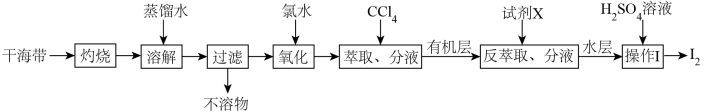
| A.氧化步骤中氯水可用过氧化氢代替 |
B.试剂X可以为 ,反萃取的离子方程式为: ,反萃取的离子方程式为: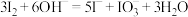 |
C. 可循环利用以有效提高干海带提碘的产率 可循环利用以有效提高干海带提碘的产率 |
| D.操作Ⅰ要用到普通漏斗、烧杯和玻璃棒 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】硫化氢(H2S)是一种有毒、有害的不良气体.处理某废气中的H2S,是将废气与空气混合通入FeCl2、CuCl2、FeCl3的混合液中,其转化的流程如图所示(CuS难溶于水),下列说法正确的是
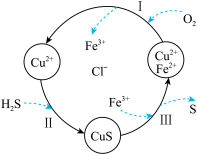

| A.过程I中11.2LO2参加反应转移2mol电子 |
| B.过程II发生复分解反应 |
| C.氧化性由强到弱的顺序:S>Fe3+>O2 |
| D.过程III中发生的离子方程式为S2-+2Fe3+=S↓+2Fe2+ |
您最近半年使用:0次


 是还原产物
是还原产物 +Fe2++H+
+Fe2++H+

