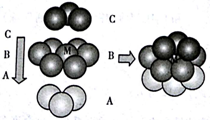
如图所示为金属原子的四种基本堆积(分别为:简单立方堆积、六方最密堆积、面心立方最密堆积、体心立方堆积、)模型,请回答以下问题:
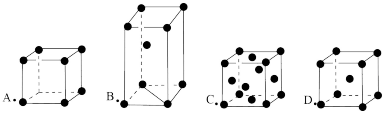
(1)图中原子堆积方式中,空间利用率最低 的是____ (在图中选择,填字母),由非密置层互相错位堆积而成的是_____ 。
(2)金属钛的晶胞为B型,其堆积方式的名称 为_____ 。
(3)某金属R的晶胞为D型,已知R原子半径为rcm,相对原子质量为M,阿佛加得德罗常数为NA,则R金属的密度____ 。(用含r、M、NA字母的式子表示)

(1)图中原子堆积方式中,空间利用率最
(2)金属钛的晶胞为B型,其堆积方式的
(3)某金属R的晶胞为D型,已知R原子半径为rcm,相对原子质量为M,阿佛加得德罗常数为NA,则R金属的密度
更新时间:2021-06-28 18:30:41
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】硼元素、钙元素、铜元素在化学中站有很重要的地位,单质及其化合物在工农业生产和生活中有广泛的应用.
(1)已知CaC2与水反应生成乙炔。请回答下列问题:
①将乙炔通入[Cu(NH3)2]Cl溶液中生成Cu2C2红棕色沉淀,Cu+基态核外电子排布式为______ 。
②CaC2中C22-与O22+互为等电子体,1molO22+中含有的 键数目为
键数目为______ 。
③乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N),丙烯腈分子中碳原子轨道杂化类型是______ ,构成丙烯腈元素中第一电离能最大的是______ 。
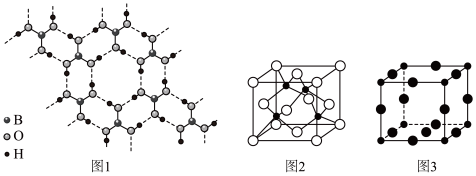
(2)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子间通过氢键相连(如上图1)则1molH3BO3的晶体中有______ mol氢键。硼酸溶于水生成弱电解质一水合硼酸B(OH)3•H2O,它电离生成少量[B(OH)4]-和H+,则[B(OH)4]-的空间构型为______ 。
(3)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如上图2所示(黑点代表铜原子,空心圆代表M原子)。
 该晶体化学式为
该晶体化学式为______ 。
 已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于
已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于______ (填“离子”、“共价”)化合物。
(4)Cu3N的晶胞结构如上图3,N3-的配位数为______ ,Cu+半径为apm,N3-半径为bpm,Cu3N的密度为______ g•cm-3(阿伏加 德罗常数用NA表示)。
(1)已知CaC2与水反应生成乙炔。请回答下列问题:
①将乙炔通入[Cu(NH3)2]Cl溶液中生成Cu2C2红棕色沉淀,Cu+基态核外电子排布式为
②CaC2中C22-与O22+互为等电子体,1molO22+中含有的
 键数目为
键数目为③乙炔与氢氰酸反应可得丙烯腈(H2C=CH-C≡N),丙烯腈分子中碳原子轨道杂化类型是

(2)硼酸(H3BO3)是一种片层状结构的白色晶体,层内的H3BO3分子间通过氢键相连(如上图1)则1molH3BO3的晶体中有
(3)某M原子的外围电子排布式为3s23p5,铜与M形成化合物的晶胞如上图2所示(黑点代表铜原子,空心圆代表M原子)。
 该晶体化学式为
该晶体化学式为 已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于
已知铜和M的电负性分别为1.9和3.0,则铜与M形成的化合物属于(4)Cu3N的晶胞结构如上图3,N3-的配位数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氮元素是重要的非金属元素,可形成卤化氮、氮化物、叠氮化物及配合物等多种化合物。
(1)NF3、NBr3、NCl3的沸点由高到低的顺序是_______ ,原因是_______ 。
(2)Mg3N2遇水发生剧烈反应,生成一种有刺激性气味的气体。该反应的化学方程式为_______ 。
(3)NaN3与KN3相比,NaN3的晶格能_______ (填“>”、“=”或“<”)KN3的晶格能。
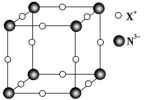
(4)某元素X形成的离子X+中K、L、M三个电子层均充满了电子。它与N3-形成晶体的结构如图所示。X+的符号是_______ ,晶体中距离每个N3-最近的X+有_______ 个。
(1)NF3、NBr3、NCl3的沸点由高到低的顺序是
(2)Mg3N2遇水发生剧烈反应,生成一种有刺激性气味的气体。该反应的化学方程式为
(3)NaN3与KN3相比,NaN3的晶格能
(4)某元素X形成的离子X+中K、L、M三个电子层均充满了电子。它与N3-形成晶体的结构如图所示。X+的符号是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】获得2016-2017年度“影响世界华人大奖”提名的“美女科学家”颜宁教授解析出了人类葡萄糖转运蛋白GLUT家族的结构,为生命科学开启了新的篇章。目前发现的葡萄糖转运蛋白有六种,它们含有C、H、O、N、P、Na、Mg、Fe等元素,请回答下列问题:
(1)下列说法正确的是________ 。
A.葡萄糖转运蛋白中的元素全部是主族元素
B.葡萄糖转运蛋白中的元素分别位于四个不同周期
C.氢化物稳定性CH4>NH3>H2O
D.离子半径大小O2−>Na+>Mg2+
(2)铊能使葡萄糖转运蛋白失去生理活性,铊的相关信息卡片如图所示:

铊在周期表中的位置是________ 。下列推断正确的是________ 。
A.Tl原子的质量数为81 B.Tl在周期表中第13列
C.Tl元素位于金属与非金属分界线旁边 D.氧化性:Tl3+>Al3+
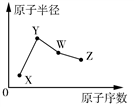
(3)X、Y为葡萄糖转运蛋白中含有的元素,W、Z是短周期元素,其原子半径随原子序数变化如图所示。已知X的一种核素的质量数为18,中子数为10;Y和Ne原子的核外电子总数相差1;W的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最强。
①画出X的阴离子的结构示意图:________ 。
②用电子式表示Z的氢化物的形成过程:________________ 。
③Y的金属性与Mg的金属性相比,________ (写化学式)的金属性强,请用实验证明它们金属性的相对强弱:_______________________________________________ 。
④写出Y的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物发生反应的化学方程式:____________________ 。
⑤工业上经常用W的氧化物制取W单质的粗产品,化学方程式为______________ 。
(1)下列说法正确的是
A.葡萄糖转运蛋白中的元素全部是主族元素
B.葡萄糖转运蛋白中的元素分别位于四个不同周期
C.氢化物稳定性CH4>NH3>H2O
D.离子半径大小O2−>Na+>Mg2+
(2)铊能使葡萄糖转运蛋白失去生理活性,铊的相关信息卡片如图所示:

铊在周期表中的位置是
A.Tl原子的质量数为81 B.Tl在周期表中第13列
C.Tl元素位于金属与非金属分界线旁边 D.氧化性:Tl3+>Al3+
(3)X、Y为葡萄糖转运蛋白中含有的元素,W、Z是短周期元素,其原子半径随原子序数变化如图所示。已知X的一种核素的质量数为18,中子数为10;Y和Ne原子的核外电子总数相差1;W的单质是一种常见的半导体材料;Z的非金属性在同周期主族元素中最强。

①画出X的阴离子的结构示意图:
②用电子式表示Z的氢化物的形成过程:
③Y的金属性与Mg的金属性相比,
④写出Y的最高价氧化物对应的水化物与Z的最高价氧化物对应的水化物发生反应的化学方程式:
⑤工业上经常用W的氧化物制取W单质的粗产品,化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】硼原子有3个价电子,但有4个价轨道,这种价电子数少于价轨道数的原子称作缺电子原子。因此,硼的一些化合物表现出缺电子特征。回答下列问题:
(1)硼酸分子结构简式可写为 ,其晶体为层型片状结构,容易在层与层之间裂解,这是因为在平面层内硼酸分子之间通过
,其晶体为层型片状结构,容易在层与层之间裂解,这是因为在平面层内硼酸分子之间通过_______ 结合,而层与层之间通过_______ 结合。
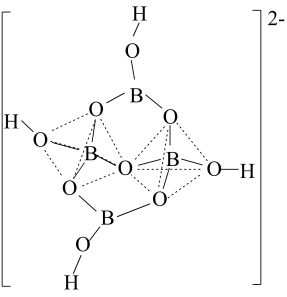
(2)硼砂是硼含氧酸的重要钠盐,其阴离子的结构如图所示,其中B原子的杂化方式为_______ 。硼砂晶体中结晶水与硼的物质的量比为 ,硼砂的化学式为
,硼砂的化学式为_______ 。
(1)硼酸分子结构简式可写为
 ,其晶体为层型片状结构,容易在层与层之间裂解,这是因为在平面层内硼酸分子之间通过
,其晶体为层型片状结构,容易在层与层之间裂解,这是因为在平面层内硼酸分子之间通过(2)硼砂是硼含氧酸的重要钠盐,其阴离子的结构如图所示,其中B原子的杂化方式为
 ,硼砂的化学式为
,硼砂的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某晶体的粒子结构如图所示:
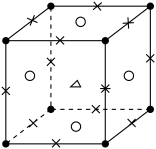
正六面体的8个顶点为A粒子,12个棱心为B粒子,6个面心为C粒子,正六面体的中心为D粒子。那么:
(1)晶体中A、B、C、D4种粒子的个数比为_______ ;
(2)此晶体中每个A粒子周围与它最接近且距离相等的A粒子有_______。

正六面体的8个顶点为A粒子,12个棱心为B粒子,6个面心为C粒子,正六面体的中心为D粒子。那么:
(1)晶体中A、B、C、D4种粒子的个数比为
(2)此晶体中每个A粒子周围与它最接近且距离相等的A粒子有_______。
| A.4个 | B.6个 | C.8个 | D.12个 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】高温超导材料是科学家研究的重点物质之一。
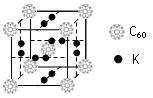
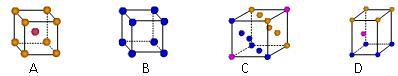
⑴科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如下左图所示。该富勒烯化合物中的K原子和C60分子的个数比为________ 。
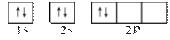
⑵某同学画出的C的核外电子排布(轨道表示式)如上右图所示,该电子排布图(轨道表示式)违背了________ ,请你画出正确的电子排布图(轨道表示式)_______ 。
⑶金属钾采用的是下列_________ (填字母代号)堆积方式。
⑷富勒烯(C60)的结构如图。
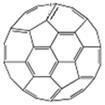
①1 mol C60分子中σ键的数目为__________ 。
②已知:金刚石中的C-C的键长为154.45 pm,C60中C-C键长为145~140 pm。有同学据此推断C60的熔点高于金刚石,你认为是否正确并阐述理由:_________ 。
⑴科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如下左图所示。该富勒烯化合物中的K原子和C60分子的个数比为

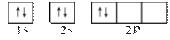
⑵某同学画出的C的核外电子排布(轨道表示式)如上右图所示,该电子排布图(轨道表示式)违背了
⑶金属钾采用的是下列

⑷富勒烯(C60)的结构如图。

①1 mol C60分子中σ键的数目为
②已知:金刚石中的C-C的键长为154.45 pm,C60中C-C键长为145~140 pm。有同学据此推断C60的熔点高于金刚石,你认为是否正确并阐述理由:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】理论计算预测,由汞(Hg)、锗(Ge)、锑(Sb)形成的一种新物质X为潜在的拓扑绝缘体材料。X的晶体可视为Ge晶体(晶胞如图a所示)中部分Ge原子被Hg和Sb取代后形成。
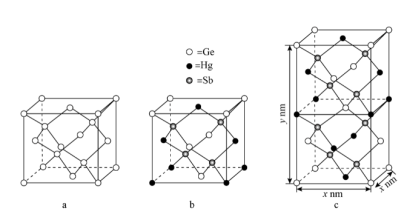
图c为X的晶胞,设X的最简式的式量为Mr,则X晶体的密度为_______ g/cm3(列出算式)。

图c为X的晶胞,设X的最简式的式量为Mr,则X晶体的密度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)A元素基态的正一价离子的3d轨道为半充满,其元素符号为_______ ,该离子占据的最高能层的符号是_______ 。
(2)利用现代仪器与方法可以测定物质的结构,其中,利用_______ 法可测定分子的相对分子质量。利用_______ 法可区分晶体与非晶体。
(3)如图的NaCl晶胞中,每个 周围与之等距离且最近的
周围与之等距离且最近的 有
有_______ 个, 的配位数为
的配位数为_______ 。
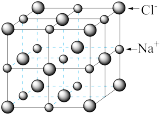
(4) 能与水混溶,却不溶于
能与水混溶,却不溶于 ,原因是
,原因是_______ 。
(5)Mn与Fe两元素的部分电离能数据如下表所示,比较两元素的 和
和 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子更难,原因是
再失去一个电子更难,原因是_______ 。
(1)A元素基态的正一价离子的3d轨道为半充满,其元素符号为
(2)利用现代仪器与方法可以测定物质的结构,其中,利用
(3)如图的NaCl晶胞中,每个
 周围与之等距离且最近的
周围与之等距离且最近的 有
有 的配位数为
的配位数为
(4)
 能与水混溶,却不溶于
能与水混溶,却不溶于 ,原因是
,原因是(5)Mn与Fe两元素的部分电离能数据如下表所示,比较两元素的
 和
和 可知,气态
可知,气态 再失去一个电子比气态
再失去一个电子比气态 再失去一个电子更难,原因是
再失去一个电子更难,原因是| 元素 | Mn | Fe | |
电离能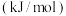 |  | 717 | 759 |
 | 1509 | 1561 | |
 | 3248 | 2957 | |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】用元素周期表中的部分元素及其化合物回答下列问题。
(1)C的基态原子的电子排布式_______ ; 在周期表中的位置是
在周期表中的位置是_______ 区。
(2)C、N、O原子电负性由大到小顺序为_______ ,阴离子 的空间构型为
的空间构型为_______ 。
(3) 分子中各原子都满足最外层8电子结构,分子中
分子中各原子都满足最外层8电子结构,分子中 键与
键与 键数目之比为
键数目之比为_______ , 分子为
分子为_______ 。(填“极性分子”或“非极佳分子”)
(4)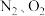 单质都能与
单质都能与 反应且反应能力增强,其原因是
反应且反应能力增强,其原因是_______ 。
(5)已知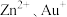 均能与
均能与 形成配离子,配位数分别为4和2,工业上常用
形成配离子,配位数分别为4和2,工业上常用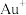 和
和 形成的配离子与
形成的配离子与 加发生置换反应来提取
加发生置换反应来提取 ,写出上述反应的离子方程式:
,写出上述反应的离子方程式:_______ 。
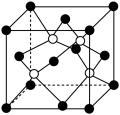
(6)阿拉班达石(alabandite)是一种属于立方晶系的硫锰矿,其晶胞如图所示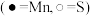 。已知该晶胞参数为
。已知该晶胞参数为 ,晶体密度为
,晶体密度为 ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值
_______ 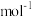 。
。
(1)C的基态原子的电子排布式
 在周期表中的位置是
在周期表中的位置是(2)C、N、O原子电负性由大到小顺序为
 的空间构型为
的空间构型为(3)
 分子中各原子都满足最外层8电子结构,分子中
分子中各原子都满足最外层8电子结构,分子中 键与
键与 键数目之比为
键数目之比为 分子为
分子为(4)
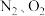 单质都能与
单质都能与 反应且反应能力增强,其原因是
反应且反应能力增强,其原因是(5)已知
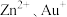 均能与
均能与 形成配离子,配位数分别为4和2,工业上常用
形成配离子,配位数分别为4和2,工业上常用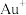 和
和 形成的配离子与
形成的配离子与 加发生置换反应来提取
加发生置换反应来提取 ,写出上述反应的离子方程式:
,写出上述反应的离子方程式:(6)阿拉班达石(alabandite)是一种属于立方晶系的硫锰矿,其晶胞如图所示
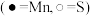 。已知该晶胞参数为
。已知该晶胞参数为 ,晶体密度为
,晶体密度为 ,则阿伏加德罗常数的值
,则阿伏加德罗常数的值
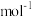 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
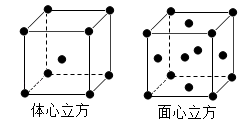
【推荐1】(1)金属铁的晶体在不同温度下有两种堆积方式,晶胞如图所示。面心立方晶胞和体心立方晶胞中实际含有的Fe原子个数之比为_____ 。
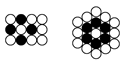
(2)等径圆球在二维空间里进行排列,可形成密置层和非密置层,在下图所示的半径相等的圆球的排列中,A属于_____ 层,配位数是_____ ,将其在三维空间中按照圆球正对圆球的方式堆积,得到_____ 堆积,其空间利用率最小,为_____ (结果取三位有效数字)。
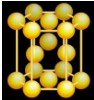
(3)将B层一层一层地在三维空间里堆积,可以得到六方最密堆积,晶体如图.在这种晶体中金属原子的配位数是_____ ,平均每个晶胞所占有的原子数目是_____ 。
(4)Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为____________ 。列式表示Al单质的密度___________________ g·cm-3(不必计算出结果)。

(2)等径圆球在二维空间里进行排列,可形成密置层和非密置层,在下图所示的半径相等的圆球的排列中,A属于

(3)将B层一层一层地在三维空间里堆积,可以得到六方最密堆积,晶体如图.在这种晶体中金属原子的配位数是

(4)Al单质为面心立方晶体,其晶胞参数a=0.405nm,晶胞中铝原子的配位数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】铜及其合金是人类最早使用的金属材料,铜的化合物在现代生活和生产中有着广泛的应用。
(1)铜的熔点比钙的高,其原因是____________________ 。
(2)金属铜的堆积方式为如图中的_____________ (填字母序号)。
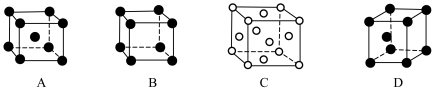
(3)某磷青铜晶胞结构如图所示。
①则其化学式为_____________ 。
②该晶体中距离Cu原子最近的Sn原子有_____ 个,这些Sn原子所呈现的构型为____
(4)磷化铜与水作用产生有毒的磷化氢(PH3)。P与N同主族,其最高价氧化物对应水化物的酸性:HNO3________ H3PO4(填“>”或“<”),从结构的角度说明理由:_________________ 。
(1)铜的熔点比钙的高,其原因是
(2)金属铜的堆积方式为如图中的

(3)某磷青铜晶胞结构如图所示。

①则其化学式为
②该晶体中距离Cu原子最近的Sn原子有
(4)磷化铜与水作用产生有毒的磷化氢(PH3)。P与N同主族,其最高价氧化物对应水化物的酸性:HNO3
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】元素周期表中第ⅦA族包括氟、氯、溴、碘、砹五种元素,统称为卤素。其中代表元素氯富集在海水中,其单质及其化合物在生活、生产中有着广泛地应用。回答下列问题:
(1)基态氯原子能量最高能层上的原子轨道数为______ ;现代化学中,常用光谱分析来鉴定元素,这与原子的___________ 有关。
(2)物质的熔点与其结构密切相关。某同学判断某些卤化物的熔点为NaF>NaCl,SiF4<SiCl4。该同学的主要判断依据是___________ 。
(3)在氢卤酸中,HF是唯一的弱酸,主要原因是__________ 。
(4)光气(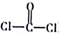 )用作有机合成、农药、药物、染料及其他化工制品的中间体。从电子云的重叠角度分析,该分子中含有的共价键类型是
)用作有机合成、农药、药物、染料及其他化工制品的中间体。从电子云的重叠角度分析,该分子中含有的共价键类型是_______ ,C原子的杂化方式为____ ,分子的空间构型为______ 。
(5)PtCl2(NH3)2为平面结构,可以形成甲、乙两种固体。其中,一种为淡黄色固体,在水中溶解度小;另一种为棕黄色固体,在水中溶解度大,是癌症治疗的常用化学药物。
① 棕黄色固体是图中的___ (填“甲”或“乙”),试解释它在水中的溶解度比淡黄色固体大的原因是___ 。
② Pt原子在三维空间里可按图 所示方式堆积形成金属Pt晶体:
该晶胞的堆积方式为____ ,M 原子的配位数为________ ,若该晶体的密度为ρg·cm3,阿伏伽德罗常数的值为NA,则Pt原子的原子半径为______ pm。
(1)基态氯原子能量最高能层上的原子轨道数为
(2)物质的熔点与其结构密切相关。某同学判断某些卤化物的熔点为NaF>NaCl,SiF4<SiCl4。该同学的主要判断依据是
(3)在氢卤酸中,HF是唯一的弱酸,主要原因是
(4)光气(
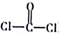 )用作有机合成、农药、药物、染料及其他化工制品的中间体。从电子云的重叠角度分析,该分子中含有的共价键类型是
)用作有机合成、农药、药物、染料及其他化工制品的中间体。从电子云的重叠角度分析,该分子中含有的共价键类型是(5)PtCl2(NH3)2为平面结构,可以形成甲、乙两种固体。其中,一种为淡黄色固体,在水中溶解度小;另一种为棕黄色固体,在水中溶解度大,是癌症治疗的常用化学药物。
① 棕黄色固体是图中的

② Pt原子在三维空间里可按图 所示方式堆积形成金属Pt晶体:
该晶胞的堆积方式为
您最近一年使用:0次



