(1)已知0.5mol的液态甲醇(CH3OH)在空气中完全燃烧生成CO2气体和液态水时放出350kJ的热量,则表示甲醇燃烧热的热化学方程式为___________ 。
(2)已知:①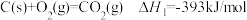
②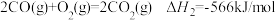
③
则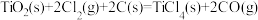 的
的
___________ 。
(3)燃料电池是一种具有应用前景的绿色电源。下图为燃料电池的结构示意图,电解质溶液为NaOH溶液,电极材料为疏松多孔的石墨棒。请回答下列问题:
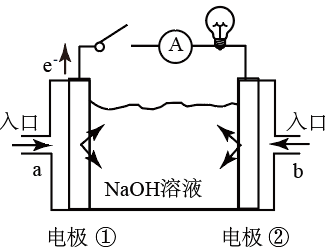
若该燃料电池为氢氧燃料电池。
①a极通入的物质为___________ (填物质名称),电解质溶液中的 移向
移向___________ 极(填“负”或“正”)。
②写出此氢氧燃料电池工作时,负极的电极反应式:___________ 。
若该燃料电池为甲烷燃料电池。已知电池的总反应为:
③下列有关说法正确的是___________ (填字母代号)。
A.燃料电池将电能转变为化学能
B.负极的电极反应式为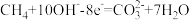
C.正极的电极反应式为
D.通入甲烷的电极发生还原反应
(2)已知:①
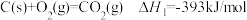
②
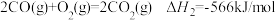
③

则
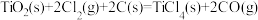 的
的
(3)燃料电池是一种具有应用前景的绿色电源。下图为燃料电池的结构示意图,电解质溶液为NaOH溶液,电极材料为疏松多孔的石墨棒。请回答下列问题:

若该燃料电池为氢氧燃料电池。
①a极通入的物质为
 移向
移向②写出此氢氧燃料电池工作时,负极的电极反应式:
若该燃料电池为甲烷燃料电池。已知电池的总反应为:

③下列有关说法正确的是
A.燃料电池将电能转变为化学能
B.负极的电极反应式为
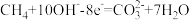
C.正极的电极反应式为

D.通入甲烷的电极发生还原反应
更新时间:2021-06-30 10:15:52
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】甲醇是一种重要的化工原料,又是一种可再生能源,具有开发和应用的广阔前景。
(1)已知:CH3OH(g)=HCHO(g)+H2(g) ΔH=+84kJ⋅mol−1,
2H2(g)+O2(g)═2H2O(g)ΔH=−484kJ⋅mol−1
工业上常以甲醇为原料制取甲醛,请写出CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式:____________________
(2)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应CO(g)+2H2(g)⇌CH3OH(g)。 CO的平衡转化率与温度,压强的关系如图所示。
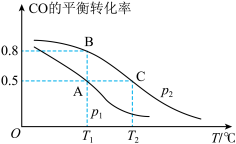
①A,B两点对应的压强大小关系是PA________ PB(填“>,<,=”)
②下列叙述能说明上述反应能达到化学平衡状态的是___________ (填代号)
a.H2的消耗速率是CH3OH生成速率的2倍 b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变 d.气体的平均相对分子质量和压强不再改变
③在P1压强、T1°C时,该反应的平衡常数K=_________ (填计算结果)
④T1°C、1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下:CO:0.1mol, H2:0.2mol, CH3OH:0.2mol。此时v正________ v逆(填> 、 < 或 =)。
(1)已知:CH3OH(g)=HCHO(g)+H2(g) ΔH=+84kJ⋅mol−1,
2H2(g)+O2(g)═2H2O(g)ΔH=−484kJ⋅mol−1
工业上常以甲醇为原料制取甲醛,请写出CH3OH(g)与O2(g)反应生成HCHO(g)和H2O(g)的热化学方程式:
(2)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应CO(g)+2H2(g)⇌CH3OH(g)。 CO的平衡转化率与温度,压强的关系如图所示。

①A,B两点对应的压强大小关系是PA
②下列叙述能说明上述反应能达到化学平衡状态的是
a.H2的消耗速率是CH3OH生成速率的2倍 b.CH3OH的体积分数不再改变
c.混合气体的密度不再改变 d.气体的平均相对分子质量和压强不再改变
③在P1压强、T1°C时,该反应的平衡常数K=
④T1°C、1L的密闭容器内发生上述反应,测得某时刻各物质的物质的量如下:CO:0.1mol, H2:0.2mol, CH3OH:0.2mol。此时v正
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】在恒压下化学反应所吸收或放出的热量,称为化学反应的焓变。回答下列问题:
(1)25℃、101kPa时,1g氨气完全燃烧放出18.6kJ的热量,则4NH3(g)+3O2(g)=2N2(g)+6H2O(l) △H=____ kJ•mol-1。
(2)常压下,某铝热反应的温度与能量变化如图所示:

①常压、1538℃时,Fe(s)→Fe(l)△H=_____ kJ•mol-1。
②常压、25℃时,该铝热反应的热化学方程式为_____ 。
(3)I-催化H2O2分解的原理分为两步,总反应可表示为:2H2O2(aq)=2H2O(l)+O2(g) △H<0
若第一步反应的热化学方程式为:H2O2(aq)+I-(aq)=IO-(aq)+H2O(l) △H>0 慢反应
①则第二步反应的热化学方程式为:_____ △H<0 快反应
②能正确表示I-催化H2O2分解原理的示意图为____ 。
A.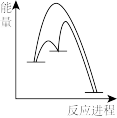 B.
B.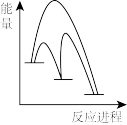 C.
C.  D.
D.
(1)25℃、101kPa时,1g氨气完全燃烧放出18.6kJ的热量,则4NH3(g)+3O2(g)=2N2(g)+6H2O(l) △H=
(2)常压下,某铝热反应的温度与能量变化如图所示:

①常压、1538℃时,Fe(s)→Fe(l)△H=
②常压、25℃时,该铝热反应的热化学方程式为
(3)I-催化H2O2分解的原理分为两步,总反应可表示为:2H2O2(aq)=2H2O(l)+O2(g) △H<0
若第一步反应的热化学方程式为:H2O2(aq)+I-(aq)=IO-(aq)+H2O(l) △H>0 慢反应
①则第二步反应的热化学方程式为:
②能正确表示I-催化H2O2分解原理的示意图为
A.
 B.
B. C.
C.  D.
D.
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,其中B是地壳中含量最多的元素。已知A、C及B、E分别是同主族元素,且B、E两元素原子核内质子数之和是A、C两元素原子核内质子数之和的2倍。处于同周期的C、D、E元素中,D是该周期金属元素中金属性最弱的元素。
(1)试比较C、D两元素最高价氧化物对应水化物碱性的强弱(填化学式)______ 。
(2)A、B、C形成的化合物的晶体类型为______ ,电子式为______ 。
(3)写出D单质与C元素最高价氧化物对应水化物反应的离子方程式______ 。
(4)写出两种均含A、B、C、E四种元素的化合物在溶液中相互反应、且生成气体的离子方程式______ 。
(5)通常条件下,C的最高价氧化物对应水化物2mol与E最高价氧化物对应水化物1mol的稀溶液间反应放出的热量为114.6kJ,试写出表示该热量变化的热化学方程式______ 。
(6)含有元素C的盐的焰色反应为______ 色。许多金属盐都可以发生焰色反应,其原因是______ 。
(1)试比较C、D两元素最高价氧化物对应水化物碱性的强弱(填化学式)
(2)A、B、C形成的化合物的晶体类型为
(3)写出D单质与C元素最高价氧化物对应水化物反应的离子方程式
(4)写出两种均含A、B、C、E四种元素的化合物在溶液中相互反应、且生成气体的离子方程式
(5)通常条件下,C的最高价氧化物对应水化物2mol与E最高价氧化物对应水化物1mol的稀溶液间反应放出的热量为114.6kJ,试写出表示该热量变化的热化学方程式
(6)含有元素C的盐的焰色反应为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。
反应A:4HCl+O2 2Cl2+2H2O
2Cl2+2H2O
已知:i.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。___________ 。
(2)反应A的热化学方程式是___________ (注意:不写条件)。
(3)断开1 mol H-O键与断开1 mol H-Cl键所需能量相差为___________ kJ,H2O中H-O键比HCl中H-Cl键(填“强”或“弱”)___________ 。
(4)请回答:
H2(g)+Br2(l)=2HBr(g) ΔH=-72 kJ·mol-1,蒸发1mol Br2(1)需要吸收的能量为30kJ,则上表中a的数值为:___________ 。
(5)已知甲烷的燃烧热为890.3kJ·mol-1,H2O(g)=H2O(l) ΔH=-44.0kJ·mol-1,N2(g)+O2(g)=2NO(g) ΔH=+180.5kJ·mol-1,则甲烷脱硝反应:CH4(g)+2NO(g)+O2(g)=CO2(g)+N2(g)+2H2O(g) ΔH=___________ 。
(6)二氧化碳经催化氢化可转化成绿色能源乙醇(CH3CH2OH)。已知:
①2H2(g)+O2(g)=2H2O(g) = -483.6 kJ·mol-1
= -483.6 kJ·mol-1
②CH3CH2OH(l)+3O2(g)=2CO2(g)+3H2O(l) =-1366.8kJ·mol-1
=-1366.8kJ·mol-1
③H2O(l)=H2O(g) =+44.0kJ·mol-1
=+44.0kJ·mol-1
则二氧化碳与氢气转化成CH3CH2OH(l)和液态水的热化学方程式为:___________ 。
反应A:4HCl+O2
 2Cl2+2H2O
2Cl2+2H2O已知:i.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ii.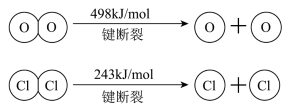
(2)反应A的热化学方程式是
(3)断开1 mol H-O键与断开1 mol H-Cl键所需能量相差为
(4)请回答:
| 参加反应的物质及状态 |  |  | 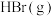 |
| 1mol分子中的化学键断裂时需要吸收的能量 | 436 | a | 369 |
(5)已知甲烷的燃烧热为890.3kJ·mol-1,H2O(g)=H2O(l) ΔH=-44.0kJ·mol-1,N2(g)+O2(g)=2NO(g) ΔH=+180.5kJ·mol-1,则甲烷脱硝反应:CH4(g)+2NO(g)+O2(g)=CO2(g)+N2(g)+2H2O(g) ΔH=
(6)二氧化碳经催化氢化可转化成绿色能源乙醇(CH3CH2OH)。已知:
①2H2(g)+O2(g)=2H2O(g)
 = -483.6 kJ·mol-1
= -483.6 kJ·mol-1②CH3CH2OH(l)+3O2(g)=2CO2(g)+3H2O(l)
 =-1366.8kJ·mol-1
=-1366.8kJ·mol-1③H2O(l)=H2O(g)
 =+44.0kJ·mol-1
=+44.0kJ·mol-1则二氧化碳与氢气转化成CH3CH2OH(l)和液态水的热化学方程式为:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】 是导致温室效应的主要气体,为减少
是导致温室效应的主要气体,为减少 对环境造成的影响,可采用以下方法将其资源化利用。回答下列问题:
对环境造成的影响,可采用以下方法将其资源化利用。回答下列问题:
(1)工业上用 与
与 反应合成甲醇(a和b均大于零):
反应合成甲醇(a和b均大于零):
①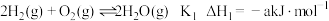 ;
;
②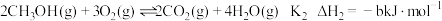 ;
;
③ 。
。
则
_______ (用含 的代数式表示),
的代数式表示),
_______  (用含a、b的代数式表示)。
(用含a、b的代数式表示)。
(2) 催化加氢合成乙烯:
催化加氢合成乙烯:
往某恒容密闭容器中,充入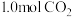 和
和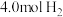 ,发生反应:
,发生反应: ,当反应达到平衡时,测得
,当反应达到平衡时,测得 的物质的量分数随温度的变化曲线如图所示:
的物质的量分数随温度的变化曲线如图所示:

①对于 ,下列说法正确的是
,下列说法正确的是_______ (填标号)。
A.该反应中反应物的总键能小于生成物的总键能
B.升高温度,该反应的 的值增大
的值增大
C.加入合适的催化剂,有利于提高 的转化率
的转化率
D.当混合气体的相对分子质量不再随时间而改变,则该反应达到平衡
②若反应达到平衡时,a点时容器内气体的总压强为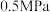 ,则该反应的平衡常数
,则该反应的平衡常数
_______  (列出计算式即可,用分压表示,分压=总压×物质的量分数)。
(列出计算式即可,用分压表示,分压=总压×物质的量分数)。
(3)草酸锌可应用于有机合成、电子工业等。工业上制取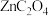 的原理如图所示(电解液不参加反应):
的原理如图所示(电解液不参加反应):
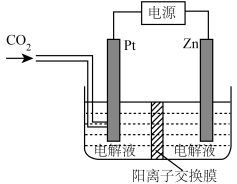
①该电池属于_______ (填“电解池”或“原电池”)。
②Pt电极上的电极反应式为_______ 。
③每转移0.2mol电子,此时消耗 的体积为
的体积为_______ L(标准状况下)。
(4) 用途广泛,写出基于其物理性质的一种用途:
用途广泛,写出基于其物理性质的一种用途:_______ 。
 是导致温室效应的主要气体,为减少
是导致温室效应的主要气体,为减少 对环境造成的影响,可采用以下方法将其资源化利用。回答下列问题:
对环境造成的影响,可采用以下方法将其资源化利用。回答下列问题:(1)工业上用
 与
与 反应合成甲醇(a和b均大于零):
反应合成甲醇(a和b均大于零):①
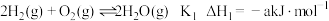 ;
;②
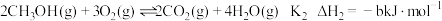 ;
;③
 。
。则

 的代数式表示),
的代数式表示),
 (用含a、b的代数式表示)。
(用含a、b的代数式表示)。(2)
 催化加氢合成乙烯:
催化加氢合成乙烯:往某恒容密闭容器中,充入
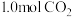 和
和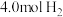 ,发生反应:
,发生反应: ,当反应达到平衡时,测得
,当反应达到平衡时,测得 的物质的量分数随温度的变化曲线如图所示:
的物质的量分数随温度的变化曲线如图所示:
①对于
 ,下列说法正确的是
,下列说法正确的是A.该反应中反应物的总键能小于生成物的总键能
B.升高温度,该反应的
 的值增大
的值增大C.加入合适的催化剂,有利于提高
 的转化率
的转化率D.当混合气体的相对分子质量不再随时间而改变,则该反应达到平衡
②若反应达到平衡时,a点时容器内气体的总压强为
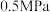 ,则该反应的平衡常数
,则该反应的平衡常数
 (列出计算式即可,用分压表示,分压=总压×物质的量分数)。
(列出计算式即可,用分压表示,分压=总压×物质的量分数)。(3)草酸锌可应用于有机合成、电子工业等。工业上制取
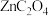 的原理如图所示(电解液不参加反应):
的原理如图所示(电解液不参加反应):
①该电池属于
②Pt电极上的电极反应式为
③每转移0.2mol电子,此时消耗
 的体积为
的体积为(4)
 用途广泛,写出基于其物理性质的一种用途:
用途广泛,写出基于其物理性质的一种用途:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】基于新材料及3D打印技术,科学家研制出一种微胶囊吸收剂能将工厂排放的CO2以更加安全、廉价和高效的方式处理掉,球形微胶囊内部充入Na2CO3溶液,其原理如图所示。

(1)这种微胶囊吸收CO2的原理是___________ (写离子方程式),此过程是___________ (填“吸收”或“放出”)能量的过程。
(2)在吸收过程中关于胶囊内溶液下列说法正确的是___________。
(3)已知NaHCO3溶液显碱性,结合化学用语解释原因___________ 。
(4)将解吸后的CO2催化加氢可制取乙烯。
已知:C2H4(g)+3O2(g)=2CO2(g)+2H2O(g) ΔH=-1323 kJ/mol
2H2(g)+O2(g)=2H2O(g) ΔH=-484 kJ/mol
写出CO2催化加氢制取乙烯的热化学方程式___________ 。
(5)如图曲线a表示在体积为2L的恒容容器中制取乙烯,投料为1 mol CO2和3 mol H2时,测得温度对CO2的平衡转化率的影响,改变投料比测量后得到曲线b。
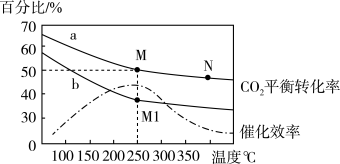
①b条件下投料比
___________ 3(填“>”、“<”或“=”),判断依据是___________ 。
②工业生产中采取较高温度(250℃左右),原因是___________ 。

(1)这种微胶囊吸收CO2的原理是
(2)在吸收过程中关于胶囊内溶液下列说法正确的是___________。
A.吸收前溶液中c(Na+)>c(CO )>c(HCO )>c(HCO )>c(OH-)>c(H+) )>c(OH-)>c(H+) |
B.吸收过程中,体系中的含碳微粒有CO 、HCO 、HCO 、H2CO3、CO2 、H2CO3、CO2 |
C.当n(CO2)∶n(Na2CO3)=1∶3时,溶液中c(CO )<c(HCO )<c(HCO ) ) |
D.溶液中始终有c(Na+)+c(H+)=2c(CO )+c(HCO )+c(HCO )+c(OH-) )+c(OH-) |
(4)将解吸后的CO2催化加氢可制取乙烯。
已知:C2H4(g)+3O2(g)=2CO2(g)+2H2O(g) ΔH=-1323 kJ/mol
2H2(g)+O2(g)=2H2O(g) ΔH=-484 kJ/mol
写出CO2催化加氢制取乙烯的热化学方程式
(5)如图曲线a表示在体积为2L的恒容容器中制取乙烯,投料为1 mol CO2和3 mol H2时,测得温度对CO2的平衡转化率的影响,改变投料比测量后得到曲线b。

①b条件下投料比

②工业生产中采取较高温度(250℃左右),原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】电化学是当今化学研究的热点之一,回答下列问题:
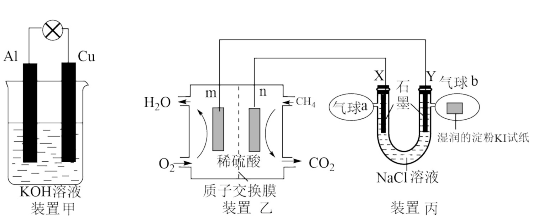
(1)碱性电池具有耐用、电流量大,储存寿命长、外壳不易腐蚀等优点。铝-铜碱性原电池的工作原理如装置甲所示:
①在_______ (“ ”或“
”或“ ”)极有
”)极有 生成,
生成, 极电极反应式为
极电极反应式为_______
②若有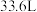 (标准状况下)
(标准状况下) 生成,则理论上电解质溶液增重
生成,则理论上电解质溶液增重_______ g。
(2)某兴趣小组设计以甲烷、氧气酸性燃料电池为电源电解 溶液,并验证氯气的某种化学性质,工作原理如装置乙、装置丙所示。
溶液,并验证氯气的某种化学性质,工作原理如装置乙、装置丙所示。
①m极为_______ 极,装置乙发生反应的化学方程式为_______
②Y极电极反应式为_______
③气球b中的现象为_______ ,证明了氯气的化学性质之一:_______ 性。
(1)碱性电池具有耐用、电流量大,储存寿命长、外壳不易腐蚀等优点。铝-铜碱性原电池的工作原理如装置甲所示:

①在
 ”或“
”或“ ”)极有
”)极有 生成,
生成, 极电极反应式为
极电极反应式为②若有
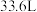 (标准状况下)
(标准状况下) 生成,则理论上电解质溶液增重
生成,则理论上电解质溶液增重(2)某兴趣小组设计以甲烷、氧气酸性燃料电池为电源电解
 溶液,并验证氯气的某种化学性质,工作原理如装置乙、装置丙所示。
溶液,并验证氯气的某种化学性质,工作原理如装置乙、装置丙所示。①m极为
②Y极电极反应式为
③气球b中的现象为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】低碳环保,减轻大气污染,必须从源头上对尾气进行净化处理。回答下列问题
(1)汽车尾气催化转换器中的反应为2NO(g)+2CO(g) 2CO2(g)+N2(g)。若在密闭容器中发生该反应时,c(N2)随温度(T)和时间(t)的变化曲线如图所示。
2CO2(g)+N2(g)。若在密闭容器中发生该反应时,c(N2)随温度(T)和时间(t)的变化曲线如图所示。
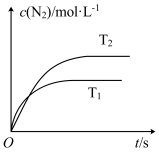
①由图甲可知,温度T1_____ T2(填“>”或“<”,下同);该反应的△H_____ 0。
②能提高尾气转化率的措施有_____ (填字母)。
a.升高温度 b.降低温度 c.增大压强 d.增大催化剂的比表面积
(2)煤燃烧产生的烟气中含有氮氧化物,可用CH4催化还原NOx,消除氮氧化物的污染。已知:①CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ•mol﹣1,②N2O4(g)⇌2NO2(g)△H=+56.9k•mol﹣1,③CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g)△H=﹣810.1kJ•mol﹣1,从原电池的工作原理分析,可设计为原电池的反应为_____ (填序号)。
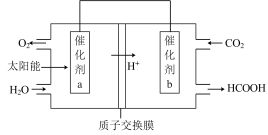
(3)下图是通过光电转化原理,以燃煤产生的二氧化碳为原料,制备新产品的示意图。试写出光电转化过程中总反应的化学方程式:_____ ;催化剂a、b之间连接导线上的电流方向是_____ 。
(1)汽车尾气催化转换器中的反应为2NO(g)+2CO(g)
 2CO2(g)+N2(g)。若在密闭容器中发生该反应时,c(N2)随温度(T)和时间(t)的变化曲线如图所示。
2CO2(g)+N2(g)。若在密闭容器中发生该反应时,c(N2)随温度(T)和时间(t)的变化曲线如图所示。
①由图甲可知,温度T1
②能提高尾气转化率的措施有
a.升高温度 b.降低温度 c.增大压强 d.增大催化剂的比表面积
(2)煤燃烧产生的烟气中含有氮氧化物,可用CH4催化还原NOx,消除氮氧化物的污染。已知:①CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=﹣867kJ•mol﹣1,②N2O4(g)⇌2NO2(g)△H=+56.9k•mol﹣1,③CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(g)△H=﹣810.1kJ•mol﹣1,从原电池的工作原理分析,可设计为原电池的反应为
(3)下图是通过光电转化原理,以燃煤产生的二氧化碳为原料,制备新产品的示意图。试写出光电转化过程中总反应的化学方程式:

您最近一年使用:0次
【推荐3】用化学方法降解水中有机物已成为污水处理领域的重要研究方向。硝基苯是一种具有稳定化学性质、高毒性、难生物降解的污染物。工业上采用吸附、还原、氧化等方法可有效降解废水中的硝基苯。
(1)活性炭因为有较大的比表面积、多孔结构而具有较强的吸附能力,其物理吸附平衡建立如图所示。活性炭处理低浓度的硝基苯废水时,当温度超过50℃,活性炭对硝基苯的吸附量显著下降,原因是:______________________ (请从平衡移动角度解释)。

(2)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图所示。铁炭混合物中极小颗粒的炭分散在铁屑内,具有吸附作用,同时作正极材料构成原电池加快反应速率,还能防止铁屑结块。

①该物质转化示意图可以描述为:___________ 。
②酸性环境中,铁炭混合物处理硝基苯废水,难生物降解的硝基苯首先被还原为亚硝基苯( ),然后进一步被还原成可生物降解的苯胺,写出生成亚硝基苯的电极反应式:
),然后进一步被还原成可生物降解的苯胺,写出生成亚硝基苯的电极反应式:___________ 。
③其他条件一定,反应相同时间,硝基苯的去除率与pH的关系如图所示。pH越大,硝基苯的去除率越低的原因是:___________ 。

(3)研究发现, 在
在 作用下能够生成羟基自由基(HO·)。HO·具有很强的氧化作用,是氧化硝基苯的有效因子。向含
作用下能够生成羟基自由基(HO·)。HO·具有很强的氧化作用,是氧化硝基苯的有效因子。向含 和苯胺(
和苯胺( )的酸性溶液中加入双氧水,写出生成HO·的离子反应方程式:
)的酸性溶液中加入双氧水,写出生成HO·的离子反应方程式:___________ 。
(4)利用电化学装置通过间接氧化法能氧化含苯胺的污水,其原理如图所示。其他条件一定,测得不同初始pH条件下,溶液中苯胺的浓度与时间的关系如图所示。反应相同时间,初始溶液 时苯胺浓度大于
时苯胺浓度大于 时的原因是
时的原因是___________ 。[已知氧化性: ]
]

(1)活性炭因为有较大的比表面积、多孔结构而具有较强的吸附能力,其物理吸附平衡建立如图所示。活性炭处理低浓度的硝基苯废水时,当温度超过50℃,活性炭对硝基苯的吸附量显著下降,原因是:

(2)酸性条件下,铁炭混合物处理污水中硝基苯时的物质转化示意图如图所示。铁炭混合物中极小颗粒的炭分散在铁屑内,具有吸附作用,同时作正极材料构成原电池加快反应速率,还能防止铁屑结块。

①该物质转化示意图可以描述为:
②酸性环境中,铁炭混合物处理硝基苯废水,难生物降解的硝基苯首先被还原为亚硝基苯(
 ),然后进一步被还原成可生物降解的苯胺,写出生成亚硝基苯的电极反应式:
),然后进一步被还原成可生物降解的苯胺,写出生成亚硝基苯的电极反应式:③其他条件一定,反应相同时间,硝基苯的去除率与pH的关系如图所示。pH越大,硝基苯的去除率越低的原因是:

(3)研究发现,
 在
在 作用下能够生成羟基自由基(HO·)。HO·具有很强的氧化作用,是氧化硝基苯的有效因子。向含
作用下能够生成羟基自由基(HO·)。HO·具有很强的氧化作用,是氧化硝基苯的有效因子。向含 和苯胺(
和苯胺( )的酸性溶液中加入双氧水,写出生成HO·的离子反应方程式:
)的酸性溶液中加入双氧水,写出生成HO·的离子反应方程式:(4)利用电化学装置通过间接氧化法能氧化含苯胺的污水,其原理如图所示。其他条件一定,测得不同初始pH条件下,溶液中苯胺的浓度与时间的关系如图所示。反应相同时间,初始溶液
 时苯胺浓度大于
时苯胺浓度大于 时的原因是
时的原因是 ]
]
您最近一年使用:0次



