氧化剂 在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关注。某实验小组以
在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关注。某实验小组以 分解为例,探究浓度、催化剂、温度对反应速率的影响。在常温下按照下表所示的方案完成实验。
分解为例,探究浓度、催化剂、温度对反应速率的影响。在常温下按照下表所示的方案完成实验。
(1)实验①和②的目的是___________ 。同学甲在进行实验①和②时并没有观察到明显现象。资料显示,通常条件下过氧化氢稳定,不易分解。为了达到实验目的,可采取的改进方法是___________ (写出一种即可)。
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化如甲图所示。分析该图能得出的结论是___________ ,___________ ;
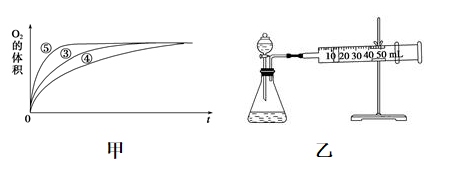
(3)同学乙设计了乙图所示的实验装置对过氧化氢的分解速率进行定量分析,以生成20 气体为准,其他影响实验的因素均已忽略。实验中需要测量的数据是
气体为准,其他影响实验的因素均已忽略。实验中需要测量的数据是___________ 。
(4)向某体积固定的密闭容器中加入0.6 A、0.2
A、0.2 C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回答:
C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回答:
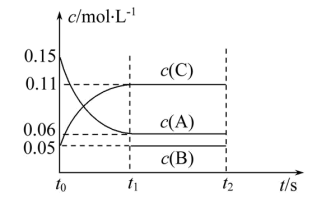
①写出反应的化学方程式:___________ ;
②若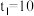 ,则
,则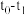 内反应速率
内反应速率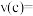
___________ ,A的转化率为___________ ;
③B的起始的物质的量是___________ ;平衡时体系内的压强为初始状态的___________ 倍。
 在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关注。某实验小组以
在反应时不产生污染物,被称为绿色氧化剂,因而受到人们越来越多的关注。某实验小组以 分解为例,探究浓度、催化剂、温度对反应速率的影响。在常温下按照下表所示的方案完成实验。
分解为例,探究浓度、催化剂、温度对反应速率的影响。在常温下按照下表所示的方案完成实验。| 实验编号 | 温度(℃) | 反应物 | 催化剂 |
| ① | 20 | 25 3% 3% 溶液 溶液 | 无 |
| ② | 20 | 25 5% 5% 溶液 溶液 | 无 |
| ③ | 20 | 25 5% 5% 溶液 溶液 | 0.1g |
| ④ | 20 | 25 5% 5% 溶液 溶液 | 1~2滴1  溶液 溶液 |
| ⑤ | 30 | 25 5% 5% 溶液 溶液 | 0.1g |
(2)实验③、④、⑤中,测得生成氧气的体积随时间变化如甲图所示。分析该图能得出的结论是

(3)同学乙设计了乙图所示的实验装置对过氧化氢的分解速率进行定量分析,以生成20
 气体为准,其他影响实验的因素均已忽略。实验中需要测量的数据是
气体为准,其他影响实验的因素均已忽略。实验中需要测量的数据是(4)向某体积固定的密闭容器中加入0.6
 A、0.2
A、0.2 C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回答:
C和一定量(未知)的B三种气体,一定条件下发生反应,各物质浓度随时间变化如图所示。已知在反应过程中混合气体的平均相对分子质量没有变化。请回答:
①写出反应的化学方程式:
②若
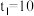 ,则
,则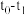 内反应速率
内反应速率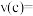
③B的起始的物质的量是
20-21高一下·江西抚州·期末 查看更多[8]
江西省抚州市2020-2021学年高一下学期期末考试化学试题(已下线)2.1.2 影响化学反应速率的因素-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)(已下线)2.1.2 影响化学反应速率的因素-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)海南省华中师范大学海南附属中学2021-2022学年高二上学期第一次月考化学试题(已下线)6.1.2 化学反应速率(第2课时 影响化学反应速率的因素)-【帮课堂】2021-2022学年高一化学同步精品讲义(沪科版2020必修第二册)(已下线)第06讲 影响化学反应速率的因素(word讲义)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)(已下线)第13讲 第二章《化学反应速率与化学平衡》单元测试(培优提升)-【帮课堂】2022-2023学年高二化学同步精品讲义(人教2019选择性必修1)江西省永修县第一中学2023-2024学年高二上学期开学考试化学试题
更新时间:2021-07-01 13:31:14
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】请阅读下列材料,回答下列小题,
人们曾认为N₂+3H₂ 2NH₃化学反应速率小,原材料利用率低,不可能用于工业化生产。化学家们不断地研究和改进该反应的条件,如催化制,温度、压强等,并更新设备,成功地开发了合成氨的生产工艺。从此,人类能为植物的生长提供足够的氮肥。道解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。
2NH₃化学反应速率小,原材料利用率低,不可能用于工业化生产。化学家们不断地研究和改进该反应的条件,如催化制,温度、压强等,并更新设备,成功地开发了合成氨的生产工艺。从此,人类能为植物的生长提供足够的氮肥。道解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。
(1)合成氨的反应属于___________
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
(2)下列反应条件的改变对反应速率的影响正确的是___________
A.增大N2的浓度能加快反应速率 B.减小H2的浓度能加快反应速率
C.升高温度能减慢反应速率 D.添加催化剂对反应速率无影响
(3)合成氨为放热反应,下列说法正确的是___________
A.断开H-H键放出能量
B.形成N-H键吸收能量
C.反应物的总能量大于生成物的总能量
D.反应物的总能量小于生成物的总能量
人们曾认为N₂+3H₂
 2NH₃化学反应速率小,原材料利用率低,不可能用于工业化生产。化学家们不断地研究和改进该反应的条件,如催化制,温度、压强等,并更新设备,成功地开发了合成氨的生产工艺。从此,人类能为植物的生长提供足够的氮肥。道解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。
2NH₃化学反应速率小,原材料利用率低,不可能用于工业化生产。化学家们不断地研究和改进该反应的条件,如催化制,温度、压强等,并更新设备,成功地开发了合成氨的生产工艺。从此,人类能为植物的生长提供足够的氮肥。道解了地球上有限的耕地资源与庞大的粮食需求之间的矛盾。(1)合成氨的反应属于
A.化合反应 B.分解反应 C.置换反应 D.复分解反应
(2)下列反应条件的改变对反应速率的影响正确的是
A.增大N2的浓度能加快反应速率 B.减小H2的浓度能加快反应速率
C.升高温度能减慢反应速率 D.添加催化剂对反应速率无影响
(3)合成氨为放热反应,下列说法正确的是
A.断开H-H键放出能量
B.形成N-H键吸收能量
C.反应物的总能量大于生成物的总能量
D.反应物的总能量小于生成物的总能量
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】一定条件下铁可以和CO2发生反应Fe(s)+CO2(g) FeO(s)+CO(g)。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和 CO 气体的浓度变化与时间的关系如图所示。
FeO(s)+CO(g)。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和 CO 气体的浓度变化与时间的关系如图所示。
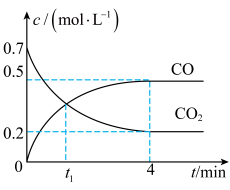
(1)t1 min 时,正、逆反应速率的大小关系为v正_____ v逆(填“>”“<”或“=”)。该温度下,化学平衡常数 K=_____ 。
(2)4min 时, CO2的转化率为___________ ;0-4min 内,CO 的平均反应速率v(CO)= ___________
(3)下列条件的改变能减慢上述反应的反应速率的是___________
①降低温度;②减少铁粉的质量;③保持压强不变,充入 He 使容器的体积增大;④保持体积不变,充入 He 使体系压强增大
(4)下列选项能说明上述反应已达平衡状态的是___________ 。
① v(CO)=v(CO2)
②单位时间内生成nmolCO2 的同时生成 n mol CO
③容器中气体压强不随时间的变化而变化
④容器中气体的平均相对分子质量不随时间的变化而变化
 FeO(s)+CO(g)。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和 CO 气体的浓度变化与时间的关系如图所示。
FeO(s)+CO(g)。一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和 CO 气体的浓度变化与时间的关系如图所示。
(1)t1 min 时,正、逆反应速率的大小关系为v正
(2)4min 时, CO2的转化率为
(3)下列条件的改变能减慢上述反应的反应速率的是
①降低温度;②减少铁粉的质量;③保持压强不变,充入 He 使容器的体积增大;④保持体积不变,充入 He 使体系压强增大
(4)下列选项能说明上述反应已达平衡状态的是
① v(CO)=v(CO2)
②单位时间内生成nmolCO2 的同时生成 n mol CO
③容器中气体压强不随时间的变化而变化
④容器中气体的平均相对分子质量不随时间的变化而变化
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO。
(1)反应需要在闪电或极高温条件下发生,说明该反应_________ 。(填字母)
A.所需的活化能很高 B.吸收的能量很多
(2)在不同温度下,反应N2(g)+O2(g) 2NO(g)的平衡常数K如下表:
2NO(g)的平衡常数K如下表:
①该反应的△H_____ 0。(填“>”、“=”或“<”)
②其他条件相同时,在上述三个温度下分别发生该反应。1538℃时,N2的转化率随时间变化如右图所示,请补充完成1760℃、2404℃时N2的转化率随时间变化的示意图。
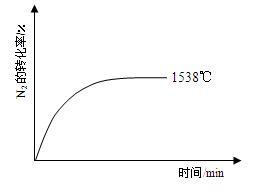
________ 。
(3)2404℃时,在容积为1.0L的密闭容器中通入2.6mol N2和2.6mol O2,计算反应N2(g)+O2(g) 2NO(g)达到平衡时NO的浓度
2NO(g)达到平衡时NO的浓度_______ 。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)
(1)反应需要在闪电或极高温条件下发生,说明该反应
A.所需的活化能很高 B.吸收的能量很多
(2)在不同温度下,反应N2(g)+O2(g)
 2NO(g)的平衡常数K如下表:
2NO(g)的平衡常数K如下表:| 温度/℃ | 1538 | 1760 | 2404 |
| 平衡常数K | 0.86×10-4 | 2.6×10-4 | 64×10-4 |
①该反应的△H
②其他条件相同时,在上述三个温度下分别发生该反应。1538℃时,N2的转化率随时间变化如右图所示,请补充完成1760℃、2404℃时N2的转化率随时间变化的示意图。

(3)2404℃时,在容积为1.0L的密闭容器中通入2.6mol N2和2.6mol O2,计算反应N2(g)+O2(g)
 2NO(g)达到平衡时NO的浓度
2NO(g)达到平衡时NO的浓度
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
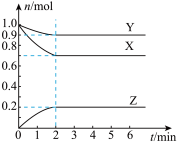
【推荐1】某温度时,在一个容积为 的密闭容器中,
的密闭容器中,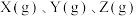 三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白。
三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白。
(1)该反应的化学方程式为______ 。
(2)反应开始至 ,气体
,气体 的平均反应速率
的平均反应速率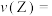
______ ;不同条件下测得该反应的速率为:①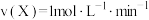 、②
、② 、③
、③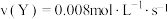 三种情况下该反应化学反应速率最小的是
三种情况下该反应化学反应速率最小的是______ (填序号)。
(3)为了增大平衡时 的转化率,可采取的措施是
的转化率,可采取的措施是______ (填字母)。
a.增大压强 b.使用合适的催化剂
c.增大 和
和 的初始投料比 d.及时分离出产物Z
的初始投料比 d.及时分离出产物Z
(4)上述反应在 内反应速率与时间图像如图所示,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是______(填字母)。
内反应速率与时间图像如图所示,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是______(填字母)。

(5)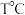 时,将等量的
时,将等量的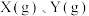 放在两个容积相等的容器中反应,并达到平衡。在该过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中
放在两个容积相等的容器中反应,并达到平衡。在该过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中 的百分含量为
的百分含量为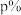 ,则乙容器中
,则乙容器中 的百分含量
的百分含量______ 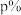 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。
 的密闭容器中,
的密闭容器中,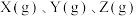 三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白。
三种物质的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白。(1)该反应的化学方程式为
(2)反应开始至
 ,气体
,气体 的平均反应速率
的平均反应速率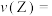
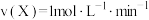 、②
、② 、③
、③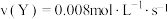 三种情况下该反应化学反应速率最小的是
三种情况下该反应化学反应速率最小的是
(3)为了增大平衡时
 的转化率,可采取的措施是
的转化率,可采取的措施是a.增大压强 b.使用合适的催化剂
c.增大
 和
和 的初始投料比 d.及时分离出产物Z
的初始投料比 d.及时分离出产物Z(4)上述反应在
 内反应速率与时间图像如图所示,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是______(填字母)。
内反应速率与时间图像如图所示,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是______(填字母)。
A.在 时增大了压强 时增大了压强 | B.在 时加入催化剂 时加入催化剂 |
C.在 时可能降低了温度 时可能降低了温度 | D. 时 时 的转化率最高 的转化率最高 |
(5)
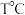 时,将等量的
时,将等量的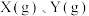 放在两个容积相等的容器中反应,并达到平衡。在该过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中
放在两个容积相等的容器中反应,并达到平衡。在该过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中 的百分含量为
的百分含量为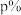 ,则乙容器中
,则乙容器中 的百分含量
的百分含量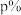 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】在2L密闭容器内,800℃时反应:2NO(g)+O2(g) 2NO2(g)体系中,c(NO)随时间的变化如表:
2NO2(g)体系中,c(NO)随时间的变化如表:
(1)分析上表,该反应达到平衡状态所需时间是_________ 。
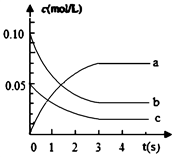
(2)上图中表示NO2的浓度变化曲线是_______________ 。
(3)用NO表示从0~2s内该反应的平均速率v=________ 。
(4)v(NO):v(O2) =______________ 。
(5)达到平衡状态时O2的转化率为________ 。
 2NO2(g)体系中,c(NO)随时间的变化如表:
2NO2(g)体系中,c(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)(mol/L) | 0.10 | 0.05 | 0.04 | 0.03 | 0.03 | 0.03 |
(1)分析上表,该反应达到平衡状态所需时间是

(2)上图中表示NO2的浓度变化曲线是
(3)用NO表示从0~2s内该反应的平均速率v=
(4)v(NO):v(O2) =
(5)达到平衡状态时O2的转化率为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】一定温度下,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如图所示:
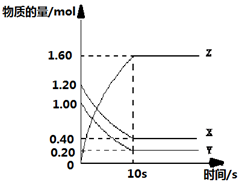
(1)反应的化学方程式为___________________ 。
(2)反应开始到10s,用X表示的平均反应速率为_______________ 。
(3)Y的转化率是_______________________ 。
下列关于该反应的说法正确的是__________ 。
A.10s时,该反应已经停止
B.10s之前X的消耗速率小于它的生成速率
C. 10s时正反应速率等于逆反应速率
D. 10s时X、Y、Z的浓度保持不变

(1)反应的化学方程式为
(2)反应开始到10s,用X表示的平均反应速率为
(3)Y的转化率是
下列关于该反应的说法正确的是
A.10s时,该反应已经停止
B.10s之前X的消耗速率小于它的生成速率
C. 10s时正反应速率等于逆反应速率
D. 10s时X、Y、Z的浓度保持不变
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】某温度下,在2 L恒容密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。回答下列问题:
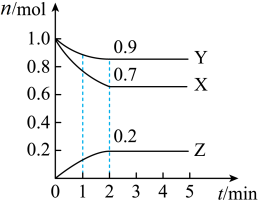
(1)2min内,气体Z的平均反应速率为_______  ;平衡时,气体Y的体积分数为
;平衡时,气体Y的体积分数为_______ %。
(2)该反应的化学方程式可以表示为_______ 。
(3)1 min时,
_______ (填“>”或“<”或“=”,下同) ;2 min时,
;2 min时,
_______ 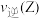 。
。
(4)反应达到平衡状态后,向容器中通入氩气,气体X的化学反应速率不变的原因是_______ 。
(5)若X、Y、Z均为气体(容器体积不变),下列能说明反应已达平衡的是_______ (填字母)。
a.X、Y、Z三种气体的物质的量相等 b.混合气体的密度不随时间变化
c.容器内气体压强不变 d.反应速率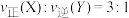

(1)2min内,气体Z的平均反应速率为
 ;平衡时,气体Y的体积分数为
;平衡时,气体Y的体积分数为(2)该反应的化学方程式可以表示为
(3)1 min时,

 ;2 min时,
;2 min时,
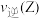 。
。(4)反应达到平衡状态后,向容器中通入氩气,气体X的化学反应速率不变的原因是
(5)若X、Y、Z均为气体(容器体积不变),下列能说明反应已达平衡的是
a.X、Y、Z三种气体的物质的量相等 b.混合气体的密度不随时间变化
c.容器内气体压强不变 d.反应速率
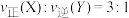
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在一定条件下,容积为2L的密闭容器中,将2molL气体和3molM气体混合,发生如下反应:2L(g)+3M(g) xQ(g)+3R(g),10s末,生成2.4molR,并测得Q的浓度为0.4mol•L-1.计算:
xQ(g)+3R(g),10s末,生成2.4molR,并测得Q的浓度为0.4mol•L-1.计算:
(1)10s末L的物质的量浓度为___________ 。
(2)前10s内用M表示的化学反应速率为___________ 。
(3)化学方程式中x值为___________ 。
(4)L(g)的转化率为___________ 。
(5)在恒温恒容条件下,往容器中加入1mol氦气,反应速率___________ 。(填“增大”、“减小”或“不变”,下同)。
 xQ(g)+3R(g),10s末,生成2.4molR,并测得Q的浓度为0.4mol•L-1.计算:
xQ(g)+3R(g),10s末,生成2.4molR,并测得Q的浓度为0.4mol•L-1.计算:(1)10s末L的物质的量浓度为
(2)前10s内用M表示的化学反应速率为
(3)化学方程式中x值为
(4)L(g)的转化率为
(5)在恒温恒容条件下,往容器中加入1mol氦气,反应速率
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】Ⅰ、某温度时,在一个 10L 的恒容容器中,X、Y、Z 均为气体,三种物质的物质的量随时间的变化曲线如图所示。根据图中数据填空:
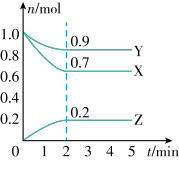
(1)该反应的化学方程式为:________________________ 。
(2)反应开始至 2min,以气体 Z 表示的平均反应速率为:____________________ 。
(3)将 a mol X 与 b mol Y 的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=2n(Z),则原混合气体中 a∶b=________ 。
Ⅱ、在恒温恒容的密闭容器中,当下列物理量不再发生变化时:
①混合气体的压强,②混合气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜色,⑥各反应物或生成物的反应速率之比等于化学计量数之比。
(1)一定能证明2SO2(g)+O2(g) ⇌2SO3(g)达到平衡状态的是__________________ 填序号,下同)。
(2)一定能证明 I2(g)+H2(g)⇌2HI(g)达到平衡状态的是____________________ 。
(3)一定能证明 A(s)+2B(g)⇌C(g)+D(g)达到平衡状态的是_________________ (B、C、D 均无色)。

(1)该反应的化学方程式为:
(2)反应开始至 2min,以气体 Z 表示的平均反应速率为:
(3)将 a mol X 与 b mol Y 的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n(X)=n(Y)=2n(Z),则原混合气体中 a∶b=
Ⅱ、在恒温恒容的密闭容器中,当下列物理量不再发生变化时:
①混合气体的压强,②混合气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜色,⑥各反应物或生成物的反应速率之比等于化学计量数之比。
(1)一定能证明2SO2(g)+O2(g) ⇌2SO3(g)达到平衡状态的是
(2)一定能证明 I2(g)+H2(g)⇌2HI(g)达到平衡状态的是
(3)一定能证明 A(s)+2B(g)⇌C(g)+D(g)达到平衡状态的是
您最近一年使用:0次



