铁在地壳中含量丰富,也是重要的人体微量元素之一
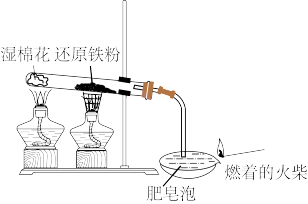
(1)用铁粉进行如图所示的实验,铁与水蒸气反应的化学方程式为_______ 。
(2)实验装置中,加热铁粉的酒精灯配用金属套筒的目的是_______ 。
(3)验证菠菜中铁元素的存在。
①取新鲜菠菜切开表皮,在内部组织上滴加KSCN溶液,无颜色变化,说明菠菜中铁元素不以_______ (填离子符号)形式存在。
②另取新鲜菠菜洗净、烘干,放入_______ 中灼烧成灰烬。冷却后将灰烬移入烧杯中,加入HNO3溶液至没有气体产生,加蒸馏水稀释,充分搅拌后过滤。取少量滤液于试管中,加入KSCN溶液,溶液变为_______ 色,由此推断滤液中有Fe3+。实验中加入HNO3溶液的目的为_______ 。
(4)为了防止缺铁性贫血,一些食品中允许添加含铁物质。某种麦片含有微量的还原铁粉,铁粉在胃酸的作用下会溶解。铁与盐酸反应的离子方程式为_______ 。

(1)用铁粉进行如图所示的实验,铁与水蒸气反应的化学方程式为
(2)实验装置中,加热铁粉的酒精灯配用金属套筒的目的是
(3)验证菠菜中铁元素的存在。
①取新鲜菠菜切开表皮,在内部组织上滴加KSCN溶液,无颜色变化,说明菠菜中铁元素不以
②另取新鲜菠菜洗净、烘干,放入
(4)为了防止缺铁性贫血,一些食品中允许添加含铁物质。某种麦片含有微量的还原铁粉,铁粉在胃酸的作用下会溶解。铁与盐酸反应的离子方程式为
2021高一下·广东·学业考试 查看更多[2]
更新时间:2021-07-14 09:31:20
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】如图所示装置,可用来制取和观察Fe(OH)2在空气中被氧化的颜色变化。实验时必须使用铁屑和6 mol·L-1的硫酸,其他试剂任选。

填写下列空白:
(1)B中盛有一定量的NaOH溶液,A中应预先加入的试剂是___________ ,A中反应的离子方程式是:___________ 。
(2)实验开始时应先将活塞a___________ (填“打开”或“关闭”)。
(3)实验完毕,打开b处活塞,放入一部分空气,此时B中发生反应的化学方程式为___________ 。
(4)下图中___________ 能较长时间看到Fe(OH)2白色沉淀。


填写下列空白:
(1)B中盛有一定量的NaOH溶液,A中应预先加入的试剂是
(2)实验开始时应先将活塞a
(3)实验完毕,打开b处活塞,放入一部分空气,此时B中发生反应的化学方程式为
(4)下图中

您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】已知A→C必须加热,否则会发生钝化现象。请回答下列问题:
(1)A是________ ,你推断的理由是___________________ 。
(2)B在酸性条件下与H2O2反应的离子方程式:_____________________ 。
(3)A与过量浓H2SO4反应的化学方程式:_______________________ 。

(1)A是
(2)B在酸性条件下与H2O2反应的离子方程式:
(3)A与过量浓H2SO4反应的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】某化工厂以废金属(主要成分为Fe和Cu,表面有少量油污)为原料回收海绵铜,并制备氯化铁的工艺流程如图所示。
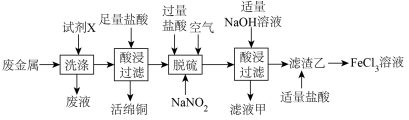
已知:NaNO2易溶于水且不与氢氧化钠反应,在“氧化”中起催化作用。该反应的化学方程式为: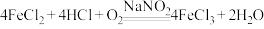
回答问题:
(1)“洗涤”的目的是去除废金属表面的油污,试剂X最好选用_______(填标号)。
(2)“酸浸”中发生反应的化学方程式为_______ 。
(3)“滤液甲”中一定含有的溶质是_______ 。
(4)向“滤渣乙”中加入适量盐酸,可以观察到的现象是_______ 。

已知:NaNO2易溶于水且不与氢氧化钠反应,在“氧化”中起催化作用。该反应的化学方程式为:
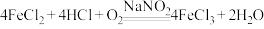
回答问题:
(1)“洗涤”的目的是去除废金属表面的油污,试剂X最好选用_______(填标号)。
| A.水 | B.氢氧化钠溶液 | C.稀硫酸 | D.氯化钠溶液 |
(3)“滤液甲”中一定含有的溶质是
(4)向“滤渣乙”中加入适量盐酸,可以观察到的现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】甲、乙同学对Fe及其化合物的相关性质与用途进行探究。
(1)实验I:甲、乙两同学分别用下图装置进行Fe粉与水蒸气反应的实验。
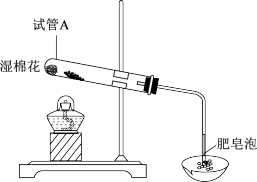
①证明生成的气体是氢气,依据的现象是_______ 。
②该反应的化学方程式是_______ 。
(2)实验II:甲、乙同学分别对各自实验I反应后的黑色固体进行研究。冷却取试管A中冷却后的固体加入过量稀HCl,充分反应后将溶液分成两份(如图)。请将下表中的现象或结论补充完整。
已知: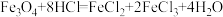
(1)实验I:甲、乙两同学分别用下图装置进行Fe粉与水蒸气反应的实验。

①证明生成的气体是氢气,依据的现象是
②该反应的化学方程式是
(2)实验II:甲、乙同学分别对各自实验I反应后的黑色固体进行研究。冷却取试管A中冷却后的固体加入过量稀HCl,充分反应后将溶液分成两份(如图)。请将下表中的现象或结论补充完整。
已知:
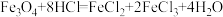
| 操作过程 | 现象及结论 | |
| 甲同学 | 乙同学 | |
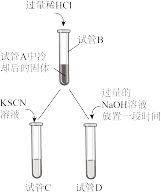 | 试管B中固体全部溶解,得到溶液M | 试管B固体全部溶解,同时有大量气泡产生,得到溶液N |
| 试管C溶液变红 | 试管C溶液没有变红,用离子方程式解释原因② | |
| 试管D开始有红褐色和灰绿色沉淀生成,最终全部变为红褐色。则溶液M中存在的阳离子有① | 试管D实验现象是③ 产生该现象发生的氧化还原反应的化学方程式是④ | |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】红热的铁能与水蒸气反应,有氢气生成,现用如图所示装置进行铁在高温下与水蒸气反应的实验,并用简单的方法收集、检验生成的氢气。请回答下列问题:

(1)写出铁在高温下与水蒸气反应的化学方程式:____________________________ 。
(2)干燥管C中盛放的是碱石灰,其作用是___________________ 。
(3)把B中反应后的产物加入足量的盐酸,用该溶液制取FeCl3·6H2O晶体。
①欲检验溶液中含有Fe3+,选用的试剂为____________ ,现象是______________________ 。
②该实验小组同学用上述试剂没有检测到Fe3+,用离子方程式解释滤液中不存在Fe3+可能的的原因:_________________ 。
③将此滤液中FeCl2完全氧化为FeCl3最好选择下列物质中的_______ 。
A.酸性KMnO4溶液 B.Cl2 C.Na2O2 D.FeCl3

(1)写出铁在高温下与水蒸气反应的化学方程式:
(2)干燥管C中盛放的是碱石灰,其作用是
(3)把B中反应后的产物加入足量的盐酸,用该溶液制取FeCl3·6H2O晶体。
①欲检验溶液中含有Fe3+,选用的试剂为
②该实验小组同学用上述试剂没有检测到Fe3+,用离子方程式解释滤液中不存在Fe3+可能的的原因:
③将此滤液中FeCl2完全氧化为FeCl3最好选择下列物质中的
A.酸性KMnO4溶液 B.Cl2 C.Na2O2 D.FeCl3
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】图中各物质均为中学化学中的常见物质,其中只有A、G为单质;D的摩尔质量比E小16,E为红棕色气体:可用 溶液检验Ⅰ中的阳离子。它们之间的相互转化关系如图所示(图中部分产物、反应条件未列出).
溶液检验Ⅰ中的阳离子。它们之间的相互转化关系如图所示(图中部分产物、反应条件未列出).
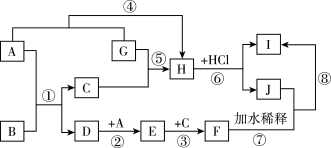
(1)B的用途为_______ (任写一种)
(2)反应③中氧化产物与还原产物的物质的量之比为_______
(3)反应⑤的化学方程式为_______
(4)实验在配制J溶液时,要加入一定量的G,其原因是_______ (用离子方程式表示)
(5)反应⑧的离子方程式为_______
 溶液检验Ⅰ中的阳离子。它们之间的相互转化关系如图所示(图中部分产物、反应条件未列出).
溶液检验Ⅰ中的阳离子。它们之间的相互转化关系如图所示(图中部分产物、反应条件未列出).
(1)B的用途为
(2)反应③中氧化产物与还原产物的物质的量之比为
(3)反应⑤的化学方程式为
(4)实验在配制J溶液时,要加入一定量的G,其原因是
(5)反应⑧的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】氯化亚铜是重要的铜盐系列化工产品,广泛应用于石油化工、有机合成等行业。CuCl晶体呈白色,见光易分解,微溶于水,不溶于稀盐酸和乙醇,露置于潮湿空气中易水解氧化为绿色的 。某研究小组以
。某研究小组以 (含少量
(含少量 )粗品为原料制取CuCl,设计的合成路线如下:
)粗品为原料制取CuCl,设计的合成路线如下:
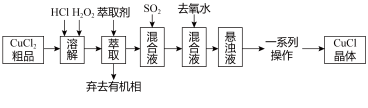
已知:①在较高浓度的盐酸下, 能溶解于甲基异丁基甲酮。
能溶解于甲基异丁基甲酮。
②CuCl在溶液中存在: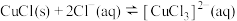
(1)上述合成路线中, 的作用是
的作用是________________________ ,萃取剂为甲基异丁基甲酮,其作用是________________ 。
(2)上述合成路线中, 通入混合液的实验装置如图所示:
通入混合液的实验装置如图所示:

①装置B、D的作用分别是________________________________________________ 。
②C中反应的离子方程式是___________________________________ 。
(3)上述合成路线中,向混合液中加入大量去氧水的目的是______________________ 。
(4)上述合成路线中,一系列操作包括:抽滤、洗涤、干燥。
干燥时应注意密封、_________________________ 。
 。某研究小组以
。某研究小组以 (含少量
(含少量 )粗品为原料制取CuCl,设计的合成路线如下:
)粗品为原料制取CuCl,设计的合成路线如下:
已知:①在较高浓度的盐酸下,
 能溶解于甲基异丁基甲酮。
能溶解于甲基异丁基甲酮。②CuCl在溶液中存在:
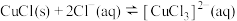
(1)上述合成路线中,
 的作用是
的作用是(2)上述合成路线中,
 通入混合液的实验装置如图所示:
通入混合液的实验装置如图所示:
①装置B、D的作用分别是
②C中反应的离子方程式是
(3)上述合成路线中,向混合液中加入大量去氧水的目的是
(4)上述合成路线中,一系列操作包括:抽滤、洗涤、干燥。
干燥时应注意密封、
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】2013年6月,我国“蛟龙”号再次刷新“中国深度”——下潜7062米,为我国深海矿物资源的开发奠定了基础。海洋深处有丰富的锰结核矿,锰结核的主要成分是MnO2,同时还含有黄铜矿。
Ⅰ.“蛟龙”号外壳是用特殊的钛合金材料制成,它可以在7000m的深海中承受重压,Ti是以钛白粉(TiO2)为原料进行生产,钛白粉是利用TiO2+和水反应生成钛酸(H2TiO3)沉淀,再煅烧沉淀制得的。TiO2+和水反应的离子方程式为___ 。
Ⅱ.MnO2是一种重要的无机功能材料,工业上从锰结核中制取纯净的MnO2工艺流程如图所示:

(1)步骤Ⅱ中以NaClO3为氧化剂,当生成0.05 mol MnO2时,消耗0.1 mol/L的NaClO3溶液200 mL,该反应离子方程式为___ 。
(2)已知溶液B的溶质之一可循环用于上述生产,此物质的名称是___ 。
Ⅲ.利用黄铜矿炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3等)可制备Fe2O3,方法为:
(A)用过量的稀盐酸浸取炉渣、过滤;
(B)向滤液中加入5%的H2O2,再向其中加入过量的NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得到Fe2O3。
根据以上信息回答下列问题:
(1)(B)中向滤液中加入5%的H2O2,其目的是___ 。
(2)设计实验证明炉渣中含有FeO___ 。
(3)将煅烧得到的Fe2O3还原为Fe单质,再将质量为mg的Fe单质分成相等的四份,分别与50 mL、100 mL、150 mL、200 mL的等浓度的稀硝酸反应,反应产物NO在标况下的体积见表:
则:①m=___ g
②写出实验②发生反应后溶液中Fe2+与Fe3+物质的量之比为:___ 。
③所用硝酸的物质的量浓度为__ mol/L。
Ⅰ.“蛟龙”号外壳是用特殊的钛合金材料制成,它可以在7000m的深海中承受重压,Ti是以钛白粉(TiO2)为原料进行生产,钛白粉是利用TiO2+和水反应生成钛酸(H2TiO3)沉淀,再煅烧沉淀制得的。TiO2+和水反应的离子方程式为
Ⅱ.MnO2是一种重要的无机功能材料,工业上从锰结核中制取纯净的MnO2工艺流程如图所示:

(1)步骤Ⅱ中以NaClO3为氧化剂,当生成0.05 mol MnO2时,消耗0.1 mol/L的NaClO3溶液200 mL,该反应离子方程式为
(2)已知溶液B的溶质之一可循环用于上述生产,此物质的名称是
Ⅲ.利用黄铜矿炼铜产生的炉渣(含Fe2O3、FeO、SiO2、Al2O3等)可制备Fe2O3,方法为:
(A)用过量的稀盐酸浸取炉渣、过滤;
(B)向滤液中加入5%的H2O2,再向其中加入过量的NaOH溶液,过滤,将沉淀洗涤、干燥、煅烧得到Fe2O3。
根据以上信息回答下列问题:
(1)(B)中向滤液中加入5%的H2O2,其目的是
(2)设计实验证明炉渣中含有FeO
(3)将煅烧得到的Fe2O3还原为Fe单质,再将质量为mg的Fe单质分成相等的四份,分别与50 mL、100 mL、150 mL、200 mL的等浓度的稀硝酸反应,反应产物NO在标况下的体积见表:
| 实验 | ① | ② | ③ | ④ |
| V(HNO3)/L | 50 | 100 | 150 | 200 |
| V(NO)/L | 1.344 | 2.688 | 3.36 | 3.36 |
则:①m=
②写出实验②发生反应后溶液中Fe2+与Fe3+物质的量之比为:
③所用硝酸的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】下图是利用废铜屑(含杂质铁)制备胆矾(硫酸铜晶体)的流程。
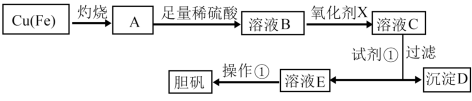
已知:
请回答:
(1)溶液B中含有的阳离子有_______ (填离子符号)。
(2)下列物质中最适宜做氧化剂X的是_______ (填字母)。
a.NaClO b.H2O2 c.KMnO4
(3)加入试剂①是为了调节pH,试剂①可以选择_______ (填化学式)。
(4)沉淀D加入盐酸可以得到FeCl3,关于FeCl3溶液的性质中说法不正确的是_______ 。
a.将FeCl3饱和溶液逐滴加入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔效应
b.向FeCl3溶液滴加NaOH溶液,出现红褐色沉淀
c.将FeCl3溶液加热蒸干并灼烧,得到FeCl3固体
d.向FeCl3溶液中滴加KSCN溶液,溶液变为红色
(5)沉淀D加入盐酸和铁粉,可以制得FeCl2溶液,实验室保存FeCl2溶液,需加入过量的铁粉,其原因是_______ (用离子方程式表示),还需要加入过量的盐酸,原因是_______ 。

已知:
| 溶液中被沉淀离子 | Fe3+ | Fe2+ | Cu2+ |
| 完全生成氢氧化物沉淀时,溶液的pH | ≥3.7 | ≥6.4 | ≥4.4 |
(1)溶液B中含有的阳离子有
(2)下列物质中最适宜做氧化剂X的是
a.NaClO b.H2O2 c.KMnO4
(3)加入试剂①是为了调节pH,试剂①可以选择
(4)沉淀D加入盐酸可以得到FeCl3,关于FeCl3溶液的性质中说法不正确的是
a.将FeCl3饱和溶液逐滴加入沸水中,并继续加热得到红褐色液体,该液体能产生丁达尔效应
b.向FeCl3溶液滴加NaOH溶液,出现红褐色沉淀
c.将FeCl3溶液加热蒸干并灼烧,得到FeCl3固体
d.向FeCl3溶液中滴加KSCN溶液,溶液变为红色
(5)沉淀D加入盐酸和铁粉,可以制得FeCl2溶液,实验室保存FeCl2溶液,需加入过量的铁粉,其原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某研究性学习小组利用如图所示的装置制备无水氯化铁。
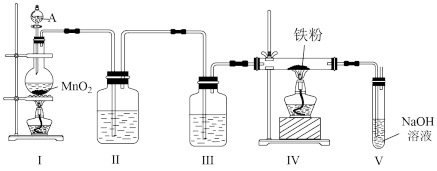
(1)装置Ⅰ中仪器A的名称是_______ ,写出装置Ⅰ中制备氯气的离子方程式_______ 。
(2)装置Ⅱ的作用是_______ 。
(3)写出在装置V中发生的反应的化学方程式_______ 。
(4)实验结束后将装置Ⅳ中的固体加水溶解并过滤,往滤液中滴加KSCN溶液,观察到_______ ,即可证明滤液中含有 。
。
(5)另一组同学发现,在装置Ⅳ和装置Ⅴ之间还需要增加一个装置才能制得无水氯化铁。为了达到这一实验目的,你认为还需在装置Ⅳ和装置Ⅴ之间添加下图中的_______ 装置(填序号)。


(1)装置Ⅰ中仪器A的名称是
(2)装置Ⅱ的作用是
(3)写出在装置V中发生的反应的化学方程式
(4)实验结束后将装置Ⅳ中的固体加水溶解并过滤,往滤液中滴加KSCN溶液,观察到
 。
。(5)另一组同学发现,在装置Ⅳ和装置Ⅴ之间还需要增加一个装置才能制得无水氯化铁。为了达到这一实验目的,你认为还需在装置Ⅳ和装置Ⅴ之间添加下图中的

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】已知稀溴水和稀氯化铁溶液都呈黄色,若在足量的稀氯化亚铁溶液中,加入1~2滴液溴,振荡后溶液呈黄色,现对溶液呈黄色的原因进行探究。
(1)仅限选用的仪器和试剂有:烧杯、试管、玻璃棒、量筒、胶头滴管、药匙;酸性高锰酸钾溶液、氢氧化钠溶液、四氯化碳、硫氰化钾溶液、硝酸银溶液、淀粉碘化钾溶液,完成以下实验探究过程:
【提出假设】
假设①:溶液呈黄色不是发生化学反应所致,是溶液中___________ 引起的(填微粒的化学式,下同)。
假设②:溶液呈黄色是发生化学反应所致,是溶液中___________ 引起的。
【设计实验方案】
为了验证上述假设①和假设②的推断,请用简要的文字说明你的实验方案:
假设①方案:___________ 。
假设②方案:___________ 。
(2)根据高中所学的知识判断,你认为___________ (填“假设①”或“假设②”)的推断是正确的;若选用淀粉碘化钾溶液验证你的假设是否可行?___________ (填“可行”或“不可行”),理由是___________ 。
(1)仅限选用的仪器和试剂有:烧杯、试管、玻璃棒、量筒、胶头滴管、药匙;酸性高锰酸钾溶液、氢氧化钠溶液、四氯化碳、硫氰化钾溶液、硝酸银溶液、淀粉碘化钾溶液,完成以下实验探究过程:
【提出假设】
假设①:溶液呈黄色不是发生化学反应所致,是溶液中
假设②:溶液呈黄色是发生化学反应所致,是溶液中
【设计实验方案】
为了验证上述假设①和假设②的推断,请用简要的文字说明你的实验方案:
假设①方案:
假设②方案:
(2)根据高中所学的知识判断,你认为
您最近一年使用:0次




