某化学兴趣小组的几位同学探究原电池原理的应用时,做了如图的实验:
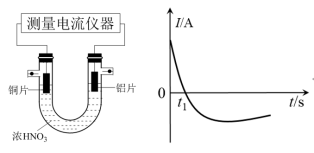
(1)甲同学利用打磨过的铜片和铝片设计了如图的实验装置,并测量和绘制了原电池的电流(I)随时间(t)的变化曲线(极短时间电流反转),则图中t1时刻之后阶段,负极材料是___________ 。
II.铜与浓硝酸反应探究
(2)乙同学将铜片直接放入浓硝酸中:
①实验现象为___________ ,溶液显绿色。
②待反应停止后,若铜有剩余,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,原因是___________ (用离子方程式表示)。
(3)电化学降解NO 的原理如图所示。
的原理如图所示。
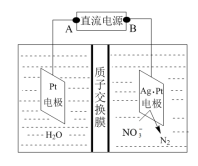
电源正极为___________ (填“A”或“B”),阳极的电极反应式为___________ 。若电解过程中转移了2mol电子,则膜两侧电极液的质量变化差(△m左-△m右)为___________ 。
(1)甲同学利用打磨过的铜片和铝片设计了如图的实验装置,并测量和绘制了原电池的电流(I)随时间(t)的变化曲线(极短时间电流反转),则图中t1时刻之后阶段,负极材料是

II.铜与浓硝酸反应探究
(2)乙同学将铜片直接放入浓硝酸中:
①实验现象为
②待反应停止后,若铜有剩余,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,原因是
(3)电化学降解NO
 的原理如图所示。
的原理如图所示。
电源正极为
更新时间:2021-07-26 09:19:31
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】物质的类别和元素的化合价是研究物质性质的两个重要角度。下图是部分含氮和含氯物质的价类二维图,回答下列问题:
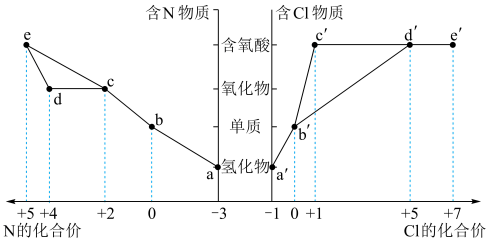
(1)b的化学式为___________ 。
(2)b′能溶于水还能与水反应,其水溶液显___________ 。(填“酸性、碱性或中性”)
(3)将a和a′两种气体混合产生的现象是___________ 。
(4)实验室制取b′气体用浓a′溶液滴入 中并加热,其反应的离子方程式为
中并加热,其反应的离子方程式为___________ 。
(5)工业上制备
___________ (填“能”或“不能”)通过a→b→c→e流程实现。
(6)由上述两种元素组成的液态化合物 ,遇水可生成化合物a和c′,该反应的化学方程式为
,遇水可生成化合物a和c′,该反应的化学方程式为___________ 。

(1)b的化学式为
(2)b′能溶于水还能与水反应,其水溶液显
(3)将a和a′两种气体混合产生的现象是
(4)实验室制取b′气体用浓a′溶液滴入
 中并加热,其反应的离子方程式为
中并加热,其反应的离子方程式为(5)工业上制备

(6)由上述两种元素组成的液态化合物
 ,遇水可生成化合物a和c′,该反应的化学方程式为
,遇水可生成化合物a和c′,该反应的化学方程式为
您最近一年使用:0次
【推荐2】已知A是气体单质,E是一种常见的强酸。A、B、C、D、E是含有一种相同元素的五种物质,在一定条件下可发生如图所示的转化。
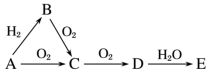
(1)写出电子式:A_______ ;B_______ 。
(2)写出D→E的化学方程式_______ ;
(3)B是一种重要的化工原料,用途十分广泛。实验室制取B,常用_______ (填干燥剂名称)干燥B,用_______ 法收集B,实验室制取B的化学方程式为_______ 。
(4)写出E的溶液和气体B反应的离子方程式_______ 。
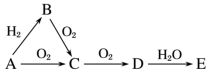
(1)写出电子式:A
(2)写出D→E的化学方程式
(3)B是一种重要的化工原料,用途十分广泛。实验室制取B,常用
(4)写出E的溶液和气体B反应的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】物质的类别和核心元素的化合价是研究物质性质的两个重要角度。请根据如图所示,回答下列问题:
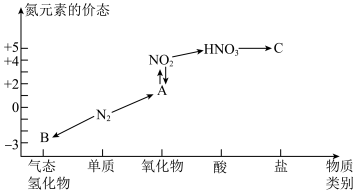
(1)B物质的电子式为:________ 。
(2) 与图中的物质C常用于检验
与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为________ 。
(3)实验室制取物质B的化学方程式为________ 。
(4)浓硝酸与木炭在加热条件下反应的化学方程式为________ 。
(5)如图装置可用于探究氯气与氨气的反应。实验时先通过三颈瓶瓶口1通入氨气,然后关闭b活塞,再通过瓶口2通入氯气。
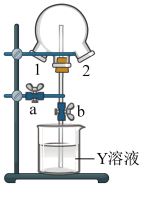
实验中三颈瓶内出现白烟并在内壁凝结成固体,发生反应的化学方程式为:________ ,请设计一个实验方案鉴定该固体中的阳离子________ 。
(6)将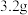 铜与
铜与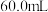 一定浓度的硝酸发生反应,铜完全溶解,产生
一定浓度的硝酸发生反应,铜完全溶解,产生 和
和 混合气体的体积为
混合气体的体积为 (标况)。待产生的气体全部释放后,向溶液加入
(标况)。待产生的气体全部释放后,向溶液加入 的
的 溶液,恰好使溶液中的
溶液,恰好使溶液中的 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为________  。
。

(1)B物质的电子式为:
(2)
 与图中的物质C常用于检验
与图中的物质C常用于检验 的存在,则C的化学式为
的存在,则C的化学式为(3)实验室制取物质B的化学方程式为
(4)浓硝酸与木炭在加热条件下反应的化学方程式为
(5)如图装置可用于探究氯气与氨气的反应。实验时先通过三颈瓶瓶口1通入氨气,然后关闭b活塞,再通过瓶口2通入氯气。

实验中三颈瓶内出现白烟并在内壁凝结成固体,发生反应的化学方程式为:
(6)将
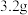 铜与
铜与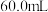 一定浓度的硝酸发生反应,铜完全溶解,产生
一定浓度的硝酸发生反应,铜完全溶解,产生 和
和 混合气体的体积为
混合气体的体积为 (标况)。待产生的气体全部释放后,向溶液加入
(标况)。待产生的气体全部释放后,向溶液加入 的
的 溶液,恰好使溶液中的
溶液,恰好使溶液中的 全部转化成沉淀,则原硝酸溶液的浓度为
全部转化成沉淀,则原硝酸溶液的浓度为 。
。
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子。
请回答下列问题:
(1)Y在元素周期表中的位置为________________ 。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是_______________ (写化学式),非金属气态氢化物还原性最强的是__________________ (写化学式)。
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有___________ (写出其中两种物质的化学式)。
(4)Z2Y2中的化学键类型是_____________________ ;Z2Y2与水反应放出气体的离子方程式为
___________________________________________ 。
(5)熔融状态下,Z的单质和FeG2能组成可充电电池(装置示意图如下),反应原理为:
2Z + FeG2 Fe + 2ZG 放电时,电池的负极材料为
Fe + 2ZG 放电时,电池的负极材料为______ ,发生____ 反应
请回答下列问题:
(1)Y在元素周期表中的位置为
(2)上述元素的最高价氧化物对应的水化物酸性最强的是
(3)Y、G的单质或两元素之间形成的化合物可作水消毒剂的有
(4)Z2Y2中的化学键类型是
(5)熔融状态下,Z的单质和FeG2能组成可充电电池(装置示意图如下),反应原理为:
2Z + FeG2
 Fe + 2ZG 放电时,电池的负极材料为
Fe + 2ZG 放电时,电池的负极材料为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】某小组同学为探究 和
和 反应的程度,进行以下实验。已知:相关物质的
反应的程度,进行以下实验。已知:相关物质的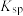 (25℃) AgCl:
(25℃) AgCl:
 :
:
(1)甲同学的实验如下:
注:经检验黑色固体为Ag。
①白色沉淀的化学式是___________ 。
②甲同学得出 氧化了
氧化了 的依据是
的依据是___________ 。
(2)乙同学为探究 和
和 反应的程度,进行实验Ⅱ。
反应的程度,进行实验Ⅱ。
a.按下图连接装置并加入药品(盐桥中的物质不参与反应),发现电压表指针偏移。
偏移的方向表明:电子由石墨经导线流向银。放置一段时间后,指针偏移减小。
b.随后向甲烧杯中逐渐加入浓 溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
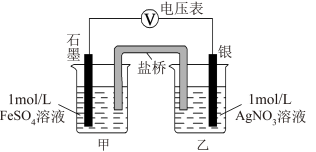
①a中甲烧杯里的电极反应式是___________ 。
②b中电压表指逆向偏移后,银为极___________ (填“正”或“负”)。
③由实验得出 和
和 反应的离子方程式是
反应的离子方程式是___________ 。
 和
和 反应的程度,进行以下实验。已知:相关物质的
反应的程度,进行以下实验。已知:相关物质的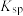 (25℃) AgCl:
(25℃) AgCl:
 :
:
(1)甲同学的实验如下:
序号 | 操作 | 现象 |
实验1 | 将2mL | 产生白色沉淀,随后有黑色固体产生 |
取上层清液,滴加KSCN溶液 | 溶液变红 |
①白色沉淀的化学式是
②甲同学得出
 氧化了
氧化了 的依据是
的依据是(2)乙同学为探究
 和
和 反应的程度,进行实验Ⅱ。
反应的程度,进行实验Ⅱ。a.按下图连接装置并加入药品(盐桥中的物质不参与反应),发现电压表指针偏移。
偏移的方向表明:电子由石墨经导线流向银。放置一段时间后,指针偏移减小。
b.随后向甲烧杯中逐渐加入浓
 溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
溶液,发现电压表指针的变化依次为:偏移减小→回到零点→逆向偏移。
①a中甲烧杯里的电极反应式是
②b中电压表指逆向偏移后,银为极
③由实验得出
 和
和 反应的离子方程式是
反应的离子方程式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】氮氧化物(NO2)是一种主要的大气污染物,必须进行处理。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其反应过程中的能量变化如下:
①△H1___ 0,△H3____ 0。(填“>”或“<”)
②N2(g)+O2(g)=2NO(g)△H=____ kJ·mol-1。
(2)利用甲烷催化还原氮氧化物。已知:
CH4(g)+4NO2(g)==4NO(g)+CO2(g)+2H2O(g)△H=-574kJ·mol-l
CH4(g)+4NO(g)==2N2(g)+CO2(g)+2H2O(g)AH=-1160 kJ·mol-l
H2O(l)=H2O(g)△H=+44kJ·mol-l
CH4与NO2反应生成N2和H2O(l)的热化学方程式为_______ 。
(3)潜艇中使用的液氮-液氧燃料电池工作原理如图所示:
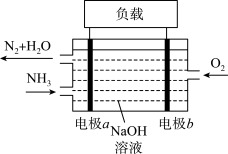
①电极a名称是______ 。
②电解质溶液中OH-离子向_____ 移动(填“电极a”或“电极b”)。
③电极b的电极反应式为_____ 。
(4)可通过NH3与NaClO反应来制得火箭燃料肼(N2H4)。该反应的化学反应方程式是_____ 。
(1)汽车发动机工作时会引发N2和O2反应生成NO,其反应过程中的能量变化如下:
| 反应 | N2(g)→2N(g) | O2(g)→2O(g) | N(g)+O(g)→NO(g) |
| 反应热 | △H1 | △H2 | △H3 |
| 热量值kJ/mol | 945 | 498 | 630 |
①△H1
②N2(g)+O2(g)=2NO(g)△H=
(2)利用甲烷催化还原氮氧化物。已知:
CH4(g)+4NO2(g)==4NO(g)+CO2(g)+2H2O(g)△H=-574kJ·mol-l
CH4(g)+4NO(g)==2N2(g)+CO2(g)+2H2O(g)AH=-1160 kJ·mol-l
H2O(l)=H2O(g)△H=+44kJ·mol-l
CH4与NO2反应生成N2和H2O(l)的热化学方程式为
(3)潜艇中使用的液氮-液氧燃料电池工作原理如图所示:

①电极a名称是
②电解质溶液中OH-离子向
③电极b的电极反应式为
(4)可通过NH3与NaClO反应来制得火箭燃料肼(N2H4)。该反应的化学反应方程式是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】硫酸亚铁可用于治疗缺铁性贫血。利用黄铜矿(CuFeS2)制备硫酸亚铁并回收铜的工艺流程如图所示:
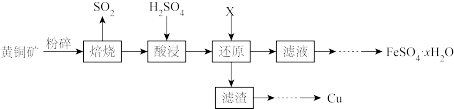
(1)①焙烧生成的SO2可用柠檬酸-柠檬酸钠溶液进行吸收,该过程采用逆流接触法进行吸收的原因是_______ 。
②还可用电化学氧化法处理SO2,同时生成H2SO4,写出SO2参与反应的电极反应式:_______ 。
(2)还原过程中加入的X为_____ (填化学式),该过程发生反应的离子方程式是_______ 。
(3)滤渣的主要成分是_______ (填化学式)。
(4)①向滤液中加入稀硫酸后经蒸发浓缩、冷却结晶、过滤可得绿矾晶体,加入稀硫酸的目的是_______ 。
②为测定产品FeSO4·xH2O中结晶水的数量,称取14g产品配制成250mL待测液,准确量取25.00mL待测液于锥形瓶中加稀硫酸酸化,用0.0500mol·L-1KMnO4标准溶液滴定至终点,重复三次,平均消耗KMnO4溶液的体积为20.00mL,则x=_______ 。

(1)①焙烧生成的SO2可用柠檬酸-柠檬酸钠溶液进行吸收,该过程采用逆流接触法进行吸收的原因是
②还可用电化学氧化法处理SO2,同时生成H2SO4,写出SO2参与反应的电极反应式:
(2)还原过程中加入的X为
(3)滤渣的主要成分是
(4)①向滤液中加入稀硫酸后经蒸发浓缩、冷却结晶、过滤可得绿矾晶体,加入稀硫酸的目的是
②为测定产品FeSO4·xH2O中结晶水的数量,称取14g产品配制成250mL待测液,准确量取25.00mL待测液于锥形瓶中加稀硫酸酸化,用0.0500mol·L-1KMnO4标准溶液滴定至终点,重复三次,平均消耗KMnO4溶液的体积为20.00mL,则x=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】铝是应用广泛的金属。以铝土矿(主要成分为 ,含
,含 和
和 等杂质)为原料制备铝的一种工艺流程如图所示:
等杂质)为原料制备铝的一种工艺流程如图所示:
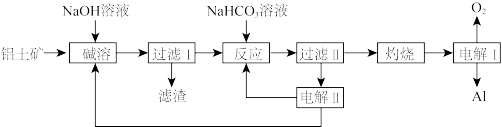
注: 在“碱溶”时转化为铝硅酸钠沉淀。
在“碱溶”时转化为铝硅酸钠沉淀。
(1)铝土矿“碱溶”时,氧化铝转化为_______ 进入溶液,提高铝土矿浸取速率的措施有_______ (任答两点)。
(2)向“过滤Ⅰ”所得滤液中加入 溶液,溶液的pH
溶液,溶液的pH_______ (填“增大”“减小”或“不变”),发生反应的离子方程式为_______ 。
(3)“电解Ⅰ”是电解熔融的 ,标准状况下每产生
,标准状况下每产生 转移的电子数为
转移的电子数为_______ 。
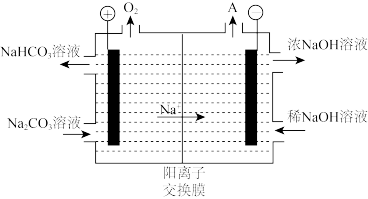
(4)“电解Ⅱ”是电解 溶液,其原理如图所示,阳极的电极反应式为
溶液,其原理如图所示,阳极的电极反应式为_______ 。
 ,含
,含 和
和 等杂质)为原料制备铝的一种工艺流程如图所示:
等杂质)为原料制备铝的一种工艺流程如图所示:
注:
 在“碱溶”时转化为铝硅酸钠沉淀。
在“碱溶”时转化为铝硅酸钠沉淀。(1)铝土矿“碱溶”时,氧化铝转化为
(2)向“过滤Ⅰ”所得滤液中加入
 溶液,溶液的pH
溶液,溶液的pH(3)“电解Ⅰ”是电解熔融的
 ,标准状况下每产生
,标准状况下每产生 转移的电子数为
转移的电子数为(4)“电解Ⅱ”是电解
 溶液,其原理如图所示,阳极的电极反应式为
溶液,其原理如图所示,阳极的电极反应式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。请回答:
I.用如图所示装置进行第一组实验。
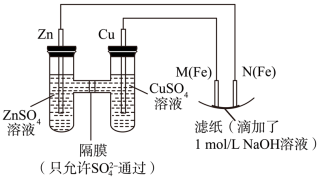
(1)N极发生反应的电极反应式为_________ .
(2)实验过程中,SO42-______ (填“从左向右”、“从右向左”或“不”)移动;
II.用如图所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色。
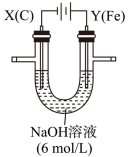
(3)电解过程中,X极区溶液的pH______ (填“增大”、“减小”或“不变”)
(4)电解过程中,Y极发生的电极反应为_____________ 和4OH-- 4e-= 2H2O + O2↑
(5)若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少______ g
(6)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2该电池正极发生的反应的电极反应式为__________
I.用如图所示装置进行第一组实验。

(1)N极发生反应的电极反应式为
(2)实验过程中,SO42-
II.用如图所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO42-)在溶液中呈紫红色。

(3)电解过程中,X极区溶液的pH
(4)电解过程中,Y极发生的电极反应为
(5)若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少
(6)在碱性锌电池中,用高铁酸钾作为正极材料,电池反应为:2K2FeO4+3Zn═Fe2O3+ZnO+2K2ZnO2该电池正极发生的反应的电极反应式为
您最近一年使用:0次
【推荐1】煤的洁净技术(包括固硫技术和脱硫技术两类)可有效降低燃煤废气中 的含量,已成为我国解决环境问题的主导技术之一、
的含量,已成为我国解决环境问题的主导技术之一、
Ⅰ.固硫技术:通过加入固硫剂,将硫元素以固体形式留在煤燃烧的残渣中。生石灰是常用的固硫剂,固硫过程中涉及的部分反应如下:
①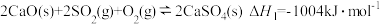
②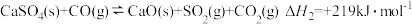
(1)表示 燃烧热的热化学方程式是
燃烧热的热化学方程式是___________ 。
(2)由上述两个反应可知,在煤燃烧过程中要提高固硫率(燃烧残渣中硫元素的质量占燃煤中硫元素总质量的百分比),可采用的方法是___________ 。
(3)某温度下,在一个恒容密闭容器中加入 和
和 ,若只发生反应②,测得如下数据:
,若只发生反应②,测得如下数据:
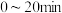 内
内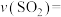
___________ ,此条件下该反应的平衡常数为___________  。
。
(4)实际生产中常用石灰石代替生石灰,石灰石吸收热量分解为生石灰,即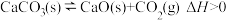 。800℃下,在一个密闭容器中加入一定量的
。800℃下,在一个密闭容器中加入一定量的 进行该反应,
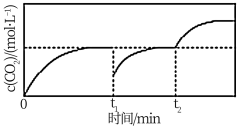
进行该反应, 气体的浓度变化如图所示,
气体的浓度变化如图所示, 和与
和与 时分别改变一个条件,则改变的条件依次是
时分别改变一个条件,则改变的条件依次是___________ 和___________ 。
Ⅱ.除去燃煤产生的废气中的 的过程如图所示。
的过程如图所示。
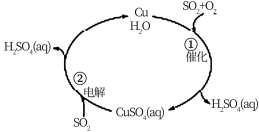
(5)过程①是 的部分催化氧化反应,若参加反应的
的部分催化氧化反应,若参加反应的 和
和 的体积比为4∶3,则反应的化学方程式为
的体积比为4∶3,则反应的化学方程式为___________ 。
(6)过程②利用电化学装置吸收另一部分 ,使得
,使得 再生,该过程中阳极的电极反应式为
再生,该过程中阳极的电极反应式为___________ 。若此过程中除去含5%(体积分数)的 的废气
的废气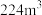 (标准状况),则需要的电量为
(标准状况),则需要的电量为___________ C(一个电子的电量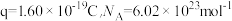 )。
)。
 的含量,已成为我国解决环境问题的主导技术之一、
的含量,已成为我国解决环境问题的主导技术之一、Ⅰ.固硫技术:通过加入固硫剂,将硫元素以固体形式留在煤燃烧的残渣中。生石灰是常用的固硫剂,固硫过程中涉及的部分反应如下:
①
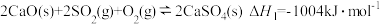
②
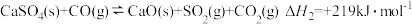
(1)表示
 燃烧热的热化学方程式是
燃烧热的热化学方程式是(2)由上述两个反应可知,在煤燃烧过程中要提高固硫率(燃烧残渣中硫元素的质量占燃煤中硫元素总质量的百分比),可采用的方法是
(3)某温度下,在一个恒容密闭容器中加入
 和
和 ,若只发生反应②,测得如下数据:
,若只发生反应②,测得如下数据: | 0 | 10 | 20 | 30 | 40 |
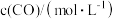 | 2 | 1.5 | 1.1 | 0.8 | 0.8 |
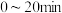 内
内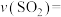
 。
。(4)实际生产中常用石灰石代替生石灰,石灰石吸收热量分解为生石灰,即
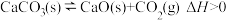 。800℃下,在一个密闭容器中加入一定量的
。800℃下,在一个密闭容器中加入一定量的 进行该反应,
进行该反应, 气体的浓度变化如图所示,
气体的浓度变化如图所示, 和与
和与 时分别改变一个条件,则改变的条件依次是
时分别改变一个条件,则改变的条件依次是
Ⅱ.除去燃煤产生的废气中的
 的过程如图所示。
的过程如图所示。
(5)过程①是
 的部分催化氧化反应,若参加反应的
的部分催化氧化反应,若参加反应的 和
和 的体积比为4∶3,则反应的化学方程式为
的体积比为4∶3,则反应的化学方程式为(6)过程②利用电化学装置吸收另一部分
 ,使得
,使得 再生,该过程中阳极的电极反应式为
再生,该过程中阳极的电极反应式为 的废气
的废气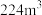 (标准状况),则需要的电量为
(标准状况),则需要的电量为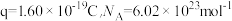 )。
)。
您最近一年使用:0次
【推荐2】工业上利用废镍催化剂(主要成分为Ni,还含有一定量的Zn、Fe、SiO2、CaO)制备草酸镍晶体(NiC2O4·2H2O)的流程如下:
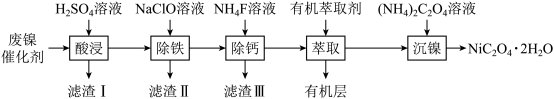
(1)NiC2O4·2H2O中C的化合价是___ 。既能加快“酸浸”反应速率又能提高“酸浸”原料利用率的操作措施为___ 。
(2)“滤渣Ⅰ”的主要成分是___ 。
(3)在隔绝空气的条件下,高温煅烧无水NiC2O4得到Ni2O3和两种含碳元素的气体,该反应的化学方程式是___ 。
(4)高能锂离子电池的总反应为2Li+FeS=Fe+Li2S。用该电池作电源电解含镍酸性废水回收Ni的装置如图(图中X、Y为电极,LiPF6·SO(CH3)2为电解质)。
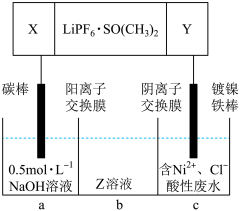
①电极X的反应材料是___ (填化学式);中间隔室b可以得到的主要物质Z是___ (填化学式)。
②电解总反应的离子方程式为___ 。
已知F=96500C/mol,若电池工作tmin,维持电流强度为I A,理论回收Ni___ g(写出计算表达式即可)。

(1)NiC2O4·2H2O中C的化合价是
(2)“滤渣Ⅰ”的主要成分是
(3)在隔绝空气的条件下,高温煅烧无水NiC2O4得到Ni2O3和两种含碳元素的气体,该反应的化学方程式是
(4)高能锂离子电池的总反应为2Li+FeS=Fe+Li2S。用该电池作电源电解含镍酸性废水回收Ni的装置如图(图中X、Y为电极,LiPF6·SO(CH3)2为电解质)。

①电极X的反应材料是
②电解总反应的离子方程式为
已知F=96500C/mol,若电池工作tmin,维持电流强度为I A,理论回收Ni
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】如图所示,通电5 min后,电极5的质量增加2.16 g,请回答下列问题:
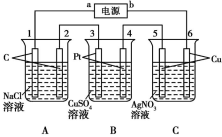
(1)a为电源的____ (填“正”或“负”)极,C池是______ 池。A池阳极的电极反应为_______ ,C池阴极的电极反应为______ 。
(2)如果B池中共收集到224 mL气体(标准状况)且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为____ 。
(3)如果A池溶液是200 mL足量的食盐水(电解过程溶液体积不变),则通电后,溶液的pH为____ 。

(1)a为电源的
(2)如果B池中共收集到224 mL气体(标准状况)且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为
(3)如果A池溶液是200 mL足量的食盐水(电解过程溶液体积不变),则通电后,溶液的pH为
您最近一年使用:0次

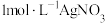 溶液加入到
溶液加入到 溶液中
溶液中

