工业上利用废镍催化剂(主要成分为Ni,还含有一定量的Zn、Fe、SiO2、CaO)制备草酸镍晶体(NiC2O4·2H2O)的流程如下:
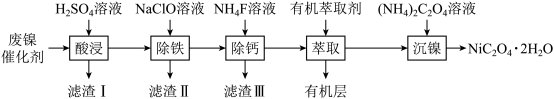
(1)NiC2O4·2H2O中C的化合价是___ 。既能加快“酸浸”反应速率又能提高“酸浸”原料利用率的操作措施为___ 。
(2)“滤渣Ⅰ”的主要成分是___ 。
(3)在隔绝空气的条件下,高温煅烧无水NiC2O4得到Ni2O3和两种含碳元素的气体,该反应的化学方程式是___ 。
(4)高能锂离子电池的总反应为2Li+FeS=Fe+Li2S。用该电池作电源电解含镍酸性废水回收Ni的装置如图(图中X、Y为电极,LiPF6·SO(CH3)2为电解质)。
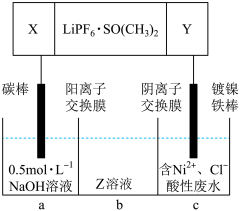
①电极X的反应材料是___ (填化学式);中间隔室b可以得到的主要物质Z是___ (填化学式)。
②电解总反应的离子方程式为___ 。
已知F=96500C/mol,若电池工作tmin,维持电流强度为I A,理论回收Ni___ g(写出计算表达式即可)。

(1)NiC2O4·2H2O中C的化合价是
(2)“滤渣Ⅰ”的主要成分是
(3)在隔绝空气的条件下,高温煅烧无水NiC2O4得到Ni2O3和两种含碳元素的气体,该反应的化学方程式是
(4)高能锂离子电池的总反应为2Li+FeS=Fe+Li2S。用该电池作电源电解含镍酸性废水回收Ni的装置如图(图中X、Y为电极,LiPF6·SO(CH3)2为电解质)。

①电极X的反应材料是
②电解总反应的离子方程式为
已知F=96500C/mol,若电池工作tmin,维持电流强度为I A,理论回收Ni
更新时间:2019-12-14 12:41:55
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】电化学在工业生产中具有重要作用。
Ⅰ.氯碱工业
如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,请按要求回答相关问题:
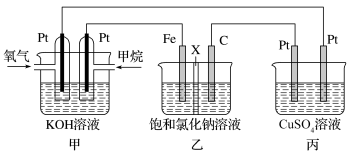
(1)甲池为___________ (填“电解池”或“原电池”);丙池中左侧Pt电极作__________ 极;乙池中X为___________ (填“阳离子交换膜”或“阴离子交换膜”)。
(2)乙池涉及的总反应的离子方程式为____________________________ 。
(3)丙池右侧Pt电极的电极反应式为______________________ 。
Ⅱ.冶金工业
一种从高炉气回收 制储氢物质
制储氢物质 的综合利用示意图如图所示,请按要求回答相关问题:
的综合利用示意图如图所示,请按要求回答相关问题:
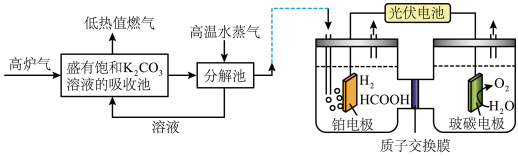
(4)某温度下,当吸收池中溶液的 时,此时该溶液中
时,此时该溶液中
__________ [已知:该温度下 ,
, ]。
]。
(5)利用电化学原理控制反应条件能将 电催化还原为
电催化还原为 ,写出铂电极上生成
,写出铂电极上生成 的电极反应式:
的电极反应式:________________________ ;电解过程中还伴随着析氢反应 ,若生成
,若生成 的电解效率为80%,生成氢气的电解效率为20%,当电路中转移
的电解效率为80%,生成氢气的电解效率为20%,当电路中转移 时,阴极室溶液的质量增加
时,阴极室溶液的质量增加_____________ g[B的电解效率 ]。
]。
Ⅰ.氯碱工业
如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,请按要求回答相关问题:

(1)甲池为
(2)乙池涉及的总反应的离子方程式为
(3)丙池右侧Pt电极的电极反应式为
Ⅱ.冶金工业
一种从高炉气回收
 制储氢物质
制储氢物质 的综合利用示意图如图所示,请按要求回答相关问题:
的综合利用示意图如图所示,请按要求回答相关问题:
(4)某温度下,当吸收池中溶液的
 时,此时该溶液中
时,此时该溶液中
 ,
, ]。
]。(5)利用电化学原理控制反应条件能将
 电催化还原为
电催化还原为 ,写出铂电极上生成
,写出铂电极上生成 的电极反应式:
的电极反应式: ,若生成
,若生成 的电解效率为80%,生成氢气的电解效率为20%,当电路中转移
的电解效率为80%,生成氢气的电解效率为20%,当电路中转移 时,阴极室溶液的质量增加
时,阴极室溶液的质量增加 ]。
]。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】本次亚运会火炬燃料甲醇是利用焦炉气中的氢气(H2)与从工业尾气中捕集的二氧化碳(CO2)合成,并由远程甲醇动力重卡提供运输保障。
Ⅰ.二氧化碳加氢制甲醇的总反应可表示为:CO2(g) + 3H2(g)=CH2OH(g) + H2O(g)
该反应一般认为通过如下步骤来实现:
①CO2(g) +H2(g)=CO(g) + H2O(g) ΔH1 = +41 kJ·mol-1
②CO (g) + 2H2(g)=CH3OH(g) ΔH2 = -90 kJ·mol-1
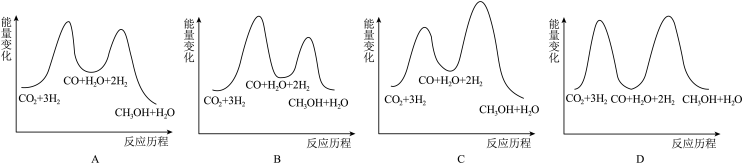
(1)总反应的 ΔH=___________ kJ·mol-1;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是___________ (填标号)。
(2)甲醇可作为燃料使用,也可用CH3OH 和O2组合形成质子交换膜燃料电池,其结构示意图如图所示:
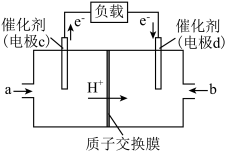
①电池总反应为2CH3OH+3O2=2CO2+4H2O,则c电极的反应方程式___________
②下图是一个电化学过程的装置示意图。 已知甲池的总反应式为 2CH3OH+3O2+4KOH=2K2CO3+6H2O
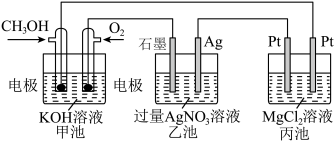
a.甲池是___________ (填“原电池”或“电解池”),通入O2的电极作___________ 极;
b.乙池是___________ (填“原电池”或“电解池”),石墨电极为___________ 极, 电极反应式为___________ 。乙池中总反应的离子方程式为___________ 。一段时间后丙池___________ 极(填“阴极”或“阳极”)附近有白色浑浊出现。
c. 当乙池中Ag极的质量增加5.40 g时, 甲池中理论上消耗O₂___________ mL(标准状况)。
(3)回收并利用CO₂一直是科研人员研究的热点。2021年,中科院天津工业生物技术研究所成果“无细胞化学酶系统催化CO₂合成淀粉”在国际学术期刊《自然》上发表。其中一步核心反应如图所示,设NA为阿伏加德罗常数的值。下列说法错误的是

(4)利用两种金属催化剂,在水溶液体系中将CO2分别转化为CO和 HCOOH的反应过程示意图如图:

下列说法正确的是___________
(5)CO用于处理大气污染物 N2O 的反应为 CO(g)+N2O(g)=CO2(g)+N2(g)。在Zn⁺作用下该反应的具体过程如图1所示,反应过程中能量变化情况如图2所示。


总反应:CO(g)+N2O(g)=CO2(g)+N2(g) ΔH=______ kJ/mol;该总反应的决速步是反应___________ (填“①”或“②”)。
Ⅰ.二氧化碳加氢制甲醇的总反应可表示为:CO2(g) + 3H2(g)=CH2OH(g) + H2O(g)
该反应一般认为通过如下步骤来实现:
①CO2(g) +H2(g)=CO(g) + H2O(g) ΔH1 = +41 kJ·mol-1
②CO (g) + 2H2(g)=CH3OH(g) ΔH2 = -90 kJ·mol-1
(1)总反应的 ΔH=

(2)甲醇可作为燃料使用,也可用CH3OH 和O2组合形成质子交换膜燃料电池,其结构示意图如图所示:

①电池总反应为2CH3OH+3O2=2CO2+4H2O,则c电极的反应方程式
②下图是一个电化学过程的装置示意图。 已知甲池的总反应式为 2CH3OH+3O2+4KOH=2K2CO3+6H2O

a.甲池是
b.乙池是
c. 当乙池中Ag极的质量增加5.40 g时, 甲池中理论上消耗O₂
(3)回收并利用CO₂一直是科研人员研究的热点。2021年,中科院天津工业生物技术研究所成果“无细胞化学酶系统催化CO₂合成淀粉”在国际学术期刊《自然》上发表。其中一步核心反应如图所示,设NA为阿伏加德罗常数的值。下列说法错误的是

| A.反应①中消耗44gCO2, 转移电子数为6NA |
| B.反应③中 cat为催化剂,实验室常用MnO2催化该反应 |
| C.30g HCHO与DHA 的混合物中所含氧原子数为2 NA |
| D.淀粉与纤维素的分子式相同,但不互为同分异构体 |

下列说法正确的是___________
| A.在转化为CO 的路径中,只涉及碳氧键的断裂和氧氢键的形成 |
| B.在转化为HCOOH的路径中,CO2被氧化为HCOOH |
| C.两个转化路径均有非极性键的形成 |
| D.上述反应过程说明催化剂具有选择性 |


总反应:CO(g)+N2O(g)=CO2(g)+N2(g) ΔH=
您最近一年使用:0次
【推荐3】绿色电源“直接二甲醚( )燃料电池”的工作原理示意图如图所示:
)燃料电池”的工作原理示意图如图所示:
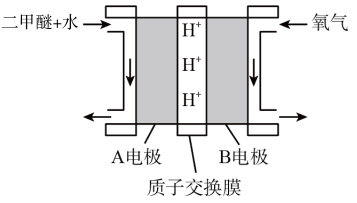
(1)正极为_______ 电极(填“A”或“B”), 移动方向为
移动方向为_______ (填“由A到B”或“由B到A”),写出A电极的电极反应式:_______ 。
(2) 和
和 是主要大气污染物,利用下图装置可同时吸收
是主要大气污染物,利用下图装置可同时吸收 和NO。
和NO。
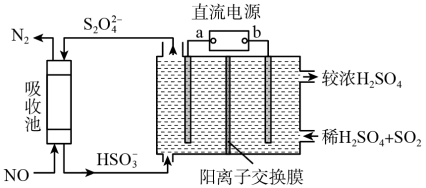
①a是直流电源的_______ 极。
②已知电解池的阴极室中溶液的pH在4~7之间,阴极的电极反应为_______ 。
(3) —空气电池是目前储电能力最高的电池。以
—空气电池是目前储电能力最高的电池。以 —空气电池为电源,用惰性电极电解硫酸铜溶液如图所示,该电池工作时的反应为
—空气电池为电源,用惰性电极电解硫酸铜溶液如图所示,该电池工作时的反应为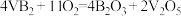 ,
, 极发生的电极反应为
极发生的电极反应为_______ 。
当外电路中通过0.04 mol电子时,B装置内共收集到0.448 L气体(标准状况),若B装置内的液体体积为200 mL(电解前后溶液体积不变),则电解前 溶液的物质的量浓度是
溶液的物质的量浓度是_______ ?(写出计算过程)
 )燃料电池”的工作原理示意图如图所示:
)燃料电池”的工作原理示意图如图所示:
(1)正极为
 移动方向为
移动方向为(2)
 和
和 是主要大气污染物,利用下图装置可同时吸收
是主要大气污染物,利用下图装置可同时吸收 和NO。
和NO。
①a是直流电源的
②已知电解池的阴极室中溶液的pH在4~7之间,阴极的电极反应为
(3)
 —空气电池是目前储电能力最高的电池。以
—空气电池是目前储电能力最高的电池。以 —空气电池为电源,用惰性电极电解硫酸铜溶液如图所示,该电池工作时的反应为
—空气电池为电源,用惰性电极电解硫酸铜溶液如图所示,该电池工作时的反应为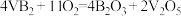 ,
, 极发生的电极反应为
极发生的电极反应为
当外电路中通过0.04 mol电子时,B装置内共收集到0.448 L气体(标准状况),若B装置内的液体体积为200 mL(电解前后溶液体积不变),则电解前
 溶液的物质的量浓度是
溶液的物质的量浓度是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性,回答下列问题:
(1)H3PO2是一元中强酸,则H3PO2(aq)中离子浓度的顺序为:__________ 。
(2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银
①H3PO2中,磷元素的化合价为_____
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为___ (填化学式);
③NaHPO2为____ (填“正盐”或“酸式盐”),其溶液显_____ (“弱酸性”,“中性”或“弱碱性”).
(3)H3PO2的工业制法是将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H3PO2),后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应的化学方程式:____________ 。
(4)H3PO2也可用电渗析法制备,“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子,阴离子通过):
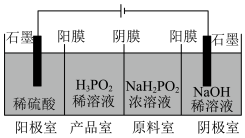
①写出阳极的电极反应式:___________ ②分析产品室可得到H3PO2的原因:__________
(5)磷酸(H3PO4) 在水溶液中各种存在形式物质的量分数δ随pH的变化曲线如图:

①向Na3PO4溶液中滴入稀盐酸后,pH从10降低到5的过程中发生的主要反应的离子方程式为______ 。
②从图中推断NaH2PO4溶液中各种微粒浓度大小关系正确的是_______ 。(填选项字母)
A、c(Na+) >c(H2PO4-) >c(H+) >c(HPO42-) >c(H3PO4)
B、c(Na+) >c(H2PO4-) >c(OH-)>c(H3PO4) >c(HPO42-)
C、c(H+)+ c(Na+)= c(OH-)+c(H2PO4-)+2c(HPO42-)+3c(PO43-)+ c(H3PO4)
D、c(Na+)= c(H2PO4-)+c(HPO42-)+c(PO43-)+ c(H3PO4)
③假设在25℃时测得0.1 mol·L-1Na3PO4溶液的pH=12,近似计算出Na3PO4第一步水解的水解常数(用Kh表示) Kh=______ mol·L-1(忽略Na3PO4第二、第三步水解,结果保留两位有效数字)。
(1)H3PO2是一元中强酸,则H3PO2(aq)中离子浓度的顺序为:
(2)H3PO2及NaH2PO2均可将溶液中的Ag+还原为银,从而可用于化学镀银
①H3PO2中,磷元素的化合价为
②利用H3PO2进行化学镀银反应中,氧化剂与还原剂的物质的量之比为4:1,则氧化产物为
③NaHPO2为
(3)H3PO2的工业制法是将白磷(P4)与Ba(OH)2溶液反应生成PH3气体和Ba(H3PO2),后者再与H2SO4反应。写出白磷与Ba(OH)2溶液反应的化学方程式:
(4)H3PO2也可用电渗析法制备,“四室电渗析法”工作原理如图所示(阳膜和阴膜分别只允许阳离子,阴离子通过):

①写出阳极的电极反应式:
(5)磷酸(H3PO4) 在水溶液中各种存在形式物质的量分数δ随pH的变化曲线如图:

①向Na3PO4溶液中滴入稀盐酸后,pH从10降低到5的过程中发生的主要反应的离子方程式为
②从图中推断NaH2PO4溶液中各种微粒浓度大小关系正确的是
A、c(Na+) >c(H2PO4-) >c(H+) >c(HPO42-) >c(H3PO4)
B、c(Na+) >c(H2PO4-) >c(OH-)>c(H3PO4) >c(HPO42-)
C、c(H+)+ c(Na+)= c(OH-)+c(H2PO4-)+2c(HPO42-)+3c(PO43-)+ c(H3PO4)
D、c(Na+)= c(H2PO4-)+c(HPO42-)+c(PO43-)+ c(H3PO4)
③假设在25℃时测得0.1 mol·L-1Na3PO4溶液的pH=12,近似计算出Na3PO4第一步水解的水解常数(用Kh表示) Kh=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】氯化钠是重要的化工原料,有着广泛的应用。
(1)图a,b、c分别为氯化钠在不同状态下的导电实验的微观示意图模型(X、Y均表示石墨电极且与直流电源连接方式相同, 表示水分子)。
表示水分子)。
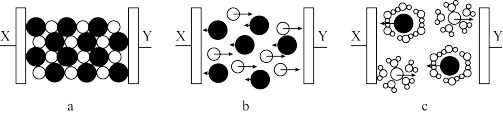
其中能观察到灯泡发亮的是_______ (填序号),原因是_______ (解释其中一个即可)。
(2)氯碱工业是化工产业的重要基础,其装置示意图如下。

①该原理的化学方程式为_______ 。
②生产过程中产生的氯酸盐副产物需要处理。已知当pH升高时, 易歧化为
易歧化为 和
和 ,下列关于
,下列关于 产生的说法中,不合理的是
产生的说法中,不合理的是_______ (填序号)。
a.阳离子交换膜破损导致 向阳极室迁移,可能产生
向阳极室迁移,可能产生
b. 在电极上放电,可能产生
在电极上放电,可能产生
c. 主要在阴极室产生
主要在阴极室产生
(1)图a,b、c分别为氯化钠在不同状态下的导电实验的微观示意图模型(X、Y均表示石墨电极且与直流电源连接方式相同,
 表示水分子)。
表示水分子)。
其中能观察到灯泡发亮的是
(2)氯碱工业是化工产业的重要基础,其装置示意图如下。

①该原理的化学方程式为
②生产过程中产生的氯酸盐副产物需要处理。已知当pH升高时,
 易歧化为
易歧化为 和
和 ,下列关于
,下列关于 产生的说法中,不合理的是
产生的说法中,不合理的是a.阳离子交换膜破损导致
 向阳极室迁移,可能产生
向阳极室迁移,可能产生
b.
 在电极上放电,可能产生
在电极上放电,可能产生
c.
 主要在阴极室产生
主要在阴极室产生
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐3】有机物A、B、C、D、E、F的转化关系如图。已知A的产量是衡量一个国家石油化工水平的标志,E具有浓郁香味,F常用于制造食物保鲜膜。回答下列问题:

(1)C中官能团的名称为______ ;A→F的反应类型为_____ 。
(2)写出B+D→E的化学方程式:_______ 。
(3)A→B的反应过程中的能量变化如图所示。

写出A→B总反应的热化学方程式:_______ 。
(4)交警对司机“酒驾”进行呼气检测的化学原理是:经硫酸酸化处理的三氧化铬(CrO3)(与重铬酸钾原理类似)硅胶检查司机呼出的气体,根据硅胶颜色的变化(硅胶中的+6价铬能被B蒸气还原为+3价铬,颜色发生变化)判断司机是否饮酒,写出K2Cr2O7的酸性溶液与B反应生成D的离子方程式:______ 。
(5)研究发现,在酸性B燃料电池中加入硝酸,可使电池持续大电流放电,其工作原理如图所示:
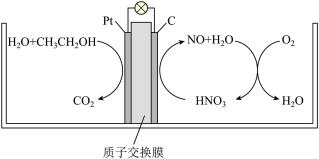
则硝酸的作用为______ ,负极电极反应式为______ 。

(1)C中官能团的名称为
(2)写出B+D→E的化学方程式:
(3)A→B的反应过程中的能量变化如图所示。

写出A→B总反应的热化学方程式:
(4)交警对司机“酒驾”进行呼气检测的化学原理是:经硫酸酸化处理的三氧化铬(CrO3)(与重铬酸钾原理类似)硅胶检查司机呼出的气体,根据硅胶颜色的变化(硅胶中的+6价铬能被B蒸气还原为+3价铬,颜色发生变化)判断司机是否饮酒,写出K2Cr2O7的酸性溶液与B反应生成D的离子方程式:
(5)研究发现,在酸性B燃料电池中加入硝酸,可使电池持续大电流放电,其工作原理如图所示:

则硝酸的作用为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】如图所示,通电5 min后,电极5的质量增加2.16 g,请回答下列问题:
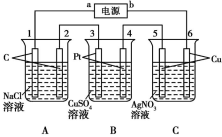
(1)a为电源的____ (填“正”或“负”)极,C池是______ 池。A池阳极的电极反应为_______ ,C池阴极的电极反应为______ 。
(2)如果B池中共收集到224 mL气体(标准状况)且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为____ 。
(3)如果A池溶液是200 mL足量的食盐水(电解过程溶液体积不变),则通电后,溶液的pH为____ 。

(1)a为电源的
(2)如果B池中共收集到224 mL气体(标准状况)且溶液体积为200 mL(设电解过程中溶液体积不变),则通电前溶液中Cu2+的物质的量浓度为
(3)如果A池溶液是200 mL足量的食盐水(电解过程溶液体积不变),则通电后,溶液的pH为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】为了探究原电池和电解池的工作原理,某研究性学习小组分别用如图所示的装置进行实验,回答下列问题。
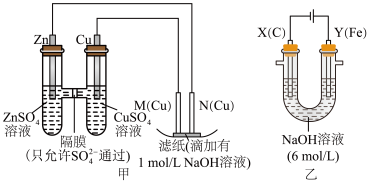
Ⅰ.用甲装置进行第一组实验:
(1)实验过程中,
________ (填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有___________________ 。
(2)该小组同学用乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子( )在溶液中呈紫红色。请根据实验现象及所查信息写出电解过程中Y极发生的电极反应为4OH--4e-=2H2O+O2↑和
)在溶液中呈紫红色。请根据实验现象及所查信息写出电解过程中Y极发生的电极反应为4OH--4e-=2H2O+O2↑和_________________ 。
II.某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,根据要求回答相关问题:
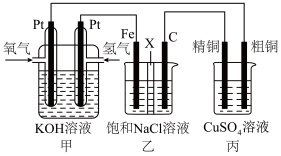
(1)若在标准状况下,甲装置有448mL氧气参加反应,则乙装置中铁电极上生成的气体在标况下体积为____
(2)若用隔膜法电解饱和食盐水生成NaClO,则X应用________ 交换膜(填“阳离子”或“阴离子”)
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将_______ (填“增大”“减 小”或“不变”)
III.以铬酸钾(K2CrO4)为原料,用电化学法制备重铬酸钾的实验装置如图.
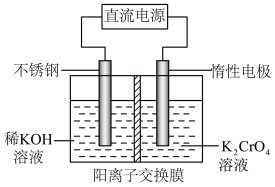
(1)不锈钢作_________ 极
(2)分析阳极区能得到重铬酸钾溶液的原因________________________________________________ 。

Ⅰ.用甲装置进行第一组实验:
(1)实验过程中,

(2)该小组同学用乙装置进行第二组实验时发现,两极均有气体产生,且Y极溶液逐渐变成紫红色,停止实验后观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根离子(
 )在溶液中呈紫红色。请根据实验现象及所查信息写出电解过程中Y极发生的电极反应为4OH--4e-=2H2O+O2↑和
)在溶液中呈紫红色。请根据实验现象及所查信息写出电解过程中Y极发生的电极反应为4OH--4e-=2H2O+O2↑和II.某同学设计一个燃料电池(如图所示),目的是探究氯碱工业原理和粗铜的精炼原理,根据要求回答相关问题:

(1)若在标准状况下,甲装置有448mL氧气参加反应,则乙装置中铁电极上生成的气体在标况下体积为
(2)若用隔膜法电解饱和食盐水生成NaClO,则X应用
(3)如果粗铜中含有锌、银等杂质,丙装置中反应一段时间,硫酸铜溶液浓度将
III.以铬酸钾(K2CrO4)为原料,用电化学法制备重铬酸钾的实验装置如图.

(1)不锈钢作
(2)分析阳极区能得到重铬酸钾溶液的原因
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
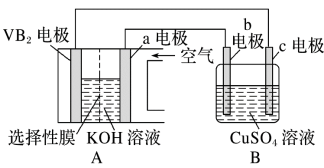
【推荐3】VB2-空气电池是目前储电能力最高的电池。以VB2-空气电池为电源,用惰性电极电解硫酸铜溶液如图所示,该电池工作时的反应为4VB2+11O2=4B2O3+2V2O5,回答下列问题:

(1)b电极发生的电极反应为_______ 。
(2)若用B装置电解精炼铜,粗铜应该做_______ 电极(填“b”或“c”),电解一段时间后,CuSO4溶液的浓度_______ (填“增大”、“减小”或“不变”)。
(3)当外电路中通过0.08 mol电子时,B装置内共收集到0.672L气体(标准状况),若B装置内的液体体积为300 mL(电解前后溶液体积不变),则电解前CuSO4溶液的物质的量浓度是_______ 。

(1)b电极发生的电极反应为
(2)若用B装置电解精炼铜,粗铜应该做
(3)当外电路中通过0.08 mol电子时,B装置内共收集到0.672L气体(标准状况),若B装置内的液体体积为300 mL(电解前后溶液体积不变),则电解前CuSO4溶液的物质的量浓度是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】回答下列问题:
(1)蒸发浓缩MgCl2溶液时,加入SOCl2的目的是______ 。
(2)醋酸亚铬[(CH3COO)2Cr•2H2O]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价铬;二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如图1所示。
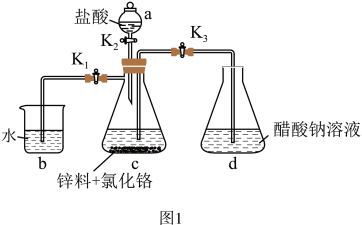
实验中所用蒸馏水均需经者沸后迅速冷却,目的是______ 。
(3)以Cl2、NaOH、(NH2)2CO(尿素)和SO2为原料可制备N2H4•H2O(水合肼)和无水Na2SO3,其主要实验流程如图2:
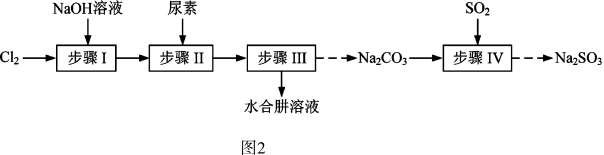
已知:①Cl2+2OH-=ClO-+Cl-+H2O是放热反应。
②N2H4•H2O沸点约118℃,具有强还原性,能与NaClO剧烈反应生成N2。
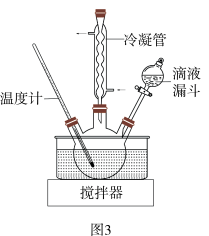
步骤II合成N2H4•H2O的装置如图3所示。NaClO碱性溶液与尿素水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应。实验中通过滴液漏斗滴加的溶液是______ ;使用冷疑管的目的是______ 。
(1)蒸发浓缩MgCl2溶液时,加入SOCl2的目的是
(2)醋酸亚铬[(CH3COO)2Cr•2H2O]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价铬;二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如图1所示。

实验中所用蒸馏水均需经者沸后迅速冷却,目的是
(3)以Cl2、NaOH、(NH2)2CO(尿素)和SO2为原料可制备N2H4•H2O(水合肼)和无水Na2SO3,其主要实验流程如图2:

已知:①Cl2+2OH-=ClO-+Cl-+H2O是放热反应。
②N2H4•H2O沸点约118℃,具有强还原性,能与NaClO剧烈反应生成N2。
步骤II合成N2H4•H2O的装置如图3所示。NaClO碱性溶液与尿素水溶液在40℃以下反应一段时间后,再迅速升温至110℃继续反应。实验中通过滴液漏斗滴加的溶液是

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
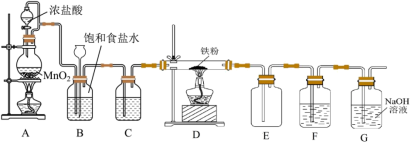
【推荐2】高铁酸钾(K2FeO4)是一种绿色高效水处理剂.某学习小组用图所示装置(夹持仪器已略去)制备KClO溶液,并通过KClO溶液与Fe(NO3)3溶液的反应制备K2FeO4.
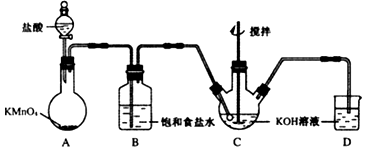
查阅资料知K2FeO4的部分性质如下:
①溶于水、微溶于浓KOH溶液
②在0℃~5℃、强碱性溶液中比较稳定
③Fe3+和Fe(OH)3催化作用下发生分解
④酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2.
请回答下列问题:
(1)仪器C和D中都盛有KOH溶液,其中C中KOH溶液的作用是__ .
(2)Cl2与KOH的浓溶液在较高温度下反应生成KClO3.为保证反应生成KClO,需要将反应温度控制在0~5℃下进行,在不改变KOH溶液浓度的前提下,实验中可以采取的措施是__ .
(3)在搅拌下,将Fe(NO3)3饱和溶液缓慢滴加到KClO饱和溶液中即可制取K2FeO4,写出该反应的化学方程式__ .
(4)制得的粗产品中含有Fe(OH)3、KCl等杂质.
提纯方案:
将一定量的K2FeO4粗产品溶于冷的3mol/L KOH溶液中,用砂芯漏斗(硬质高硼玻璃)过滤,将滤液置于冰水浴中,向滤液中加入饱和KOH溶液,搅拌、静置,再用砂芯漏斗过滤,晶体用适量乙醇洗涤2~3次后,在真空干燥箱中干燥.
第一次和第二次过滤得到的固体分别对应的是(填化学式)__ 、__ ,过滤时不用普通漏斗而采用砂芯漏斗的原因是(用离子方程式说明)__ .

查阅资料知K2FeO4的部分性质如下:
①溶于水、微溶于浓KOH溶液
②在0℃~5℃、强碱性溶液中比较稳定
③Fe3+和Fe(OH)3催化作用下发生分解
④酸性至弱碱性条件下,能与水反应生成Fe(OH)3和O2.
请回答下列问题:
(1)仪器C和D中都盛有KOH溶液,其中C中KOH溶液的作用是
(2)Cl2与KOH的浓溶液在较高温度下反应生成KClO3.为保证反应生成KClO,需要将反应温度控制在0~5℃下进行,在不改变KOH溶液浓度的前提下,实验中可以采取的措施是
(3)在搅拌下,将Fe(NO3)3饱和溶液缓慢滴加到KClO饱和溶液中即可制取K2FeO4,写出该反应的化学方程式
(4)制得的粗产品中含有Fe(OH)3、KCl等杂质.
提纯方案:
将一定量的K2FeO4粗产品溶于冷的3mol/L KOH溶液中,用砂芯漏斗(硬质高硼玻璃)过滤,将滤液置于冰水浴中,向滤液中加入饱和KOH溶液,搅拌、静置,再用砂芯漏斗过滤,晶体用适量乙醇洗涤2~3次后,在真空干燥箱中干燥.
第一次和第二次过滤得到的固体分别对应的是(填化学式)
您最近一年使用:0次

 。已知
。已知