现有150mLNH4Cl-Na2SO4混合溶液,总质量为185g,其中有30gNH4Cl、40gNa2SO4,欲对其进行处理以得到NH4Cl。已知一些物质的溶解度(g/100gH2O)如下:
*溶解度数据按100克水中溶解Na2SO4的克数计。下列说法正确的是
| 温度/°C | 0 | 10 | 20 | 30 | 32.4 | 40 | 60 | 90 | 100 |
| NH4Cl | 29.7 | 33.3 | 37.2 | 41.4 | 45.8 | 55.2 | 71.3 | 77.3 | |
| Na2SO4·10H2O* | 4.9 | 9.1 | 19.5 | 41.0 | |||||
| Na2SO4 | 48.8 | 45.3 | 42.7 | 42.5 | |||||
| NaCl | 35.7 | 35.8 | 36.0 | 36.2 | 36.5 | 37.3 | 38.6 | 39.2 | |
| (NH4)2SO4 | 70.6 | 73.0 | 75.4 | 78.0 | 81.0 | 88.0 | 99.2 | 103.3 |
| A.若在90°C左右加热,将溶液蒸发浓缩至100mL,此时会析出5.8gNa2SO4,和6.4gNaCl |
| B.若在90°C左右加热,将溶液蒸发浓缩至70mL,此时会析出10.1gNa2SO4、5.0gNH4Cl和15.8gNaCl |
| C.在90°C左右蒸发浓缩时应控制溶液为80mL,趁热过滤分离析出的Na2SO4,然后将滤液冷却结晶,在35°C左右过滤即可得到较纯净的NH4Cl |
| D.可将混合溶液冷却至0~10°C,充分析出Na2SO4·10H2O过滤分离,然后对滤液进行加热蒸发浓缩,控制好浓缩程度,冷却结晶,在35°C左右过滤即可到较纯净的NH4Cl |
2018高二·广东·竞赛 查看更多[1]
更新时间:2021-08-01 12:15:15
|
相似题推荐
【推荐1】国家速滑馆又称为“冰丝带”,所用的碲化镉(CdTe)发电玻璃被誉为“挂在墙上的油田”。一种以镉废渣(含CdO及少量ZnO、CuO、MnO、FeO杂质)为原料制备镉的工艺流程如图:

已知:部分阳离子以氢氧化物形式沉淀时溶液的PH
下列说法错误的是

 |  |  | |
| 开始沉淀 | 2.7 | 6.3 | 3.8 |
| 完全沉淀 | 3.2 | 8.3 | 5.0 |
下列说法错误的是
A.调节 目的主要是除去Cu元素 目的主要是除去Cu元素 |
B.“滤渣2”主要成分为 |
C.“置换”后滤液溶质主要成分是 |
D.“熔炼”过程利用Cd与 的密度差异可以将二者分离 的密度差异可以将二者分离 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
【推荐2】下列实验方案能达到实验目的的是
实验方案 | 实验目的 | |
A | 向 的 的 溶液中加入浓NaOH溶液,振荡、静置、分液,向水层中加入 溶液中加入浓NaOH溶液,振荡、静置、分液,向水层中加入 溶液,过滤 溶液,过滤 | 从 的 的 溶液中提取 溶液中提取 |
B | 向工业食盐中加入酸性 溶液 溶液 | 检验是否含有 |
C | 将含少量 的NaCl固体溶于水,蒸发浓缩至有晶膜析出,冷却结晶后过滤 的NaCl固体溶于水,蒸发浓缩至有晶膜析出,冷却结晶后过滤 | 除去NaCl中的 |
D | 室温下,用pH计分别测定 、 、 醋酸溶液的pH 醋酸溶液的pH | 测定弱电解质浓度大小与电离程度的关系 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐3】下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 除去碳酸钠固体中碳酸氢钠 | 将固体放置在坩埚中加热,一段时间后,在干燥器中冷却、称量整个坩埚与固体的质量为 ,再次加热、冷却、称量质量为 ,再次加热、冷却、称量质量为 | 若 ,则说明杂质已除尽 ,则说明杂质已除尽 |
| B | 检验苯中的苯酚 | 取少量样品,加入适量的浓溴水,观察现象 | 滴加溴水后,若未出现白色沉淀,则说明苯中不存在苯酚 |
| C | 探究铁与水蒸气反应后固体物质 | 取少量固体粉末,用磁铁吸引,观察现象 | 若磁铁能吸引,则固体物质为 |
| D | 检验含氟化钠的牙膏中的 | 向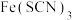 稀溶液中加过量含氟牙膏的浸泡液 稀溶液中加过量含氟牙膏的浸泡液 | 血红色褪去说明含 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐1】石灰氮是由Ca、N、C等三种元素组成的盐,其含钙、碳的质量分数分别为50%、l5%。①石灰氮完全水解的产物是A和B,其中B可方便地制成一种氮肥;②A在高温下分解生成C和D,通常状况下,C为气体;③B的催化氧化产物为E和F;④E遇到D生成唯一产物G,G与C反应重新生成A和E;⑤F再被氧气氧化后的产物遇到E可制备常用的一种强酸H;⑥B、C、E混合反应生成一种常用的氮肥I。以下有关叙述中正确的是
| A.石灰氮是化学式为Ca(CN)2 |
| B.②、⑤、⑥为有关工业生产过程的反应原理 |
| C.1molB经过催化氧化生成E和F的过程中有3mol电子发生转移 |
| D.足量B和C与饱和氯化钠溶液反应可以制得发酵粉的一种主要成分 |
您最近一年使用:0次
多选题
|
较难
(0.4)
解题方法
【推荐2】某工厂利用FeCl3溶液腐蚀镀有铜的绝缘板生产电路板,一实验小组对该厂生产电路后所得的废液进行分析。取50.0mL废液,向其中加入0.64gCu,金属铜全部溶解。另取50.0mL废液,向其中加入足量的AgNO3,析出沉淀43.05g,下列说法正确的是
| A.原废液中含有的金属阳离子只有Fe2+和Cu2+ |
| B.该工厂原来使用的FeCl3溶液的物质的量浓度约为2mol/L |
| C.若向500mL废液中加入足量的稀HNO3溶液,在标况下产生NO气体4.48L,则原废液中Fe2+和Cu2+的物质的量浓度之比为2:1 |
| D.可以使用硫氰化钾溶液检验该废液中是否含有Fe2+ |
您最近一年使用:0次




