HN3(叠氮酸)是一种易爆炸的油状物,在水中稳定,是一种弱酸。分子中N的化合价是___________ ,HN3与KOH反应的方程式是___________ 。HN3受热时反应的方程式是___________ ,在水溶液中的电离方程式是___________ 。H3N的氧化性与HNO3相似,请完成下列方程式Cu +3HN3=___________ + N2 +NH3
更新时间:2021-08-03 18:06:41
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】物质的量是宏观量与微观量相互联系的桥梁,回答下列问题。
(1)1mol NH 中含
中含___________ 个电子;34g OH- 中含___________ mol质子。
(2)等质量的O2和O3所含分子个数比为___________ 。等温等压下,等体积的O2和O3所含原子个数比为___________ ,质量比为___________ 。
(3)已知17g H2R中含1mol H,则R的摩尔质量为___________ 。
(4)酸性条件下,含I-的卤水发生如下反应。配平方程式并回答下列问题。__________________________________________________________
该反应当有1 I-参与反应时,转移了
I-参与反应时,转移了___________  电子,在标准状况下产生气体的体积是
电子,在标准状况下产生气体的体积是___________ L。
(1)1mol NH
 中含
中含(2)等质量的O2和O3所含分子个数比为
(3)已知17g H2R中含1mol H,则R的摩尔质量为
(4)酸性条件下,含I-的卤水发生如下反应。配平方程式并回答下列问题。
该反应当有1
 I-参与反应时,转移了
I-参与反应时,转移了 电子,在标准状况下产生气体的体积是
电子,在标准状况下产生气体的体积是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硫元素是动植物生长不可缺少的元素,广泛存在于自然界中。
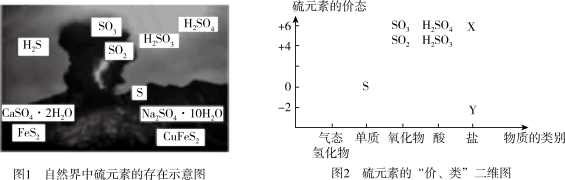
(1)从图1中选择符合图2要求的X、Y代表的物质:X_______ ,Y_______ 。
(2)硫酸是重要的化工原料,查阅资料,工业制硫酸的过程如图:
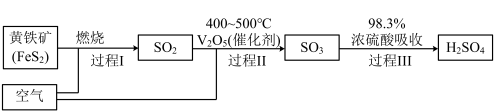
①上述过程中,发生氧化还原反应的是_______ (填“Ⅰ”、“Ⅱ”或“Ⅲ”)。
②下列对浓硫酸的叙述不正确的是_______ (填字母)。
a.常温下,浓硫酸与铁、铝不反应,所以铁质、铝质容器能盛放浓硫酸
b.浓硫酸和铜片加热既表现出酸性,又表现出氧化性
c.浓硫酸与亚硫酸钠反应制取SO2时,浓硫酸表现出强氧化性
d.过量的锌和浓硫酸反应,产生的气体含有SO2和H2
(3)铜跟浓硫酸反应的化学方程式:_______ ,被还原的元素是_______ 。

(1)从图1中选择符合图2要求的X、Y代表的物质:X
(2)硫酸是重要的化工原料,查阅资料,工业制硫酸的过程如图:

①上述过程中,发生氧化还原反应的是
②下列对浓硫酸的叙述不正确的是
a.常温下,浓硫酸与铁、铝不反应,所以铁质、铝质容器能盛放浓硫酸
b.浓硫酸和铜片加热既表现出酸性,又表现出氧化性
c.浓硫酸与亚硫酸钠反应制取SO2时,浓硫酸表现出强氧化性
d.过量的锌和浓硫酸反应,产生的气体含有SO2和H2
(3)铜跟浓硫酸反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】磷及其化合物在工农业生产中具有重要用途。回答下列问题:
(1)提纯白磷样品(含惰性杂质)的流程如图1所示。过程I中,被还原的元素是_______ (填元素符号),过程III的化学方程式为_______ 。

(2)磷酸钒锂/碳复合材料[Li3V2(PO4)3/C]是一种十分具有商业潜力的电极材料,其制备流程如图2:
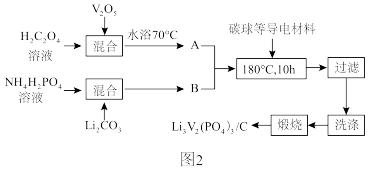
①A的主要成分为V2(C2O4)3,H2C2O4溶液与V2O5反应生成A的化学方程式为_______ 。
②流程中加入碳球的作用是_______ 。
③已知常温下,Li2CO3微溶于水,LiHCO3可溶于水。工业级Li2CO3中含有少量难溶于水且与CO2不反应的杂质。提纯工业级Li2CO3的实验方案是:将工业级Li2CO3与水混合,_______ ,得到LiHCO3溶液;控温加热使LiHCO3分解形成Li2CO3沉淀,再过滤、洗涤、干燥,得到Li2CO3纯品。“洗涤”时用乙醇而不用水的目的是_______ 。
④锂离子电池是一种二次电池。若用LixC6和Li3V2(PO4)3/C作电极,放电时的电池总反应为LixC6+Li3-xV2(PO4)3=Li3V2(PO4)3+C6。电池放电时,正极的电极反应式为_______ 。
(1)提纯白磷样品(含惰性杂质)的流程如图1所示。过程I中,被还原的元素是

(2)磷酸钒锂/碳复合材料[Li3V2(PO4)3/C]是一种十分具有商业潜力的电极材料,其制备流程如图2:

①A的主要成分为V2(C2O4)3,H2C2O4溶液与V2O5反应生成A的化学方程式为
②流程中加入碳球的作用是
③已知常温下,Li2CO3微溶于水,LiHCO3可溶于水。工业级Li2CO3中含有少量难溶于水且与CO2不反应的杂质。提纯工业级Li2CO3的实验方案是:将工业级Li2CO3与水混合,
④锂离子电池是一种二次电池。若用LixC6和Li3V2(PO4)3/C作电极,放电时的电池总反应为LixC6+Li3-xV2(PO4)3=Li3V2(PO4)3+C6。电池放电时,正极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题
(1) 溶于水的电离方程式为
溶于水的电离方程式为___________ 。
(2)向 溶液中加水稀释时,电离平衡向
溶液中加水稀释时,电离平衡向___________ (填“右”或“左”)移动,导电能力___________ 。
(3)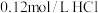 溶液与
溶液与 的
的 溶液等体积混合(设混合后溶液体积的微小变化忽略不计),混合溶液的
溶液等体积混合(设混合后溶液体积的微小变化忽略不计),混合溶液的
___________ 。
(4)某温度下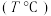 时,水的离子积为
时,水的离子积为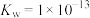 ,若将此温度下
,若将此温度下 的苛性钠溶液
的苛性钠溶液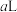 与
与 的稀硫酸
的稀硫酸 (设混合后溶液体积的微小变化忽略不计),若所得溶液为中性,则
(设混合后溶液体积的微小变化忽略不计),若所得溶液为中性,则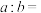
___________ ,若所得溶液的 ,则
,则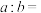
___________ 。
(1)
 溶于水的电离方程式为
溶于水的电离方程式为(2)向
 溶液中加水稀释时,电离平衡向
溶液中加水稀释时,电离平衡向(3)
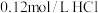 溶液与
溶液与 的
的 溶液等体积混合(设混合后溶液体积的微小变化忽略不计),混合溶液的
溶液等体积混合(设混合后溶液体积的微小变化忽略不计),混合溶液的
(4)某温度下
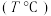 时,水的离子积为
时,水的离子积为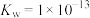 ,若将此温度下
,若将此温度下 的苛性钠溶液
的苛性钠溶液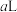 与
与 的稀硫酸
的稀硫酸 (设混合后溶液体积的微小变化忽略不计),若所得溶液为中性,则
(设混合后溶液体积的微小变化忽略不计),若所得溶液为中性,则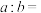
 ,则
,则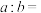
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)H2O2的水溶液为二元弱酸,科学家对H2O2结构的认识经历了较为漫长的过程,最初他们提出了两种观点:
a. (式中O→O表示共用电子对由前一个氧原子提供)和b.H—O—O—H
(式中O→O表示共用电子对由前一个氧原子提供)和b.H—O—O—H
①请用电子式表示b的结构________________________________________ 。
②写出H2O2在水溶液中的电离方程式_______________________________________ 。
(2)①用单质碘和氯酸钾可以制得碘酸钾,其中涉及的一个反应为:
I2+ KClO3+ H2O → KH(IO3)2+ KCl + Cl2↑.因此有人认为I2的氧化性强于氯气,你
______ (填“同意”或“不同意”)该观点,理由是___________________________ 。
②用电化学方法也可以制碘酸钾.原理是以石墨为阳极,不锈钢为阴极,以碘化钾溶液为电解质溶液,在一定电流和温度下进行电解(同时不断搅拌电解质溶液)其电解总反应式为: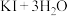

 试写出阳极的电极反应式
试写出阳极的电极反应式_______________________ 。
a.
 (式中O→O表示共用电子对由前一个氧原子提供)和b.H—O—O—H
(式中O→O表示共用电子对由前一个氧原子提供)和b.H—O—O—H①请用电子式表示b的结构
②写出H2O2在水溶液中的电离方程式
(2)①用单质碘和氯酸钾可以制得碘酸钾,其中涉及的一个反应为:
I2+ KClO3+ H2O → KH(IO3)2+ KCl + Cl2↑.因此有人认为I2的氧化性强于氯气,你
②用电化学方法也可以制碘酸钾.原理是以石墨为阳极,不锈钢为阴极,以碘化钾溶液为电解质溶液,在一定电流和温度下进行电解(同时不断搅拌电解质溶液)其电解总反应式为:
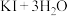

 试写出阳极的电极反应式
试写出阳极的电极反应式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】人体内尿酸(HUr)含量偏高,关节滑液中产生尿酸钠晶体(NaUr)会引发痛风,NaUr(s) Na+(aq)+Ur−(aq),∆H>0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
Na+(aq)+Ur−(aq),∆H>0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
已知:
①37℃时,Ka(HUr)=4×10−6,Kw=2.4×10−14,Ksp(NaUr)=6.4×10−5
②37℃时,模拟关节滑液pH=7.4,c(Ur-)=4.6×10−4mol∙L−1
(1)尿酸电离方程式为___________
(2)37℃时,向HUr溶液中加入NaOH溶液配制“模拟关节滑液”,溶液当中c(Na+)___________ c(Ur−)(填“>”、“<”或“=”),写出溶液中电荷守恒的等式:___________ 。
(3)37℃时,向模拟关节滑液中加入NaCl(s)至c(Na+)=0.2mol∙L−1时,通过计算溶液Q=c(Na+)∙c(Ur-)=___________ 。判断是否有NaUr晶体析出___________ (填是/否)。
(4)对于尿酸偏高的人群,下列建议正确的是___________ 。
a.加强锻炼,注意关节保暖
b.多饮酒,利用乙醇杀菌消毒
c.多喝水,饮食宜少盐、少脂
d.减少摄入易代谢出尿酸的食物
 Na+(aq)+Ur−(aq),∆H>0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:
Na+(aq)+Ur−(aq),∆H>0。某课题组配制“模拟关节滑液”进行研究,回答下列问题:已知:
①37℃时,Ka(HUr)=4×10−6,Kw=2.4×10−14,Ksp(NaUr)=6.4×10−5
②37℃时,模拟关节滑液pH=7.4,c(Ur-)=4.6×10−4mol∙L−1
(1)尿酸电离方程式为
(2)37℃时,向HUr溶液中加入NaOH溶液配制“模拟关节滑液”,溶液当中c(Na+)
(3)37℃时,向模拟关节滑液中加入NaCl(s)至c(Na+)=0.2mol∙L−1时,通过计算溶液Q=c(Na+)∙c(Ur-)=
(4)对于尿酸偏高的人群,下列建议正确的是
a.加强锻炼,注意关节保暖
b.多饮酒,利用乙醇杀菌消毒
c.多喝水,饮食宜少盐、少脂
d.减少摄入易代谢出尿酸的食物
您最近一年使用:0次



