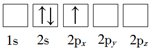
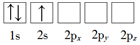
对于基态Cr原子,下列叙述正确的是
| A.轨道处于半充满时体系总能量低,核外电子排布应为[Ar]3d54s1 |
| B.4s电子能量较高,总是在比3d电子离核更远的地方运动 |
| C.电负性比钾高,原子对键合电子的吸引力比钾大 |
2021高三·全国·专题练习 查看更多[2]
更新时间:2021-08-09 19:14:12
|
相似题推荐
多选题
|
适中
(0.65)
解题方法
【推荐1】甲、乙、丙、丁、戊均为短周期主族元素,甲的原子半径是第二周期中最小的;乙的单质能跟冷水剧烈反应产生氢气;丙原子核外p电子比s电子多5个;丁和丙在同周期,丁的最高价为+4价;戊的单质是气体,其密度介于H2和O2的密度之间。下列推断错误的是
| A.甲的非金属性最强 |
| B.戊的最高价氧化物的水化物酸性最强 |
| C.原子半径大小为:乙>丙>甲 |
| D.乙分别与甲、丙形成晶体M、N的熔点大小为:M<N |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】下列各组表述中,两个微粒一定不属于同种元素原子的是( )
| A.3p能级有一个未成对电子的基态原子和核外电子排布为1s22s22p63s23p1的原子 |
| B.M层全充满而N层为4s2的原子和核外电子排布为1s22s22p63s23p64s2的原子 |
C.最外层电子数是核外电子总数的 的原子和价电子排布为3s23p5的原子 的原子和价电子排布为3s23p5的原子 |
| D.2p能级有一个空轨道的基态原子和原子的价电子排布为2s22p2的原子 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】氢气作为一种很有发展前途的绿色能源,得到了日益广泛的重视。我国科学家构建的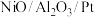 双组分催化剂(NiO的晶胞与NaCl相似),可实现氨硼烷
双组分催化剂(NiO的晶胞与NaCl相似),可实现氨硼烷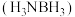 与
与 高效产
高效产 的目的,发生反应的化学方程式为
的目的,发生反应的化学方程式为 。下列说法正确的是。
。下列说法正确的是。
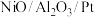 双组分催化剂(NiO的晶胞与NaCl相似),可实现氨硼烷
双组分催化剂(NiO的晶胞与NaCl相似),可实现氨硼烷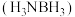 与
与 高效产
高效产 的目的,发生反应的化学方程式为
的目的,发生反应的化学方程式为 。下列说法正确的是。
。下列说法正确的是。A.NiO晶胞中与 等距最近的 等距最近的 为8 为8 |
| B.第一电离能:H<B<O<N,电负性:O>N>B>H>Al |
C.氮硼键键能: |
D.根据VSEPR模型计算, 、 、 、 、 的中心原子上的价层电子对数都是4 的中心原子上的价层电子对数都是4 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐2】已知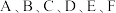 是原子序数依次增大的前四周期元素。其中
是原子序数依次增大的前四周期元素。其中 是宇宙中含量最多的元素;
是宇宙中含量最多的元素; 元素原子最高能级的不同轨道都有电子,并且自旋方向相同;
元素原子最高能级的不同轨道都有电子,并且自旋方向相同; 元素原子的价层电子排布式为
元素原子的价层电子排布式为 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子; 与
与 的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
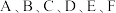 是原子序数依次增大的前四周期元素。其中
是原子序数依次增大的前四周期元素。其中 是宇宙中含量最多的元素;
是宇宙中含量最多的元素; 元素原子最高能级的不同轨道都有电子,并且自旋方向相同;
元素原子最高能级的不同轨道都有电子,并且自旋方向相同; 元素原子的价层电子排布式为
元素原子的价层电子排布式为 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子; 与
与 的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是A.A、B、C三种元素的电负性: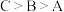 |
B.B、C、D、E四种元素的第一电离能: |
C.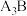 的稳定性大于 的稳定性大于 |
D. 的常见离子的核外电子排布图为 的常见离子的核外电子排布图为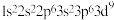 |
您最近一年使用:0次