下列各项叙述中,正确的是
| A.电负性:S>As>Se | B.键角:H2O<NH3<CH4 |
| C.沸点:HF>HCl>HBr>HI | D.离子还原性:S2->I->Br->Cl- |
更新时间:2022-09-24 20:25:50
|
相似题推荐
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知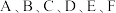 是原子序数依次增大的前四周期元素。其中
是原子序数依次增大的前四周期元素。其中 是宇宙中含量最多的元素;
是宇宙中含量最多的元素; 元素原子最高能级的不同轨道都有电子,并且自旋方向相同;
元素原子最高能级的不同轨道都有电子,并且自旋方向相同; 元素原子的价层电子排布式为
元素原子的价层电子排布式为 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子; 与
与 的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
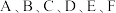 是原子序数依次增大的前四周期元素。其中
是原子序数依次增大的前四周期元素。其中 是宇宙中含量最多的元素;
是宇宙中含量最多的元素; 元素原子最高能级的不同轨道都有电子,并且自旋方向相同;
元素原子最高能级的不同轨道都有电子,并且自旋方向相同; 元素原子的价层电子排布式为
元素原子的价层电子排布式为 ;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子;
;D元素原子中只有两种形状的电子云,最外层只有一种自旋方向的电子; 与
与 的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是
的最高能层数相同,但其价层电子数等于其电子层数。F元素原子的最外层只有一个电子,其次外层内的所有轨道的电子均成对。下列说法正确的是A.A、B、C三种元素的电负性: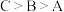 |
B.B、C、D、E四种元素的第一电离能: |
C.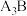 的稳定性大于 的稳定性大于 |
D. 的常见离子的核外电子排布图为 的常见离子的核外电子排布图为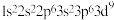 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】硫和氮是两种常见的“明星元素”,其化合物是现代无机化学研究的最为活跃的领域之一.如图是已经合成的某硫氮化合物的分子结构,下列说法错误的是
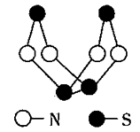

| A.该物质的分子式为SN | B.该物质的熔沸点较低 |
| C.该物质的分子中不含非极性键 | D.N的电负性比S的电负性强 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
解题方法
【推荐1】C60可用作储存氢气的材料,结构如图所示。继C60后,科学家又合成了Si60、N60,三种物质结构相似。下列有关说法正确的是
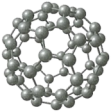

| A.C60、Si60、N60都属于分子晶体 |
| B.C60、Si60、N60分子内共用电子对数目相同 |
| C.由于N-N键键能小于N≡N键,故N60的稳定性弱于N2 |
| D.由于C-C键的键长小于Si-Si键,所以C60的熔、沸点低于Si60 |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】“点击化学”研究获得2022年诺贝尔化学奖,用该原理可制得如图含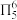 大
大 键的产物。已知杂化轨道中s成分越多,所形成的化学键越稳定。下列说法错误为是
键的产物。已知杂化轨道中s成分越多,所形成的化学键越稳定。下列说法错误为是
 大
大 键的产物。已知杂化轨道中s成分越多,所形成的化学键越稳定。下列说法错误为是
键的产物。已知杂化轨道中s成分越多,所形成的化学键越稳定。下列说法错误为是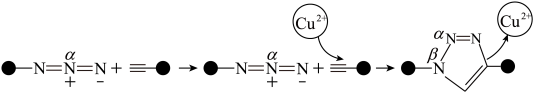
| A.铜离子增大了反应的活化能 |
| B.反应物中黑球元素的电负性强于N |
C.产物中 、 、 两位置中的N原子中, 两位置中的N原子中, 位置的N原子更容易形成配位键 位置的N原子更容易形成配位键 |
| D.反应物中氮氮键比产物中氮氮键的键长短 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐3】氨作为化工原料有多种应用。氨水配成的银氨溶液,可用于工业制镜。强碱性条件NaClO和NH3生成火箭燃料N2H4(肼),1mol液态肼完全燃烧生成N2气体和液态水放577kJ的热量。NH3和CO2反应制备尿素[CO(NH2)2],尿素在高温条件下可净化汽车尾气中的NO。下列有关说法正确的是
A.NH3中的键角小于 中的键角 中的键角 |
| B.1molNaClO可得到1molN2H4 |
| C.1mol[Ag(NH3)2]+中有2molσ键 |
| D.净化汽车尾气时氧化产物为CO2 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.标准状况下,HF呈液态,NH3呈气态,原因是HF分子间存在氢键,而NH3分子间只存在范德华力 |
| B.H2S的分解温度高于H2Se,原因是H—S键的键能大于H-Se键 |
| C.用浓氨水可以除去Mg(OH)2中的少量Cu(OH)2,原因是Cu(OH)2与NH3形成较稳定的[Cu(NH3)4]2+ |
| D.北京冬奥会采用CO2作制冷剂,原因是断裂共价键需要吸收大量的热量 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】下列对一些实验事实及其理论解释都正确的是
选项 | 实验事实 | 理论解释 |
A | Be原子的第一电离能小于B原子 | 同周期元素原子的电离能随原子序数增大而增大 |
B | CH4为正四面体形分子 | CH4分子中C为sp3杂化,键角为109°28′ |
C | 金刚石的熔点高于石墨 | 金刚石是原子晶体,石墨是分子晶体 |
D | HF的沸点高于HCl | HF分子间能形成氢键,HCl不能 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次





