回答下列问题
(1)某课外兴趣小组对H2O2的分解速率做了如下实验探究,下表是该小组探究影响H2O2分解速率因素时测得的一组数据:用10mLH2O2溶液制取150mLO2所需时间(s)
上述实验结果表明___________ 、___________ 、___________ 等因素对H2O2分解速率的影响。
(2)某温度时,在一个2L的密闭容器中,M、N、W气体的物质的量随时间的变化曲线如图所示。
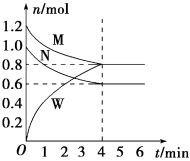
根据图中数据,回答下列问题:
①该反应的化学方程式为___________ 。
②从反应开始至4min,N的反应速率为___________ 。
(1)某课外兴趣小组对H2O2的分解速率做了如下实验探究,下表是该小组探究影响H2O2分解速率因素时测得的一组数据:用10mLH2O2溶液制取150mLO2所需时间(s)
| 项目 | 30%H2O2 | 15%H2O2 | 10%H2O2 | 5%H2O2 |
| 无催化剂、不加热 | 几乎不反应 | 几乎不反应 | 几乎不反应 | 几乎不反应 |
| 无催化剂、加热 | 360 | 480 | 540 | 720 |
| MnO2、加热 | 10 | 25 | 60 | 120 |
(2)某温度时,在一个2L的密闭容器中,M、N、W气体的物质的量随时间的变化曲线如图所示。

根据图中数据,回答下列问题:
①该反应的化学方程式为
②从反应开始至4min,N的反应速率为
更新时间:2021-08-22 00:42:49
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】Ⅰ.影响化学反应速率的因素有多种,请在横线上填入与下列各项关系最为密切的影响化学反应速率的因素(填“温度”、“浓度”、“催化剂”、“压强”、“物质本身的性质”或“固体表面积”):
(1)夏天的食品易变霉,在冬天不易发生该现象:_______ 。
(2)同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气体有快有慢:_______ 。
(3)MnO2加入双氧水中放出气泡加快:__________ 。
Ⅱ.在一定温度下,4 L密闭容器内某一反应中气体M、气体N的物质的量浓度随时间变化的曲线如图所示。
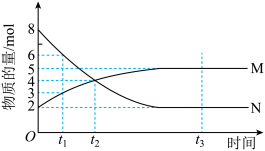
(1)比较t2时刻,正、逆反应速率大小:v(正)________ (填“>”“=”或“<”)v(逆)。
(2)若t2=2 min,反应开始至t2时刻,M的平均化学反应速率v(M)=______ mol·L-1·min-1。
(3)t1、t2、t3三个时刻中处于平衡状态的时刻为_________ (填“t1”“t2”或“t3”)。
(4)如果升高温度,则v(逆)________ (填“增大”“减小”或“不变”)。
(1)夏天的食品易变霉,在冬天不易发生该现象:
(2)同浓度不同体积的盐酸中放入同样大小的锌块和镁块,产生气体有快有慢:
(3)MnO2加入双氧水中放出气泡加快:
Ⅱ.在一定温度下,4 L密闭容器内某一反应中气体M、气体N的物质的量浓度随时间变化的曲线如图所示。

(1)比较t2时刻,正、逆反应速率大小:v(正)
(2)若t2=2 min,反应开始至t2时刻,M的平均化学反应速率v(M)=
(3)t1、t2、t3三个时刻中处于平衡状态的时刻为
(4)如果升高温度,则v(逆)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】某温度时,在一个2L的密闭容器中,A、B、C三种气体物质的浓度随时间的变化曲线如图所示。

根据图中数据,试填写下列空白:
(1)该反应的化学方程式为_______ ;
(2)从开始至2min,B的平均反应速率为_______ ;平衡时,C的物质的量为_______ ;
(3)下列叙述能说明该反应已达到化学平衡状态的是_______ (填序号);
A.A、B、C的物质的量之比为3:1:3
B.相同时间内消耗3molA,同时生成3molC
C.相同时间内消耗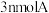 ,同时消耗
,同时消耗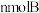
D.混合气体的总质量不随时间的变化而变化
E.B的体积分数不再发生变化
(4)在某一时刻采取下列措施能使该反应速率减小的是_______ (填序号)。
A.加催化剂
B.降低温度
C.容积不变,充入A
D.容积不变,从容器中分离出A

根据图中数据,试填写下列空白:
(1)该反应的化学方程式为
(2)从开始至2min,B的平均反应速率为
(3)下列叙述能说明该反应已达到化学平衡状态的是
A.A、B、C的物质的量之比为3:1:3
B.相同时间内消耗3molA,同时生成3molC
C.相同时间内消耗
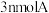 ,同时消耗
,同时消耗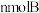
D.混合气体的总质量不随时间的变化而变化
E.B的体积分数不再发生变化
(4)在某一时刻采取下列措施能使该反应速率减小的是
A.加催化剂
B.降低温度
C.容积不变,充入A
D.容积不变,从容器中分离出A
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】化学反应速率和限度与生产、生活密切相关。
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气标准状况,实验记录如表累计值:
①哪一时间段反应速率最大__ (填0~1、1~2、2~3、3~4、4~5min)。反应开始后反应速率先增大的原因是__ 。
②求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率___ (设溶液体积不变)。
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入少量的下列溶液以减慢反应速率,你认为不可行的是__ 。
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(3)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。
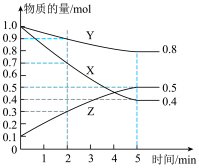
①该反应的化学方程式是__ 。
②该反应达到平衡状态的标志是__ 。
A.X、Y、Z的反应速率相等
B.X、Y的反应速率比为3:1
C.容器内气体压强保持不变
D.生成2mol Z的同时生成3mol X
(1)某学生为了探究锌与盐酸反应过程中的速率变化,在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气标准状况,实验记录如表累计值:
| 时间 | 1 | 2 | 3 | 4 | 5 |
| 氢气体积 | 100 | 240 | 464 | 576 | 620 |
①哪一时间段反应速率最大
②求3~4分钟时间段以盐酸的浓度变化来表示的该反应速率
(2)另一学生为控制反应速率防止反应过快难以测量氢气体积,他事先在盐酸中加入少量的下列溶液以减慢反应速率,你认为不可行的是
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(3)某温度下在4L密闭容器中,X、Y、Z三种气态物质的物质的量随时间变化曲线如图。

①该反应的化学方程式是
②该反应达到平衡状态的标志是
A.X、Y、Z的反应速率相等
B.X、Y的反应速率比为3:1
C.容器内气体压强保持不变
D.生成2mol Z的同时生成3mol X
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】为有效控制雾霾,各地积极采取措施改善大气质量。有效控制空气中氮氧化物、硫氧化物显得尤为重要。
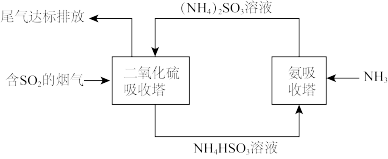
I.某企业利用下列流程综合处理工厂排放的含有 的烟气,以减少其对环境造成的污染。试回答下列问题:
的烟气,以减少其对环境造成的污染。试回答下列问题:
(1)二氧化硫吸收塔中发生反应的化学方程式为_______ 。
(2)氨吸收塔中发生反应的离子方程式为_______ 。
(3)一定条件下,通过下列反应可实现燃煤烟气中硫的回收: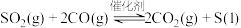 ,该反应的能量变化如图所示。
,该反应的能量变化如图所示。
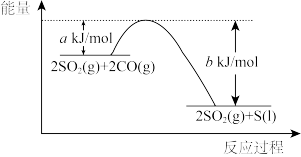
①该反应为_______ (填“放热”或“吸热”)反应。
②如果要提高该反应的反应速率,可以采取的措施是_______ (选填编号)
A.减压 B.增加 的浓度 C.升温 D.及时移出产物
的浓度 C.升温 D.及时移出产物
II.用活性炭还原法处理氮氧化物。有关反应为: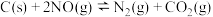 某研究小组向一个容器容积为3L且容积不变的密闭真空容器(固体试样体积忽略不计)中加入
某研究小组向一个容器容积为3L且容积不变的密闭真空容器(固体试样体积忽略不计)中加入 和足量的活性炭,在恒温(T1℃)条件下反应,测得不同时间(t)时各物质的物质的量(n)如表:
和足量的活性炭,在恒温(T1℃)条件下反应,测得不同时间(t)时各物质的物质的量(n)如表:
(4)①表中b=_______ ,计算T1℃时 内,用
内,用 浓度增加来表示该反应的平均速率
浓度增加来表示该反应的平均速率_______ 。
②下列各项能判断该反应达到平衡状态的是_______ (填序号字母)。
A.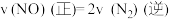 B.容器内
B.容器内 和
和 的体积比为
的体积比为
C.混合气体的平均相对分子质量保持不变 D.容器内压强保持不变

I.某企业利用下列流程综合处理工厂排放的含有
 的烟气,以减少其对环境造成的污染。试回答下列问题:
的烟气,以减少其对环境造成的污染。试回答下列问题:(1)二氧化硫吸收塔中发生反应的化学方程式为
(2)氨吸收塔中发生反应的离子方程式为
(3)一定条件下,通过下列反应可实现燃煤烟气中硫的回收:
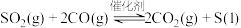 ,该反应的能量变化如图所示。
,该反应的能量变化如图所示。
①该反应为
②如果要提高该反应的反应速率,可以采取的措施是
A.减压 B.增加
 的浓度 C.升温 D.及时移出产物
的浓度 C.升温 D.及时移出产物II.用活性炭还原法处理氮氧化物。有关反应为:
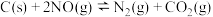 某研究小组向一个容器容积为3L且容积不变的密闭真空容器(固体试样体积忽略不计)中加入
某研究小组向一个容器容积为3L且容积不变的密闭真空容器(固体试样体积忽略不计)中加入 和足量的活性炭,在恒温(T1℃)条件下反应,测得不同时间(t)时各物质的物质的量(n)如表:
和足量的活性炭,在恒温(T1℃)条件下反应,测得不同时间(t)时各物质的物质的量(n)如表:| 时间/min | NO物质的量(mol) |  物质的量(mol) 物质的量(mol) |  物质的量(mol) 物质的量(mol) |
| 0 | 2.00 | 0 | 0 |
| 10 | 1.16 | a | a |
| 20 | b | 0.60 | 0.60 |
| 30 | b | 0.60 | 0.60 |
 内,用
内,用 浓度增加来表示该反应的平均速率
浓度增加来表示该反应的平均速率②下列各项能判断该反应达到平衡状态的是
A.
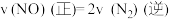 B.容器内
B.容器内 和
和 的体积比为
的体积比为
C.混合气体的平均相对分子质量保持不变 D.容器内压强保持不变
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】一定温度下,反应3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g),在一密闭容器中进行达平衡后,试回答:
Fe3O4(s)+4H2(g),在一密闭容器中进行达平衡后,试回答:
(1)增加Fe的物质的量,其正反应速率___________ 。
(A.变快 B.不变 C变慢,填字母代号)。
(2)将容器的体积缩小一半,其正反应速率___________ ,逆反应速率___________ 。
(3)若保持体积不变,充入Ar,其逆反应速率___________ 。
(4)保持压强不变,充入Ar,其正反应速率___________ 。
 Fe3O4(s)+4H2(g),在一密闭容器中进行达平衡后,试回答:
Fe3O4(s)+4H2(g),在一密闭容器中进行达平衡后,试回答:(1)增加Fe的物质的量,其正反应速率
(A.变快 B.不变 C变慢,填字母代号)。
(2)将容器的体积缩小一半,其正反应速率
(3)若保持体积不变,充入Ar,其逆反应速率
(4)保持压强不变,充入Ar,其正反应速率
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】按要求填空或计算,(1)(2)小题为判断题。
(1)蛋白质溶液中加入饱和的硫酸铵溶液有白色固体析出,这是化学变化。___________ (填“×”或“√”)
(2)合金的熔点一般比成分金属要高,硬度比成分金属要低。___________ (填“×”或“√”)
(3)加热时,浓硫酸可与碳发生反应:C+2H2SO4(浓) CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出
CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出___________ (填“吸水”、“脱水”或“氧化”)性。
(4)Na与水反应,增大水的用量:反应速率___________ (选填“加快”、“减慢”、“不变”)。
(5)某反应的反应物A浓度在5min内由6mol·L-1变成了2mol·L-1,则v(A)=___________ mol·L-1·min-1。
(1)蛋白质溶液中加入饱和的硫酸铵溶液有白色固体析出,这是化学变化。
(2)合金的熔点一般比成分金属要高,硬度比成分金属要低。
(3)加热时,浓硫酸可与碳发生反应:C+2H2SO4(浓)
 CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出
CO2↑+2SO2↑+2H2O。在该反应中,浓H2SO4表现出(4)Na与水反应,增大水的用量:反应速率
(5)某反应的反应物A浓度在5min内由6mol·L-1变成了2mol·L-1,则v(A)=
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】简要回答下列问题。
(1)NO暴露在空气中,出现红棕色的原因是________ 。
(2)将食品置于低温条件下,常常可以保存更长时间的原因是________ 。
(3)盛有浓硫酸的容器敞口放置一段时间后,硫酸浓度变小的原因是________ 。
(4)推广使用新能源汽车的目的是________ 。
(1)NO暴露在空气中,出现红棕色的原因是
(2)将食品置于低温条件下,常常可以保存更长时间的原因是
(3)盛有浓硫酸的容器敞口放置一段时间后,硫酸浓度变小的原因是
(4)推广使用新能源汽车的目的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】我校化学兴趣小组的小王同学用相同质量的锌和相同浓度的足量的稀盐酸反应得到实验数据如下表所示:
(1)该实验的目的是探究_______ (对锌和稀盐酸反应速率的影响;
(2)实验①和②表明_______ ,化学反应速率越大;
(3)能表明固体的表面积对反应速率有影响的实验编号是_______ 和_______ ;
| 实验编号 | 锌的状态 | 反应温度/℃ | 收集100mL氢气所需时间/s |
| ① | 薄片 | 15 | 180 |
| ② | 薄片 | 25 | 70 |
| ③ | 粉末 | 25 | 15 |
(1)该实验的目的是探究
(2)实验①和②表明
(3)能表明固体的表面积对反应速率有影响的实验编号是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
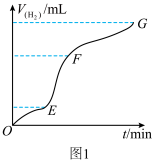
【推荐3】I.用一定质量的Zn跟足量的稀硫酸反应制氢气,请回答:
(1)实验过程如图1所示,EF段化学反应速率加快与该反应是___________ (填“放热”或“吸热”)反应有关。
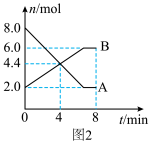
Ⅱ.某温度时,气体A、B在5 L密闭容器中反应的物质的量随时间变化的曲线如图2所示。由图中数据分析求:___________ 。
(4)反应开始至4 min时,A的平均反应速率为___________ 。
(5)4min时,正、逆反应速率的大小关系为:v(正)___________ v(逆) (填“>”、“<”或“=”)。
(6)平衡时气体A的体积分数为___________ 。
(1)实验过程如图1所示,EF段化学反应速率加快与该反应是
| A.蒸馏水 | B.NaCl溶液 | C.NaNO3固体 | D.CuSO4固体 |
Ⅱ.某温度时,气体A、B在5 L密闭容器中反应的物质的量随时间变化的曲线如图2所示。由图中数据分析求:
(4)反应开始至4 min时,A的平均反应速率为
(5)4min时,正、逆反应速率的大小关系为:v(正)
(6)平衡时气体A的体积分数为
您最近一年使用:0次
【推荐1】根据以下叙述,回答(1)~(2)小题。
大气中的臭氧层可滤除大量的紫外光,保护地球上的生物。氟利昂(如CCl2F2)可在光的作用下分解,产生Cl原子,Cl原子会对臭氧层产生长久的破坏作用,臭氧的分子式为O3。有关反应为:
O3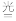 O2+O
O2+O
Cl+O3荣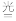 ClO+O2
ClO+O2
O+ClO=Cl+O2
总反应为2O3=3O2。
(1)在上述臭氧变成氧气的过程中,Cl原子是__ 。
A.反应物 B.生成物
C.中间产物 D.催化剂
(2)O3和O2是__ 。
A.同一种物质 B.同素异形体
C.氧的同位素 D.同一种元素
大气中的臭氧层可滤除大量的紫外光,保护地球上的生物。氟利昂(如CCl2F2)可在光的作用下分解,产生Cl原子,Cl原子会对臭氧层产生长久的破坏作用,臭氧的分子式为O3。有关反应为:
O3
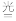 O2+O
O2+OCl+O3荣
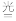 ClO+O2
ClO+O2O+ClO=Cl+O2
总反应为2O3=3O2。
(1)在上述臭氧变成氧气的过程中,Cl原子是
A.反应物 B.生成物
C.中间产物 D.催化剂
(2)O3和O2是
A.同一种物质 B.同素异形体
C.氧的同位素 D.同一种元素
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】硫酸的消费量是衡量一个国家化工生产水平的重要标志。而在硫酸的生产中,最关键的一步反应为:2SO2(g)+O2(g) 2SO3(g)。
2SO3(g)。
(1)一定条件下,SO2与O2反应10min后,若SO2和SO3物质的量浓度分别为1mol/L和3mol/L,则SO2起始物质的量浓度为___________________ ;10min生成SO3的化学反应速率为___________________ 。
(2)下列关于该反应的说法正确的是___________________ 。
A.增加O2的浓度能加快反应速率
B.降低体系温度能加快反应速率
C.使用催化剂能加快反应速率
D.一定条件下达到反应限度时SO2全部转化为SO3
(3)工业制硫酸,用过量的氨水对SO2尾气处理,请写出相关的离子方程式:____________ 。
 2SO3(g)。
2SO3(g)。(1)一定条件下,SO2与O2反应10min后,若SO2和SO3物质的量浓度分别为1mol/L和3mol/L,则SO2起始物质的量浓度为
(2)下列关于该反应的说法正确的是
A.增加O2的浓度能加快反应速率
B.降低体系温度能加快反应速率
C.使用催化剂能加快反应速率
D.一定条件下达到反应限度时SO2全部转化为SO3
(3)工业制硫酸,用过量的氨水对SO2尾气处理,请写出相关的离子方程式:
您最近一年使用:0次

 Z(g),在其他条件不变时,改变其中一个条件,则生成Z的速率(填“增大”“减小”或“不变”):
Z(g),在其他条件不变时,改变其中一个条件,则生成Z的速率(填“增大”“减小”或“不变”):

