一定温度下,反应3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g),在一密闭容器中进行达平衡后,试回答:
Fe3O4(s)+4H2(g),在一密闭容器中进行达平衡后,试回答:
(1)增加Fe的物质的量,其正反应速率___________ 。
(A.变快 B.不变 C变慢,填字母代号)。
(2)将容器的体积缩小一半,其正反应速率___________ ,逆反应速率___________ 。
(3)若保持体积不变,充入Ar,其逆反应速率___________ 。
(4)保持压强不变,充入Ar,其正反应速率___________ 。
 Fe3O4(s)+4H2(g),在一密闭容器中进行达平衡后,试回答:
Fe3O4(s)+4H2(g),在一密闭容器中进行达平衡后,试回答:(1)增加Fe的物质的量,其正反应速率
(A.变快 B.不变 C变慢,填字母代号)。
(2)将容器的体积缩小一半,其正反应速率
(3)若保持体积不变,充入Ar,其逆反应速率
(4)保持压强不变,充入Ar,其正反应速率
更新时间:2019-11-06 09:11:57
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】密闭容器中发生反应: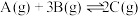
 ,根据下列
,根据下列 图象,回答问题:
图象,回答问题:
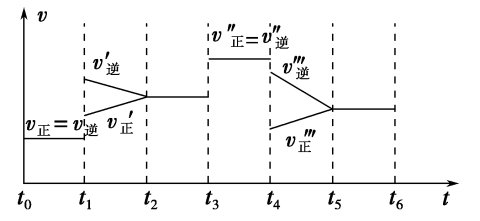
(1)下列时刻所改变的外界条件是
_______ ;
_______ ;
_______ 。
(2)反应速率最快的时间段是_______ 。
(3)下列措施能增大正反应速率的是_______。
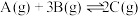
 ,根据下列
,根据下列 图象,回答问题:
图象,回答问题:
(1)下列时刻所改变的外界条件是



(2)反应速率最快的时间段是
(3)下列措施能增大正反应速率的是_______。
A.通入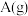 | B.分离出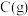 | C.降温 | D.增大容积 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】在相同条件下进行Mg和酸反应的对比实验,相关数据如下;
(1)试比较有关量的大小:
________  ,
,
________  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
(2)现欲改变反应条件,使实验I中 降低,
降低, 不变,试写出两种可行的方法:
不变,试写出两种可行的方法:
①_______ ; ②______ 。
Mg的质量 | 酸溶液 | 开始的反应速率 | 产生 | |
Ⅰ |
|
|
|
|
Ⅱ |
|
|
|
|
(1)试比较有关量的大小:

 ,
,
 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。(2)现欲改变反应条件,使实验I中
 降低,
降低, 不变,试写出两种可行的方法:
不变,试写出两种可行的方法:①
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】海带中含有丰富的碘元素,某化学兴趣小组设计如下流程提取碘:
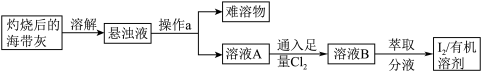
请回答下列问题:
(1)操作a的名称是___________ (填“过滤”或“蒸发”);
(2)溶液A中通入足量 的目的是将
的目的是将 氧化为
氧化为 ,则
,则 起到的作用是
起到的作用是___________ (填“氧化剂”或“还原剂”);
(3)在萃取时,可选用的萃取剂为___________ (填“酒精”或“四氯化碳”);
(4)将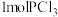 和
和 充入
充入 的密闭容器中,在一定条件下发生反应
的密闭容器中,在一定条件下发生反应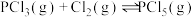 ,5min后测得
,5min后测得 的物质的量为
的物质的量为 。
。
①用 表示该反应的化学反应速率是
表示该反应的化学反应速率是___________  ;
;
②当其他条件不变时,增大压强,该反应速率将___________ (填“增大”或“减小”)。

请回答下列问题:
(1)操作a的名称是
(2)溶液A中通入足量
 的目的是将
的目的是将 氧化为
氧化为 ,则
,则 起到的作用是
起到的作用是(3)在萃取时,可选用的萃取剂为
(4)将
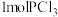 和
和 充入
充入 的密闭容器中,在一定条件下发生反应
的密闭容器中,在一定条件下发生反应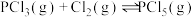 ,5min后测得
,5min后测得 的物质的量为
的物质的量为 。
。①用
 表示该反应的化学反应速率是
表示该反应的化学反应速率是 ;
;②当其他条件不变时,增大压强,该反应速率将
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】请解释下列现象。
(1)夏季常把食物放在冰箱中冷藏_______ 。
(2)将大小相同的铁片分别放入相同体积的 和
和 盐酸中,后者产生氢气的速率比前者大
盐酸中,后者产生氢气的速率比前者大________ 。
(3)常温常压下合成氨反应的速率极小,工业上常采用的反应条件是约500℃、20~50MPa(约200~500个大气压)下用铁触媒作催化剂_______ 。
(1)夏季常把食物放在冰箱中冷藏
(2)将大小相同的铁片分别放入相同体积的
 和
和 盐酸中,后者产生氢气的速率比前者大
盐酸中,后者产生氢气的速率比前者大(3)常温常压下合成氨反应的速率极小,工业上常采用的反应条件是约500℃、20~50MPa(约200~500个大气压)下用铁触媒作催化剂
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】在一密闭容器中充入1molH2和1molI2,压强为p(Pa),并在一定温度下使其发生反应:H2(g)+I2(g) 2HI(g) ΔH<0.(用“加快”、“减慢”、“不变”填空)
2HI(g) ΔH<0.(用“加快”、“减慢”、“不变”填空)
(1)保持容器容积不变,再向其中充入1molH2,反应速率_____ 。
(2)保持容器容积不变,再向其中充入1molN2(不参加反应),反应速率_____ 。
(3)保持容器内气体的压强不变,再向其中充入1molN2,反应速率_____ 。
(4)保持容器容积不变,再向其中充入1molH2和1molI2,反应速率_____ 。
(5)保持容器内气体的压强不变,再向其中充入1molH2和1molI2,反应速率_____ 。
 2HI(g) ΔH<0.(用“加快”、“减慢”、“不变”填空)
2HI(g) ΔH<0.(用“加快”、“减慢”、“不变”填空)(1)保持容器容积不变,再向其中充入1molH2,反应速率
(2)保持容器容积不变,再向其中充入1molN2(不参加反应),反应速率
(3)保持容器内气体的压强不变,再向其中充入1molN2,反应速率
(4)保持容器容积不变,再向其中充入1molH2和1molI2,反应速率
(5)保持容器内气体的压强不变,再向其中充入1molH2和1molI2,反应速率
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】(1)写出纯碱的化学式:____ 。
(2)写出一氯甲烷的结构式:_____ 。
(3)面粉在相对密闭的空间内悬浮在空气中,达到一定浓度时,遇火却会发生剧烈的反应,导致爆炸,请用化学知识解释其现象___ 。
(4)写出工业制粗硅的化学方程式:___ 。
(2)写出一氯甲烷的结构式:
(3)面粉在相对密闭的空间内悬浮在空气中,达到一定浓度时,遇火却会发生剧烈的反应,导致爆炸,请用化学知识解释其现象
(4)写出工业制粗硅的化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】100mL浓度为2mol•L-1的硫酸与过量锌粒反应,为加快反应速率,又不影响生成氢气的总量,可采取的方法是________ 。
A.加入适量的6mol•L-1的硫酸
B.将锌粒改为锌粉
C.加入适量的KCl溶液
D.升高溶液温度
E.加入适量硫酸铜
A.加入适量的6mol•L-1的硫酸
B.将锌粒改为锌粉
C.加入适量的KCl溶液
D.升高溶液温度
E.加入适量硫酸铜
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】定条件下,发生反应A(g)+B(g) C(g) △H>0,达到平衡后根据下列图像判断:
C(g) △H>0,达到平衡后根据下列图像判断:
A.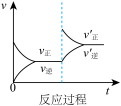 B.
B.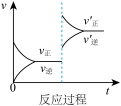 C.
C. D.
D.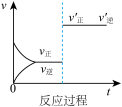 E.
E.
(1)表示升高温度,达到新平衡的是图______ (填“A”、“B”、“C”、“D”或“E”,下同),新平衡中C的质量分数______ (填“增大”、“减小”或“不变”,下同)。
(2)表示降低压强,达到新平衡的是图______ ,A的转化率______ 。
(3)表示减少C的浓度,达到新平衡的是图______ ,表示使用催化剂,达新平衡的是图。
(4)增加A的浓度,达到新平衡的是图______ ,达到平衡后A的转化率______ 。
 C(g) △H>0,达到平衡后根据下列图像判断:
C(g) △H>0,达到平衡后根据下列图像判断:A.
 B.
B. C.
C. D.
D. E.
E.
(1)表示升高温度,达到新平衡的是图
(2)表示降低压强,达到新平衡的是图
(3)表示减少C的浓度,达到新平衡的是图
(4)增加A的浓度,达到新平衡的是图
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】利用废镍电池的金属电极芯(主要成分为Co、 Ni,还含少量Fe、Al等)生产醋酸钴晶体、硫酸镍晶体的工艺流程如下。
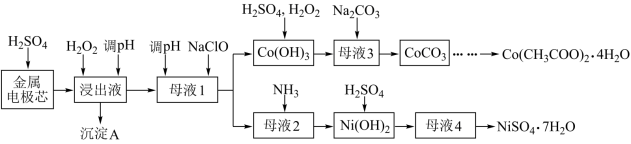
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
用硫酸浸取金属电极芯时,提高浸取率的方法有___________ (写出一种合理方法即可)。

已知:部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Co(OH)3 | Al(OH)3 | Ni(OH)2 |
| 开始沉淀pH | 2.2 | 7.4 | 7.6 | 0.1 | 4.0 | 7.6 |
| 完全沉淀pH | 3.2 | 8.9 | 9.2 | 1.1 | 5.2 | 9.2 |
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】甲同学用等质量的锌粉先后与1mol·L-1盐酸及相同体积、未知浓度的盐酸反应,记录相关数据,并作出这两个反应过程中放出气体的体积随反应时间的变化曲线图(如图所示)。

(1)如果请你做这个实验,你测量该反应所放气体的体积的方法是___ 。
(2)根据图示可判断,该同学所用的盐酸的浓度比1 mol/L___ (填“大”或“小”)。理由是___ 。
(3)乙同学为控制反应速率,防止因反应过快而难以测量氢气体积,想事先在盐酸中加入等体积的下列溶液以减慢反应速率。你认为在以下试剂中,不可行的是___ 。
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(4)丙同学用1mol·L-1硫酸代替上述实验中的1mol·L-1盐酸,请问二者的反应速率是否相同___ 。理由是___ 。

(1)如果请你做这个实验,你测量该反应所放气体的体积的方法是
(2)根据图示可判断,该同学所用的盐酸的浓度比1 mol/L
(3)乙同学为控制反应速率,防止因反应过快而难以测量氢气体积,想事先在盐酸中加入等体积的下列溶液以减慢反应速率。你认为在以下试剂中,不可行的是
A.蒸馏水 B.KCl溶液 C.KNO3溶液 D.CuSO4溶液
(4)丙同学用1mol·L-1硫酸代替上述实验中的1mol·L-1盐酸,请问二者的反应速率是否相同
您最近一年使用:0次

 的总量
的总量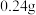
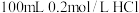 溶液
溶液 溶液
溶液

