沉淀溶解平衡状态
(1)定义:在一定条件下,当难溶固体_______ 的速率与_______ 的速率相等时,溶液中离子浓度、固体的量保持不变的状态。
(2)表示方法:如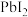 的沉淀溶解平衡可表示为
的沉淀溶解平衡可表示为_______ 。
(1)定义:在一定条件下,当难溶固体
(2)表示方法:如
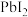 的沉淀溶解平衡可表示为
的沉淀溶解平衡可表示为
更新时间:2021-09-03 21:27:28
|
【知识点】 难溶电解质溶解平衡定义及特征解读
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】依据所学知识回答问题:
(1)0.1 mol·L-1的KAl(SO4)2溶液中各离子的浓度由大到小的顺序为_______ 。
(2)液态SO2是一种似水溶剂,可以微弱电离:SO2+SO2 SO2++SO
SO2++SO 在液态SO2中,视SOCl2为酸,Cs2SO3为碱,试写出二者在液态SO2体系中发生反应的化学方程式:
在液态SO2中,视SOCl2为酸,Cs2SO3为碱,试写出二者在液态SO2体系中发生反应的化学方程式:_______ 。
(3)盐类水解的实质就是盐产生的阴阳离子与水电离出的H+或OH-结合的过程,下列物质与水反应和盐类水解类似,写出相应的化学方程式:
Mg3N2与水反应:_______ ;
PCl5与热水反应:_______ 。
(4)常温下,BaCO3(s)在水中的溶解平衡曲线如图所示,则该温度下,Ksp(BaCO3)=_______ ;将0.2 mol·L-1的Ba(OH)2溶液与0.2 mol·L-1的NaHCO3溶液等体积混合后,混合溶液的pH=_______ ,c(CO )=
)=_______ 。(忽略混合时溶液体积的变化)

(1)0.1 mol·L-1的KAl(SO4)2溶液中各离子的浓度由大到小的顺序为
(2)液态SO2是一种似水溶剂,可以微弱电离:SO2+SO2
 SO2++SO
SO2++SO 在液态SO2中,视SOCl2为酸,Cs2SO3为碱,试写出二者在液态SO2体系中发生反应的化学方程式:
在液态SO2中,视SOCl2为酸,Cs2SO3为碱,试写出二者在液态SO2体系中发生反应的化学方程式:(3)盐类水解的实质就是盐产生的阴阳离子与水电离出的H+或OH-结合的过程,下列物质与水反应和盐类水解类似,写出相应的化学方程式:
Mg3N2与水反应:
PCl5与热水反应:
(4)常温下,BaCO3(s)在水中的溶解平衡曲线如图所示,则该温度下,Ksp(BaCO3)=
 )=
)=
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】难溶电解质沉淀溶解平衡的影响因素
已知沉淀溶解平衡:Mg(OH)2(s)=Mg2+(aq)+2OH-(aq)
Q:离子积对于AmBn(s)=mAn+(aq)+nBm-(aq)任意时刻Q=cm(An+)·cn(Bm-)。
(1)Q>Ksp,溶液过饱和,有_______ 析出,直至溶液_______ ,达到新的平衡。
(2)Q=Ksp,溶液饱和,沉淀与溶解处于_______ 。
(3)Q<Ksp,溶液未饱和,无_______ 析出,若加入过量难溶电解质,难溶电解质_______ 直至溶液_______ 。
已知沉淀溶解平衡:Mg(OH)2(s)=Mg2+(aq)+2OH-(aq)
| 条件改变 | 移动方向 | c(Mg2+) | c(OH-) |
| 加少量水 | |||
| 升温 | |||
| 加MgCl2(s) | |||
| 加盐酸 | |||
| 加NaOH(s) |
(1)Q>Ksp,溶液过饱和,有
(2)Q=Ksp,溶液饱和,沉淀与溶解处于
(3)Q<Ksp,溶液未饱和,无
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】写出下列物质在水溶液中的水解离子方程式及沉淀溶解平衡方程式:
(1)NaClO水解离子方程式___________________________
(2)NH4Cl水解离子方程式____________________________
(3)KAl(SO4)2·12H2O水解离子方程式__________________________
(4)CaCO3沉淀溶解平衡方程式__________________________
(5)Fe(OH)3沉淀溶解平衡方程式__________________________
(1)NaClO水解离子方程式
(2)NH4Cl水解离子方程式
(3)KAl(SO4)2·12H2O水解离子方程式
(4)CaCO3沉淀溶解平衡方程式
(5)Fe(OH)3沉淀溶解平衡方程式
您最近一年使用:0次



