下列叙述正确的是
| A.某醋酸溶液的pH=a,将此溶液稀释10倍后,溶液的pH=b,则a>b |
| B.常温下,某溶液中由水电离的c(OH-) = 1.0×10-13mol/L,则此溶液一定呈酸性 |
| C.25℃时,将pH=4的盐酸稀释1000倍后,溶液的pH=7 |
| D.25℃时,pH=13的强碱溶液与pH=2的强酸溶液混合,若所得混合液的pH=7,则强碱与强酸的体积比是1:10 |
11-12高二·河南安阳·阶段练习 查看更多[10]
江西省宜春市万载中学2021-2022学年高一下学期第二次月考化学试题四川省乐山市峨眉第二中学校2021-2022学年高二下学期3月月考化学试题天津市第九十五中益中学校2021-2022学年高三上学期第二次月考化学试题天津市第二十一中学2021-2022学年高二上学期期中检测化学试题辽宁省辽河油田第二高级中学2021-2022学年高二上学期开学考试化学试题黑龙江省大庆中学2020-2021学年高二上学期期中考试化学试题吉林省白城市通榆县第一中学2019-2020学年高二上学期第三次月考化学试题安徽省安庆市第二中学2018-2019学年高二下学期开学考试化学试题山东省新泰市第二中学2018-2019学年高二上学期第三次阶段性测试化学试题(已下线)2012-2013学年河南省安阳一中高二第二次阶段考试化学试卷
更新时间:2016-12-09 03:52:19
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】25℃时,在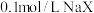 溶液中,水电离出的
溶液中,水电离出的 浓度为
浓度为 ;在
;在 盐酸中,水电离出的
盐酸中,水电离出的 浓度为
浓度为 ,若
,若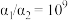 ,则
,则 溶液的
溶液的 值为
值为
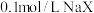 溶液中,水电离出的
溶液中,水电离出的 浓度为
浓度为 ;在
;在 盐酸中,水电离出的
盐酸中,水电离出的 浓度为
浓度为 ,若
,若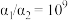 ,则
,则 溶液的
溶液的 值为
值为| A.5 | B.7 | C.10 | D.11 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】捕获并利用二氧化碳是实现碳减排的重要举措之一。某发明利用 和
和 捕获二氧化碳,
捕获二氧化碳, 是其中间产物之一、设NA为阿伏加德罗常数的值,室温下,下列说法正确的是
是其中间产物之一、设NA为阿伏加德罗常数的值,室温下,下列说法正确的是
 和
和 捕获二氧化碳,
捕获二氧化碳, 是其中间产物之一、设NA为阿伏加德罗常数的值,室温下,下列说法正确的是
是其中间产物之一、设NA为阿伏加德罗常数的值,室温下,下列说法正确的是A.  中所含的电子数目为2.2 NA 中所含的电子数目为2.2 NA |
B.   溶液中, 溶液中, 和 和 的微粒数之和为0.1 NA 的微粒数之和为0.1 NA |
C.  晶体中,阴、阳离子总数为0.3 NA 晶体中,阴、阳离子总数为0.3 NA |
D.  的 的 溶液中的 溶液中的 数目为0.1 NA 数目为0.1 NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,pH=10的M、N两种碱溶液各1mL,分别加水稀释到100mL,其pH与溶液体积的关系如图所示,下列说法正确的是
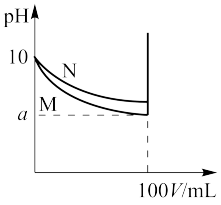

A.稀释前,两溶液中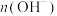 不等 不等 |
| B.稀释后,M溶液的碱性比N溶液的碱性强 |
| C.完全中和M、N溶液时,消耗同浓度盐酸的体积相等 |
| D.若8<a<10,则M、N都是弱碱 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常温下,有下列四种溶液:①pH=2的HCl溶液;②pH=2的CH3COOH溶液;③pH=12的NaOH溶液;④pH=12的氨水。下列有关说法不正确的是( )
| A.四种溶液中的Kw相同,由水电离出的c(H+):①=②=③=④ |
| B.取体积相同的溶液①、②、③分别与足量铝粉反应,生成H2的量:①最少 |
| C.将等体积的四种溶液分别稀释100倍,所得溶液的pH:③>④>②>① |
| D.常温下,将②和③等体积混合:c(CH3COO-)-c(Na+)=c(H+)-c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】常温下1体积pH=2.5的盐酸与10体积某一元强碱溶液恰好完全反应,则该碱溶液的pH等于( )
| A.9.0 | B.9.5 | C.1 0.5 | D.1 1.0 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列说法错误的是
| A.弱酸pH=a,加水稀释到10n倍,则pH<a+n(a+n<7) |
| B.中和相同体积相同pH的盐酸和醋酸溶液所需NaOH的物质的量不相同,醋酸消耗NaOH的物质的量多 |
| C.pH=3的一元酸和pH=11的一元碱等体积混合后,混合液中一定存在c(H+)=c(OH-) |
| D.常温,pH=2的盐酸、pH=2的醋酸中由水电离出的c(H+)=c(OH-)=10-12 mol·L-1 |
您最近一年使用:0次




