下列说法正确的是
| A.根据化学反应速率可以判断反应物转变为生成物的难易 |
| B.根据∆H可以判断反应的活化能 |
| C.根据熵变可以判断所有化学反应能否自发进行 |
| D.根据化学平衡常数可以判断化学反应进行的程度 |
更新时间:2021-10-26 16:23:37
|
相似题推荐
单选题
|
较易
(0.85)
名校
【推荐1】反应X=2Z经历两步:①X→Y:②Y→2Z。反应体系中X、Y、Z的物质的量(n)随时间(t)的变化曲线如图所示。下列说法正确的是
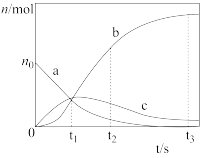

| A.曲线c为n(Z)随t的变化曲线 |
| B.0~t1时间段内,反应速率v(X)=v(Y)=v(Z) |
| C.t2时,Y的消耗速率大于生成速率 |
| D.t3时,n(Z)=2n0-n(Y) |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】草酸与高锰酸钾在酸性溶液中反应生成Mn2+和CO2,当溶液呈褐色时,视为反应达到终点。实验室可利用该反应发生时溶液褐色出现的快慢来研究反应条件对反应速率的影响。某实验小组用5mL0.002mol·L-1KMnO4溶液与3mL0.01mol·L-1H2C2O4溶液在不同条件下的反应,来研究不同条件对反应速率的影响,相关实验数据如表所示:
下列说法错误的是
| 组别 | 10%H2SO4溶液 体积/mL | 温度/℃ | 其他物质 | 褐色出现时间/s |
| ① | 2 | 20 | a | |
| ② | 2 | 20 | 10滴饱和MnSO4溶液 (体积变化忽略不计) | 10 |
| ③ | 2 | 30 | b | |
| ④ | 1 | 20 | 1mL蒸馏水 | c |
| A.第②组实验中用高锰酸钾表示的反应速率为v(KMnO4)=1×10-4mol·L-1·s-1 |
| B.第①组与第②组实验用于研究催化剂对反应速率的影响 |
| C.第①组与第③组实验用于研究温度对反应速率的影响 |
| D.实验数据中,b是否小于10将无法确定,而c则一定大于10 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列关于有效碰撞理论的说法一定正确的是
| A.催化剂在化学反应过程中参与了反应,使用催化剂单位体积内活化分子数增大,反应速率加快 |
| B.增大浓度,活化分子百分数增大,反应速率加快 |
| C.升高温度,反应的活化能降低,反应速率加快 |
| D.增大压强,所有反应的有效碰撞概率增大,反应速率加快 |
您最近一年使用:0次
单选题
|
较易
(0.85)
真题
名校
【推荐2】据报道,科学家开发出了利用太阳能分解水的新型催化剂。下列有关水分解过程的能量变化示意图正确的是
A.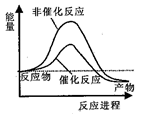 | B.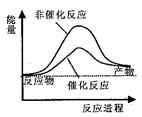 |
C.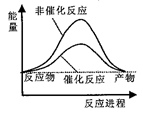 | D.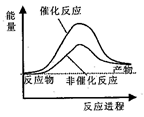 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】已知反应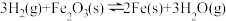 ,该反应的平衡常数表达式为
,该反应的平衡常数表达式为
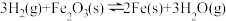 ,该反应的平衡常数表达式为
,该反应的平衡常数表达式为A.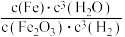 | B. |
C. | D. |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
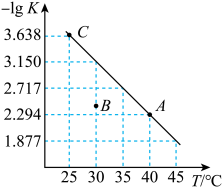
【推荐2】将一定量纯净的氨基甲酸铵固体置于密闭容器中,发生反应:NH2COONH4(s) 2NH3(g)+CO2(g)。该反应的平衡常数的负对数值(-lgK)随温度(T)的变化如图所示。下列说法不正确的是
2NH3(g)+CO2(g)。该反应的平衡常数的负对数值(-lgK)随温度(T)的变化如图所示。下列说法不正确的是
 2NH3(g)+CO2(g)。该反应的平衡常数的负对数值(-lgK)随温度(T)的变化如图所示。下列说法不正确的是
2NH3(g)+CO2(g)。该反应的平衡常数的负对数值(-lgK)随温度(T)的变化如图所示。下列说法不正确的是
| A.该反应的△H>0 |
| B.30℃时,B点对应状态的v(正)>v(逆) |
| C.A点对应状态的平衡常数K(A)=10-2.294mol3/L3 |
| D.NH3体积分数不变时,该反应不一定达到平衡状态 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】常温下,某密闭容器中反应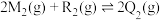 能自发进行。下列有关该反应的说法正确的是
能自发进行。下列有关该反应的说法正确的是
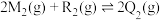 能自发进行。下列有关该反应的说法正确的是
能自发进行。下列有关该反应的说法正确的是| A.化学键断裂时放出热量 |
B.催化剂使正反应的 降低 降低 |
| C.该反应为放热反应 |
| D.若平衡常数不变,则平衡不移动 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】下列有关化学反应进行的方向描述正确的是
| A.判断反应进行的方向可以单独考虑体系的焓变与熵变 |
| B.涂有防锈漆和未涂有防锈漆的钢制器件,其发生腐蚀过程的自发性是相同的 |
| C.依据自发反应的自发性,自发反应的实现与条件无关 |
| D.对于△H>0的化学反应,不可能发生 |
您最近一年使用:0次

 3R(g);经2s后达到平衡,测得R气体的浓度为0.6mol/L。下列说法中错误的是
3R(g);经2s后达到平衡,测得R气体的浓度为0.6mol/L。下列说法中错误的是

