回答下列问题:
(1)在一定条件下N2与H2反应生成NH3,请回答:
①若反应物的总能量为E1,生成物的总能量为E2,且E1>E2,则该反应为___ (填“吸热”或“放热”)反应。
②已知拆开1molH—H键、1molN—H键、1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为___ 。
(2)N2H4和H2O2混合可作火箭推进剂,已知:16g液态N2H4和足量氧气反应生成N2(g)和H2O(l),放出310.6kJ的热量;2H2O2(l)=O2(g)+2H2O(l) ΔH=-196.4kJ·mol-1。反应N2H4(l)+O2(g)=N2(g)+2H2O(l)的ΔH=___ kJ·mol-1。N2H4和H2O2反应生成N2(g)和H2O(l)的热化学方程式为___ 。
(3)向1L1mol/L的NaOH溶液中加入下列物质:①浓H2SO4;②稀硝酸;③稀醋酸,恰好完全反应的热效应为△H1、△H2、△H3,则三者由小到大顺序为___ 。
(1)在一定条件下N2与H2反应生成NH3,请回答:
①若反应物的总能量为E1,生成物的总能量为E2,且E1>E2,则该反应为
②已知拆开1molH—H键、1molN—H键、1molN≡N键分别需要的能量是436kJ、391kJ、946kJ,则N2与H2反应生成NH3的热化学方程式为
(2)N2H4和H2O2混合可作火箭推进剂,已知:16g液态N2H4和足量氧气反应生成N2(g)和H2O(l),放出310.6kJ的热量;2H2O2(l)=O2(g)+2H2O(l) ΔH=-196.4kJ·mol-1。反应N2H4(l)+O2(g)=N2(g)+2H2O(l)的ΔH=
(3)向1L1mol/L的NaOH溶液中加入下列物质:①浓H2SO4;②稀硝酸;③稀醋酸,恰好完全反应的热效应为△H1、△H2、△H3,则三者由小到大顺序为
更新时间:2021-10-28 19:06:33
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】从化石燃料中能获得许多重要的有机化工原料,请回答下列问题。
(1)在一定条件下, 甲烷气体充分燃烧生成二氧化碳气体和液态水放出
甲烷气体充分燃烧生成二氧化碳气体和液态水放出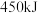 的热量,则该反应的热化学方程式为:
的热量,则该反应的热化学方程式为:___________ 。
(2)甲烷可以用来设计成燃料电池,如图是甲烷燃料电池原理示意图。请写出该电池负极的电极反应式:___________ 。

(1)在一定条件下,
 甲烷气体充分燃烧生成二氧化碳气体和液态水放出
甲烷气体充分燃烧生成二氧化碳气体和液态水放出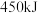 的热量,则该反应的热化学方程式为:
的热量,则该反应的热化学方程式为:(2)甲烷可以用来设计成燃料电池,如图是甲烷燃料电池原理示意图。请写出该电池负极的电极反应式:

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知:①CaCO3(s)=CaO+CO2(g) ΔH=+177.7 kJ·mol-1
②C(s)+H2O(g)=CO(g)+H2(g) ΔH=-131.3 kJ·mol-1
③C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
④CO(g)+ O2(g)=CO2(g) ΔH=-283 kJ·mol-1
O2(g)=CO2(g) ΔH=-283 kJ·mol-1
⑤ H2SO4(l)+NaOH(l)=
H2SO4(l)+NaOH(l)=  Na2SO4(l)+H2O(l) ΔH=-57.3 kJ·mol-1
Na2SO4(l)+H2O(l) ΔH=-57.3 kJ·mol-1
⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3 kJ·mol-1
⑦2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
(1)上述热化学方程式中,不正确的有___________ ,不正确的理由分别是:___________ 。
(2)根据上述信息,写出C转化为CO的热化学方程式___________ 。
(3)上述正确的热化学方程式中,表示燃烧热的热化学方程式有___________ ;表示中和热的热化学方程式有___________ 。
②C(s)+H2O(g)=CO(g)+H2(g) ΔH=-131.3 kJ·mol-1
③C(s)+O2(g)=CO2(g) ΔH=-393.5 kJ·mol-1
④CO(g)+
 O2(g)=CO2(g) ΔH=-283 kJ·mol-1
O2(g)=CO2(g) ΔH=-283 kJ·mol-1⑤
 H2SO4(l)+NaOH(l)=
H2SO4(l)+NaOH(l)=  Na2SO4(l)+H2O(l) ΔH=-57.3 kJ·mol-1
Na2SO4(l)+H2O(l) ΔH=-57.3 kJ·mol-1⑥HNO3(aq)+NaOH(aq)=NaNO3(aq)+H2O(l) ΔH=-57.3 kJ·mol-1
⑦2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
(1)上述热化学方程式中,不正确的有
(2)根据上述信息,写出C转化为CO的热化学方程式
(3)上述正确的热化学方程式中,表示燃烧热的热化学方程式有
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】I、依据事实,写出下列反应的热化学方程式。
(1)在25 ℃、101 kPa下,1 g甲烷燃烧生成CO2和液态水时放热55.625 kJ。则表示甲烷燃烧热的热化学方程式为________________________ 。
(2)若适量的N2和O2完全反应,每生成23 g NO2需要吸收16.95 kJ热量,则表示该反应的热化学方程式为______________ 。
(3)在25 ℃、101 kPa条件下,C(s)、H2(g)、CH3COOH(1)的燃烧热分别为393.5 kJ/mol、285.8 kJ/mol、870.3 kJ/mol,则2C(s)+2H2(g)+O2(g)===CH3COOH(1)的反应热ΔH为________ 。
II、锌锰干电池是应用最普遍的电池之一。其基本反应为:
X极:Zn-2e-===Zn2+
Y极:2MnO2+2NH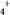 +2e-===Mn2O3+2NH3+H2O
+2e-===Mn2O3+2NH3+H2O
(1)X是电池的________ (填“正”或“负”,下同)极,Y是电池的________ 极。
(2)该电池总反应的离子方程式为:_______________________ 。
(3)若反应消耗16.25gZn,则电池中转移电子的物质的量为________ 。
(1)在25 ℃、101 kPa下,1 g甲烷燃烧生成CO2和液态水时放热55.625 kJ。则表示甲烷燃烧热的热化学方程式为
(2)若适量的N2和O2完全反应,每生成23 g NO2需要吸收16.95 kJ热量,则表示该反应的热化学方程式为
(3)在25 ℃、101 kPa条件下,C(s)、H2(g)、CH3COOH(1)的燃烧热分别为393.5 kJ/mol、285.8 kJ/mol、870.3 kJ/mol,则2C(s)+2H2(g)+O2(g)===CH3COOH(1)的反应热ΔH为
II、锌锰干电池是应用最普遍的电池之一。其基本反应为:
X极:Zn-2e-===Zn2+
Y极:2MnO2+2NH
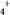 +2e-===Mn2O3+2NH3+H2O
+2e-===Mn2O3+2NH3+H2O(1)X是电池的
(2)该电池总反应的离子方程式为:
(3)若反应消耗16.25gZn,则电池中转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】能源、环境与人类生活和社会发展密切相关,研究它们的综合利用有重要意义。
(1)二氧化碳能引起温室效应,而对二氧化碳的捕集、利用是当今世界能源领域的一个重要研究方向。工业上用CO2和H2在一定条件下反应可合成二甲醚,已知:CO2(g)+3H2(g)═CH3OH(g)+H2O(g);△H1=-53.7kJ/mol
CH3OCH3(g)+H2O(g)═2CH3OH(g);△H2=+23.4kJ/mol
则2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g);△H3=
CH3OCH3(g)+3H2O(g);△H3=________ kJ/mol
(2)在一定条件下CO2和H2充入一定固定容积的密闭容器中,在两种不同温度下发生反应:2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g),测得CH3OCH3(g)的物质的量随时间的变化如图1所示。
CH3OCH3(g)+3H2O(g),测得CH3OCH3(g)的物质的量随时间的变化如图1所示。
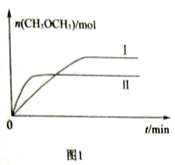

①曲线I、Ⅱ对应的平衡常数大小关系为KI________ KⅡ(填“>”或“=”或“<”)。
②一定温度下,若此反应在恒压容器中进行,不能判断该反应达到化学平衡状态依据的是______ 。
a.混合气体的密度 b.CH3OCH3(g)和H2O(g)体积比不变
c.c(H2)=2c(H2O) d.4个C=O断裂的同时有6个H-O断裂
③一定条件下,上述合成二甲醚的反应达到平衡状态后,若改变反应的某一个条件,下列变化能说明平衡一定向正反应方向移动的是________ (填代号)。
A.CO2的转化率增大 B.逆反应速率先增大后减小
C.容器中的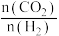 值变大 D.平衡常数增大
值变大 D.平衡常数增大
(3)合成气CO和H2在一定条件下能发生如下反应:CO(g)+2H2(g) CH3OH(g);△H。
CH3OH(g);△H。
①在某压强下,合成甲醇的反应在不同温度、不同投料比时,CO的转化率如图2所示。500K温度下,将2molCO和4molH2充入2L的密闭容器中,5min后反应达到平衡状态,则0~5min内的平均反应速率v(CH3OH)=________ 。
②△H________ 0(填“>”或“=”或“<”)。
③上述合成甲醇的过程中提高CO的转化率可采取的措施有________ 、________ (回答2点)。
(1)二氧化碳能引起温室效应,而对二氧化碳的捕集、利用是当今世界能源领域的一个重要研究方向。工业上用CO2和H2在一定条件下反应可合成二甲醚,已知:CO2(g)+3H2(g)═CH3OH(g)+H2O(g);△H1=-53.7kJ/mol
CH3OCH3(g)+H2O(g)═2CH3OH(g);△H2=+23.4kJ/mol
则2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g);△H3=
CH3OCH3(g)+3H2O(g);△H3=(2)在一定条件下CO2和H2充入一定固定容积的密闭容器中,在两种不同温度下发生反应:2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g),测得CH3OCH3(g)的物质的量随时间的变化如图1所示。
CH3OCH3(g)+3H2O(g),测得CH3OCH3(g)的物质的量随时间的变化如图1所示。

①曲线I、Ⅱ对应的平衡常数大小关系为KI
②一定温度下,若此反应在恒压容器中进行,不能判断该反应达到化学平衡状态依据的是
a.混合气体的密度 b.CH3OCH3(g)和H2O(g)体积比不变
c.c(H2)=2c(H2O) d.4个C=O断裂的同时有6个H-O断裂
③一定条件下,上述合成二甲醚的反应达到平衡状态后,若改变反应的某一个条件,下列变化能说明平衡一定向正反应方向移动的是
A.CO2的转化率增大 B.逆反应速率先增大后减小
C.容器中的
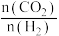 值变大 D.平衡常数增大
值变大 D.平衡常数增大(3)合成气CO和H2在一定条件下能发生如下反应:CO(g)+2H2(g)
 CH3OH(g);△H。
CH3OH(g);△H。①在某压强下,合成甲醇的反应在不同温度、不同投料比时,CO的转化率如图2所示。500K温度下,将2molCO和4molH2充入2L的密闭容器中,5min后反应达到平衡状态,则0~5min内的平均反应速率v(CH3OH)=
②△H
③上述合成甲醇的过程中提高CO的转化率可采取的措施有
您最近一年使用:0次
【推荐2】丙烯是工业上合成精细化学品的原料,随着天然气和页岩气的可用性不断提高,制取丙烯的技术受到人们越来越多的关注。
(1)主反应I :C3H8(g) C3 H6(g)+H2(g) △H1
C3 H6(g)+H2(g) △H1
副反应Ⅱ :C3H8(g) C2H4(g)+CH4(g) △H2
C2H4(g)+CH4(g) △H2
已知H2、丙烷(C3H8 )和丙烯(C3 H6)的燃烧热(△H)分别是-285.8 kJ·mol-1、-2220 kJ·mol-1和-2051 kJ·mol-1,则△H=_______ kJ·mol-1.主反应I在_______ (填“高温”、“低温”或“任意温度”)时能自发进行。
(2)一定温度下,向总压恒定为p kPa的容器中充入一定量C3H8气体,在催化作用下,发生上述反应制备C3 H6。
①下列情况表明反应达到平衡状态的是_______ (填标号)。
A.气体密度不再改变
B.体系压强不再改变
C.混合气体的平均摩尔质量不再改变
D.单位时间内消耗C3H8的物质的量与生成C3 H6的物质的量相等
②从平衡移动的角度判断,达到平衡后通入N2的作用是_______ 。
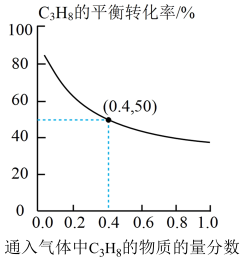
(3)在温度为T时,向起始压强为120 kPa的恒压容器中通入4 mol C3H8和6 mol N2发生反应,经10 min反应达到平衡,C3H8的平衡转化率与通入气体中C3H8的物质的量分数的关系如图所示。该条件下,C3H8的选择性为80%,则0~ 10 min内生成C3 H6的平均速率为_______ kPa·min-1;反应I的平衡常数 Kp=_______ kPa(以分压表示,分压=总压X物质的量分数,保留一位小数)。
(4)向恒温刚性密闭容器中通入一定体积比的C3H8、O2、N2的混合气体,已知某反应条件下只发生如下反应(k、k'为速率常数):
反应I :2C3H8(g) +O2(g)=2C3 H6(g) +2H2O(g) k
反应Ⅳ :2C3 H6(g) + 9O2 (g)=6CO2(g)+ 6H2O(g) k'
实验测得丙烯的净生成速率方程为v(C3 H6)=kp(C3H8)-k'p(C3H6),可推测丙烯的浓度随时间的变化趋势为_______ ,其理由是_______
(1)主反应I :C3H8(g)
 C3 H6(g)+H2(g) △H1
C3 H6(g)+H2(g) △H1副反应Ⅱ :C3H8(g)
 C2H4(g)+CH4(g) △H2
C2H4(g)+CH4(g) △H2已知H2、丙烷(C3H8 )和丙烯(C3 H6)的燃烧热(△H)分别是-285.8 kJ·mol-1、-2220 kJ·mol-1和-2051 kJ·mol-1,则△H=
(2)一定温度下,向总压恒定为p kPa的容器中充入一定量C3H8气体,在催化作用下,发生上述反应制备C3 H6。
①下列情况表明反应达到平衡状态的是
A.气体密度不再改变
B.体系压强不再改变
C.混合气体的平均摩尔质量不再改变
D.单位时间内消耗C3H8的物质的量与生成C3 H6的物质的量相等
②从平衡移动的角度判断,达到平衡后通入N2的作用是
(3)在温度为T时,向起始压强为120 kPa的恒压容器中通入4 mol C3H8和6 mol N2发生反应,经10 min反应达到平衡,C3H8的平衡转化率与通入气体中C3H8的物质的量分数的关系如图所示。该条件下,C3H8的选择性为80%,则0~ 10 min内生成C3 H6的平均速率为

(4)向恒温刚性密闭容器中通入一定体积比的C3H8、O2、N2的混合气体,已知某反应条件下只发生如下反应(k、k'为速率常数):
反应I :2C3H8(g) +O2(g)=2C3 H6(g) +2H2O(g) k
反应Ⅳ :2C3 H6(g) + 9O2 (g)=6CO2(g)+ 6H2O(g) k'
实验测得丙烯的净生成速率方程为v(C3 H6)=kp(C3H8)-k'p(C3H6),可推测丙烯的浓度随时间的变化趋势为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】(1)N2H4和H2O2混合可作火箭推进剂,已知:16g液态N2H4和足量氧气反应生成N2(g)和H2O(l),放出310.6kJ的热量;2H2O2(l)=O2(g)+2H2O(l) ΔH=-196.4kJ·mol-1。反应N2H4(g)+O2(g)=N2(g)+2H2O(l)的ΔH=__ kJ·mol-1。N2H4和H2O2反应生成N2(g)和H2O(l)的热化学方程式为__ 。
(2)已知拆开1mol氢气中的化学键需要消耗436kJ能量,拆开1mol氧气中的化学键需要消耗498kJ能量,根据下面的能量图,回答下列问题::
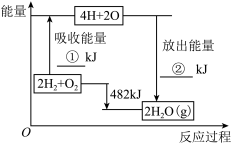
分别写出①、②的数值:①__ kJ;②__ kJ。
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1275.6kJ·mol-1
②H2O(l)=H2O(g) ΔH=+44.0kJ·mol-1
写出表示甲醇燃烧热的热化学方程式__ 。
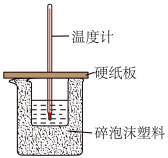
(4)实验室用50mL0.50mol·L-1盐酸与50mL某浓度的NaOH溶液在如图所示装置中反应,通过测定反应过程中所放出的热量可计算中和热。该装置有两处明显的错误,其中一处是缺少一种玻璃仪器,该仪器的名称为__ ;实验室提供了0.50mol·L-1和0.55mol·L-1两种浓度的NaOH溶液,应选择__ mol·L-1的NaOH溶液进行实验。
(2)已知拆开1mol氢气中的化学键需要消耗436kJ能量,拆开1mol氧气中的化学键需要消耗498kJ能量,根据下面的能量图,回答下列问题::

分别写出①、②的数值:①
(3)已知在常温常压下:
①2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g) ΔH=-1275.6kJ·mol-1
②H2O(l)=H2O(g) ΔH=+44.0kJ·mol-1
写出表示甲醇燃烧热的热化学方程式
(4)实验室用50mL0.50mol·L-1盐酸与50mL某浓度的NaOH溶液在如图所示装置中反应,通过测定反应过程中所放出的热量可计算中和热。该装置有两处明显的错误,其中一处是缺少一种玻璃仪器,该仪器的名称为

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)已知:A.金刚石、B.MgF2、C.NH4Cl、D.固体碘,用序号填写空白:既存在离子键又存在共价键的是______ ,熔化时不需破坏化学键的是______ 。
(2)意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如图所示,已知断裂1 molN-N键吸收167 kJ热量,生成1 molN≡N键放出942 kJ热量。根据以上信息和数据,则1molN4完全转化为N2______ (填“放出”或“吸收”)热量______ kJ。

(3)50 mL 0.50 mol/L的盐酸与50 mL0.55 mol/L的NaOH溶液在如图2所示的装置中进行中和反应。请回答下列问题:如图,烧杯间填满碎泡沫塑料的作用是______ 。大烧杯上如不盖硬纸板,则求得的中和热数值______ (填“偏大”、“偏小”或“无影响”)。
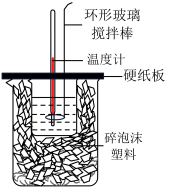
(4)向50mL0.50 mol/L的NaOH溶液中分别加入稀醋酸、稀盐酸、浓硫酸,则恰好完全反应时的放出热量Q1、Q2、Q3从大到小的排序是______ 。
(2)意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N4分子。N4分子结构如图所示,已知断裂1 molN-N键吸收167 kJ热量,生成1 molN≡N键放出942 kJ热量。根据以上信息和数据,则1molN4完全转化为N2

(3)50 mL 0.50 mol/L的盐酸与50 mL0.55 mol/L的NaOH溶液在如图2所示的装置中进行中和反应。请回答下列问题:如图,烧杯间填满碎泡沫塑料的作用是

(4)向50mL0.50 mol/L的NaOH溶液中分别加入稀醋酸、稀盐酸、浓硫酸,则恰好完全反应时的放出热量Q1、Q2、Q3从大到小的排序是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】化学反应伴随能量变化,获取反应能量变化有多条途径。
(1)下列反应中,属于放热反应的是_________ (填字母)。
A.碳与水蒸气反应 B.铝和氧化铁反应 C.CaCO3受热分解 D.氢气还原三氧化钨制取钨 E.锌与盐酸反应
(2)获取能量变化的途径
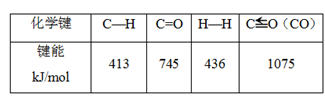
①通过化学键的键能计算。通常人们把断裂1mol某化学键所吸收的能量或形成1mol某化学键所释放的能量看作该化学键的键能,键能的大小可用于估算化学反应的反应热ΔH。已知部分化学键的键能数据如表所示:
则H2(g)+Cl2(g)=2HCl(g)的反应热ΔH为__________________________
②通过盖斯定律可计算。发射卫星用 作燃料,
作燃料, 作氧化剂,两者反应生成N2和水蒸气,已知:N2(g) +2O2(g)= 2NO2(g)△H1 =+67.7kJ/mol;N2H4(g)+O2(g)= N2(g)+2H2O(g) △H2=-534kJ/mol,写出气体肼和NO2气体反应生成N2和水蒸气的热化学方程式
作氧化剂,两者反应生成N2和水蒸气,已知:N2(g) +2O2(g)= 2NO2(g)△H1 =+67.7kJ/mol;N2H4(g)+O2(g)= N2(g)+2H2O(g) △H2=-534kJ/mol,写出气体肼和NO2气体反应生成N2和水蒸气的热化学方程式___________________________________________________
③利用实验装置测量利用下图图装置测定中和热的实验步骤如下:
回答下列问题:
I.仪器a的名称为______________________________
II.做了四次实验,并将实验数据记录如下:
近似认为0.55 mol/L NaOH溶液和0.25 mol/L硫酸溶液的密度都是1g/cm3,中和后生成溶液的比热容c=4.18 J/(g·℃),通过以上数据计算中和热ΔH=_________________ ( 结果保留小数点后一位)。
(1)下列反应中,属于放热反应的是
A.碳与水蒸气反应 B.铝和氧化铁反应 C.CaCO3受热分解 D.氢气还原三氧化钨制取钨 E.锌与盐酸反应
(2)获取能量变化的途径
①通过化学键的键能计算。通常人们把断裂1mol某化学键所吸收的能量或形成1mol某化学键所释放的能量看作该化学键的键能,键能的大小可用于估算化学反应的反应热ΔH。已知部分化学键的键能数据如表所示:
| 化学键 | H-H | Cl-Cl | H-Cl |
| 键能/(kJ·mol-1) | 436 | 243 | 431 |
②通过盖斯定律可计算。发射卫星用
 作燃料,
作燃料, 作氧化剂,两者反应生成N2和水蒸气,已知:N2(g) +2O2(g)= 2NO2(g)△H1 =+67.7kJ/mol;N2H4(g)+O2(g)= N2(g)+2H2O(g) △H2=-534kJ/mol,写出气体肼和NO2气体反应生成N2和水蒸气的热化学方程式
作氧化剂,两者反应生成N2和水蒸气,已知:N2(g) +2O2(g)= 2NO2(g)△H1 =+67.7kJ/mol;N2H4(g)+O2(g)= N2(g)+2H2O(g) △H2=-534kJ/mol,写出气体肼和NO2气体反应生成N2和水蒸气的热化学方程式③利用实验装置测量利用下图图装置测定中和热的实验步骤如下:
 | ①用量筒量取0.25mol/L的硫酸50mL倒入小烧杯中,测出硫酸溶液温度; ②用另一量筒量取50mL 0.55mol/L NaOH溶液,并用同一温度计测出其温度; ③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液的最高温度。 |
I.仪器a的名称为
II.做了四次实验,并将实验数据记录如下:
| 温度 实验次数 | 起始温度t1℃ | 终止温度t2/℃ | ||
| H2SO4 | NaOH | 平均值 | ||
| 1 | 26.2 | 26.0 | 26.1 | 29.5 |
| 2 | 27.0 | 27.4 | 27.2 | 32.3 |
| 3 | 25.9 | 25.9 | 25.9 | 29.2 |
| 4 | 26.4 | 26.2 | 26.3 | 29.8 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】合成氨工业中的原料气制取与净化是重要的环节。
(1)已知有关反应的能量变化如下图:
写出CH4(g)与H2O(g)反应制取CO(g)和H2(g)的热化学方程式:___________________ 。
(2)“CH4-CO2催化重整法”制氢气:CH4(g)+CO2(g) 2CO (g)+2H2(g),ΔH
2CO (g)+2H2(g),ΔH
不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。上述反应中相关的化学键键能数据如下表所示。①根据键能计算,该反应的ΔH=_______ kJ·mol-1。
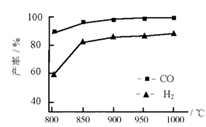
②按一定体积比加入CH4和CO2,在恒压下发生反应,温度对CO和H2产率的影响如图所示。实际生产中此反应优选温度为900℃,原因是_______________________ 。
③某温度下,将1 mol CH4、2 mol CO2以及催化剂进行加入2 L容器中,达到平衡时α(CH4)=50%,平衡常数K=____ mol2·L-2。
(3)合成气在进入合成塔前常用醋酸二氨合铜(Ⅰ)溶液来吸收其中的CO杂质,其反应是:Cu(NH3)2(CH3COO)+CO+NH3 Cu(NH3)3(CH3COO)·CO ΔH<0
Cu(NH3)3(CH3COO)·CO ΔH<0
必须除去原料气中CO的原因是_______________________ 。
醋酸二氨合铜(Ⅰ)吸收CO的生产适宜条件应是__________ (填序号)。
A.高温高压 B.高温低压 C.低温高压 D.低温低压
(1)已知有关反应的能量变化如下图:

写出CH4(g)与H2O(g)反应制取CO(g)和H2(g)的热化学方程式:
(2)“CH4-CO2催化重整法”制氢气:CH4(g)+CO2(g)
 2CO (g)+2H2(g),ΔH
2CO (g)+2H2(g),ΔH不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。上述反应中相关的化学键键能数据如下表所示。①根据键能计算,该反应的ΔH=
②按一定体积比加入CH4和CO2,在恒压下发生反应,温度对CO和H2产率的影响如图所示。实际生产中此反应优选温度为900℃,原因是
③某温度下,将1 mol CH4、2 mol CO2以及催化剂进行加入2 L容器中,达到平衡时α(CH4)=50%,平衡常数K=
(3)合成气在进入合成塔前常用醋酸二氨合铜(Ⅰ)溶液来吸收其中的CO杂质,其反应是:Cu(NH3)2(CH3COO)+CO+NH3
 Cu(NH3)3(CH3COO)·CO ΔH<0
Cu(NH3)3(CH3COO)·CO ΔH<0必须除去原料气中CO的原因是
醋酸二氨合铜(Ⅰ)吸收CO的生产适宜条件应是
A.高温高压 B.高温低压 C.低温高压 D.低温低压
您最近一年使用:0次
【推荐1】已知在1×105Pa、298K时断裂1molH—H键吸收的能量为436kJ,断裂1molN—H键吸收的能量为391kJ,断裂1molN≡N键吸收的能量是945kJ。
(1)根据以上数据判断工业合成氨的反应N2(g)+3H2(g)⇌2NH3(g)是_____ (填“吸热”或“放热”)反应。
(2)在298K时,取1molN2和3molH2放入一密闭容器中,加入催化剂进行反应。理论上完全反应放出或吸收的热量为Q1,则Q1为_____ kJ。
(3)实际生产中,放出或吸收的热量为Q2,Q1与Q2的大小系为_____
A.Q1<Q2B.Q1>Q2C.Q1=Q2
(1)根据以上数据判断工业合成氨的反应N2(g)+3H2(g)⇌2NH3(g)是
(2)在298K时,取1molN2和3molH2放入一密闭容器中,加入催化剂进行反应。理论上完全反应放出或吸收的热量为Q1,则Q1为
(3)实际生产中,放出或吸收的热量为Q2,Q1与Q2的大小系为
A.Q1<Q2B.Q1>Q2C.Q1=Q2
您最近一年使用:0次
【推荐2】比较下列各组热化学方程式中ΔH的大小关系。
(1)S(s)+O2(g)= SO2(g) ΔH1 S(g)+O2(g)=SO2(g) ΔH2 ΔH1______ ΔH2
(2)CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1 CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH2 ΔH1______ ΔH2
(3)煤作为燃料有两种途径:
途径1-直接燃烧
C(s)+O2(g)=CO2(g) ΔH1<0
途径2-先制水煤气
C(s)+H2O(g)=CO(g)+H2(g) ΔH2>0
再燃烧水煤气:
2CO(g)+O2(g)= 2CO2(g) ΔH3<0
2H2(g)+O2(g)= 2H2O(g) ΔH4<0
ΔH1、ΔH2、ΔH3、ΔH4的关系式是_______ 。
(1)S(s)+O2(g)= SO2(g) ΔH1 S(g)+O2(g)=SO2(g) ΔH2 ΔH1
(2)CH4(g)+2O2(g)=CO2(g)+2H2O(l) ΔH1 CH4(g)+2O2(g)=CO2(g)+2H2O(g) ΔH2 ΔH1
(3)煤作为燃料有两种途径:
途径1-直接燃烧
C(s)+O2(g)=CO2(g) ΔH1<0
途径2-先制水煤气
C(s)+H2O(g)=CO(g)+H2(g) ΔH2>0
再燃烧水煤气:
2CO(g)+O2(g)= 2CO2(g) ΔH3<0
2H2(g)+O2(g)= 2H2O(g) ΔH4<0
ΔH1、ΔH2、ΔH3、ΔH4的关系式是
您最近一年使用:0次
【推荐3】(1)同温同压下,H2(g)+Cl2(g)=2HCl(g),在光照和点燃条件下的ΔH(化学计量数相同)分别为ΔH1、ΔH2,则ΔH1___ ΔH2。(填“>”“<”或“=”)
(2)相同条件下,2mol氢原子所具有的能量___ 1mol氢分子所具有的能量。(填“>”“<”或“=”)
(3)已知常温下红磷比白磷稳定,比较下列反应中(反应条件均为点燃)ΔH的大小:ΔH1___ ΔH2。(填“>”“<”或“=”)
①P4(白磷,s)+5O2(g)=2P2O5(s)ΔH1,②4P(红磷,s)+5O2(g)=2P2O5(s)ΔH2。
(4)已知:101kPa时,2C(s)+O2(g)=2CO(g)ΔH=-221kJ·mol-1,则碳的燃烧热数值___ 110.5kJ·mol-1。(填“>”“<”或“=”)
(5)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式___ 。
(6)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)═2Al2O3(s)+3TiC(s)△H=-1176kJ·mol-1,则反应过程中,每转移1mol电子放出的热量为___ 。
(7)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H=+489.0kJ·mol-1,CO(g)+ O2(g)=CO2(g)△H=-283.0kJ·mol-1,C(石墨)+O2(g)=CO2(g)△H=-393.5kJ·mol-1,则4Fe(s)+3O2(g)=2Fe2O3(s)△H=
O2(g)=CO2(g)△H=-283.0kJ·mol-1,C(石墨)+O2(g)=CO2(g)△H=-393.5kJ·mol-1,则4Fe(s)+3O2(g)=2Fe2O3(s)△H=___ 。
(2)相同条件下,2mol氢原子所具有的能量
(3)已知常温下红磷比白磷稳定,比较下列反应中(反应条件均为点燃)ΔH的大小:ΔH1
①P4(白磷,s)+5O2(g)=2P2O5(s)ΔH1,②4P(红磷,s)+5O2(g)=2P2O5(s)ΔH2。
(4)已知:101kPa时,2C(s)+O2(g)=2CO(g)ΔH=-221kJ·mol-1,则碳的燃烧热数值
(5)使Cl2和H2O(g)通过灼热的炭层,生成HCl和CO2,当有1molCl2参与反应时释放出145kJ热量,写出该反应的热化学方程式
(6)火箭和导弹表面的薄层是耐高温物质。将石墨、铝粉和二氧化钛按一定比例混合在高温下煅烧,所得物质可作耐高温材料,4Al(s)+3TiO2(s)+3C(s)═2Al2O3(s)+3TiC(s)△H=-1176kJ·mol-1,则反应过程中,每转移1mol电子放出的热量为
(7)已知:Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)△H=+489.0kJ·mol-1,CO(g)+
 O2(g)=CO2(g)△H=-283.0kJ·mol-1,C(石墨)+O2(g)=CO2(g)△H=-393.5kJ·mol-1,则4Fe(s)+3O2(g)=2Fe2O3(s)△H=
O2(g)=CO2(g)△H=-283.0kJ·mol-1,C(石墨)+O2(g)=CO2(g)△H=-393.5kJ·mol-1,则4Fe(s)+3O2(g)=2Fe2O3(s)△H=
您最近一年使用:0次



