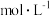10毫升0.1mol/L的XO4-离子恰好将15毫升0.1mol/L的亚硫酸钠氧化,则元素X在还原产物中的化合价为多少
| A.+1 | B.+2 | C.+3 | D.+4 |
更新时间:2017-02-23 21:00:52
|
【知识点】 基于氧化还原反应守恒规律的计算解读
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】某工厂排放的废水中含有氰化物,可在碱性条件下对氰化物进行净化处理:2CN-+8OH- +5Cl2=2CO2+N2+10Cl-+4H2O。下列分析中错误的是
| A.当反应消耗0.2 mol CN-时,反应中转移电子的物质的量是1 mol |
| B.还原性:CN->Cl- |
C.CN-的电子式为 |
| D.该反应中氧化剂和还原剂的物质的量之比是2∶5 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】已知溶液中,还原性HSO3>I-,氧化性IO3->I2。在含有3molNaHSO3的溶液中逐滴加入KIO3溶液,加入KIO3和析出I2的物质的量的关系如图所示,则下列说法中错误的是
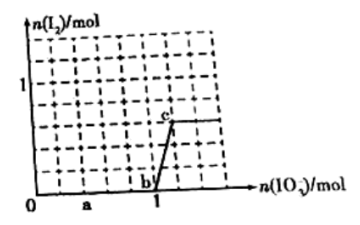

| A.a点时NaHSO3剩余 |
| B.b点时还原产物为I- |
| C.b点到c点,KIO3与NaHSO3反应生成I2 |
| D.加入的KIO3为0.4mol或1.12mol时,反应后溶液中I-均为0.4mol |
您最近一年使用:0次

 溶液中,金属恰好溶解,分别转化成
溶液中,金属恰好溶解,分别转化成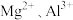 和
和 ;还原产物为NO,在标准状况下体积为6.72L。在反应后的溶液中加入300mL某浓度的NaOH溶液,金属阳离子恰好全部沉淀,干燥后测得质量为27.2g。下列有关推断正确的是
;还原产物为NO,在标准状况下体积为6.72L。在反应后的溶液中加入300mL某浓度的NaOH溶液,金属阳离子恰好全部沉淀,干燥后测得质量为27.2g。下列有关推断正确的是