在标准状况下,由CO和CO2组成的混合气体为6.72L,质量为12g。则:
(1)CO和CO2的物质的量之比是___________ 。
(2)CO的体积分数是___________ 。
(3)混合气体中所含氧原子的物质的量是___________ 。
(1)CO和CO2的物质的量之比是
(2)CO的体积分数是
(3)混合气体中所含氧原子的物质的量是
更新时间:2021-11-10 12:13:29
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】归纳、演绎和模型等是化学学习的重要方法,回答下列问题。
(1)元素的“价-类”二维图是学习元素及其化合物的重要工具。下图是部分硫及其化合物的“价-类”二维图。

根据图示回答下列问题:
①Y的化学式为_______ 。
②根据“价-类”二维图预测,下列能与 反应且
反应且 表现还原性的物质是
表现还原性的物质是_______ (填序号), 与其反应的离子方程式是
与其反应的离子方程式是_______ 。
a. b.酸性
b.酸性 溶液 c.
溶液 c. 溶液 d.
溶液 d. 溶液
溶液
③分析 的物质类别,写出它和过量NaOH溶液反应的离子方程式
的物质类别,写出它和过量NaOH溶液反应的离子方程式_______ 。
(2)欲制备 ,从氧化还原角度分析,合理的是
,从氧化还原角度分析,合理的是_______ (填序号)。
a. b.
b. c.
c. d.
d.
(3)一定条件下,1mol不同气体的质量和体积如下表所示:
分析表中数据,可得出温度、压强与气体体积关系的结论是_______ (写出两点即可)
(1)元素的“价-类”二维图是学习元素及其化合物的重要工具。下图是部分硫及其化合物的“价-类”二维图。

根据图示回答下列问题:
①Y的化学式为
②根据“价-类”二维图预测,下列能与
 反应且
反应且 表现还原性的物质是
表现还原性的物质是 与其反应的离子方程式是
与其反应的离子方程式是a.
 b.酸性
b.酸性 溶液 c.
溶液 c. 溶液 d.
溶液 d. 溶液
溶液③分析
 的物质类别,写出它和过量NaOH溶液反应的离子方程式
的物质类别,写出它和过量NaOH溶液反应的离子方程式(2)欲制备
 ,从氧化还原角度分析,合理的是
,从氧化还原角度分析,合理的是a.
 b.
b. c.
c. d.
d.
(3)一定条件下,1mol不同气体的质量和体积如下表所示:
化学式 | 质量 | 0℃、101kPa | 20℃、101kPa | 0℃、202kPa |
| 2g | 22.4L | 24.0L | 11.2L |
| 32g | 22.4L | 24.0L | 11.2L |
| 44g | 22.3L | 24.0L | 11.2L |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某液态化合物 ,在一定量
,在一定量 中恰好完全反应:
中恰好完全反应: 冷却后在标准状况下,测得生成物的体积为
冷却后在标准状况下,测得生成物的体积为 ,则(l表示液态,
,则(l表示液态, 表示气态):
表示气态):
(1)反应前 在标况下的体积是
在标况下的体积是___________  。
。
(2)在 分子中,X、Y两元素的质量比为
分子中,X、Y两元素的质量比为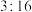 ,则X、Y两元素的相对原子质量之比为
,则X、Y两元素的相对原子质量之比为___________ 。
 ,在一定量
,在一定量 中恰好完全反应:
中恰好完全反应: 冷却后在标准状况下,测得生成物的体积为
冷却后在标准状况下,测得生成物的体积为 ,则(l表示液态,
,则(l表示液态, 表示气态):
表示气态):(1)反应前
 在标况下的体积是
在标况下的体积是 。
。(2)在
 分子中,X、Y两元素的质量比为
分子中,X、Y两元素的质量比为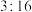 ,则X、Y两元素的相对原子质量之比为
,则X、Y两元素的相对原子质量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】Mg2Ni是一种储氢材料,2.14g Mg2Ni在一定条件下能吸收0.896LH2(标准状况下)生成X,X的化学式为_______________
您最近一年使用:0次
【推荐1】氧化还原反应原理在生产生活和科学研究中应用广泛。
(1)下列表述中没有氧化还原反应发生的是_____ 。
a.滴水成冰 b.蜡炬成灰 c.百炼成钢
(2)NH3和Cl2反应的方程式为:NH3+Cl2﹣N2+HCl
①该反应中被氧化的元素是_____ (填元素名称),氧化剂是_____ (填化学式)。
②配平该方程式:_____ NH3+_____ Cl2=_____ N2+_____ HCl
(3)“地康法”制氯气的反应原理图示如下:

①反应I的化学方程式为_____ 。
②若要制得标准状况下氯气11.2L,则整个反应中转移电子的物质的量为_____ 。
(1)下列表述中没有氧化还原反应发生的是
a.滴水成冰 b.蜡炬成灰 c.百炼成钢
(2)NH3和Cl2反应的方程式为:NH3+Cl2﹣N2+HCl
①该反应中被氧化的元素是
②配平该方程式:
(3)“地康法”制氯气的反应原理图示如下:

①反应I的化学方程式为
②若要制得标准状况下氯气11.2L,则整个反应中转移电子的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I.现有以下物质:①NaCl晶体②干冰③液态的醋酸④铜⑤BaSO4固体⑥蔗糖⑦酒精⑧熔融的KNO3⑨浓HNO3。回答下列问题(填序号)
(1)以上状态下能导电的是:__ 。
(2)以上物质属于非电解质的是:__ 。
(3)以上物质属于电解质的是:__ 。
(4)以上状态下的电解质不能导电的是:__ 。
(5)将1.42gNa2SO4溶于水中,要使每100个水分子中溶有1个Na+,则需水的质量为__ g。
(6)30gRO 中,核外电子总数比质子总数多6.02×1023个,则R的摩尔质量为
中,核外电子总数比质子总数多6.02×1023个,则R的摩尔质量为__ 。
(7)已知CO、CO2的混合气体质量共16.0g,标准状况下体积为8.96L,则可推知该混合气体中所含CO2在标准状况下的体积为__ L。
(8)同温同压下,NH3和H2S气体的密度比是__ ,同温同密度同体积的NH3和H2S气体中所含H原子个数比是___ 。
(1)以上状态下能导电的是:
(2)以上物质属于非电解质的是:
(3)以上物质属于电解质的是:
(4)以上状态下的电解质不能导电的是:
(5)将1.42gNa2SO4溶于水中,要使每100个水分子中溶有1个Na+,则需水的质量为
(6)30gRO
 中,核外电子总数比质子总数多6.02×1023个,则R的摩尔质量为
中,核外电子总数比质子总数多6.02×1023个,则R的摩尔质量为(7)已知CO、CO2的混合气体质量共16.0g,标准状况下体积为8.96L,则可推知该混合气体中所含CO2在标准状况下的体积为
(8)同温同压下,NH3和H2S气体的密度比是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ⅰ.认真观察下图,回答问题:
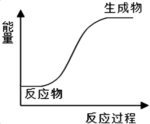

(1)图中所示反应是___________ (填“吸热”或“放热”)反应。
(2)已知拆开1mol H—H键、1mol Cl—Cl、1mol H—Cl键分别需要吸收的能量为436kJ、243kJ、431kJ,则由1mol氢气和1mol 氯气反应生成2mol HCl会___________ (填“放出”或“吸收”)___________ kJ的热量。
(3)下列反应中,属于放热反应的是___________ 。
① 物质燃烧 ② 炸药爆炸 ③ 煅烧石灰石 ④二氧化碳通过炽热的碳 ⑤ 酸碱中和反应 ⑥ Ba(OH)2·8H2O与NH4Cl晶体反应 ⑦浓硫酸稀释
Ⅱ.燃料电池是一种高效供能装置,上右图所示为甲烷燃料工作原理示意图。请回答下列问题:
(4)a电极为电池的___________ (填“正极”或“负极”),电解质溶液中Na+流向___________ 极 (填“a”或“b”)。
(5)写出a电极反应式:___________ 。
Ⅲ.(6)为了检测熟肉中NaNO2含量,某兴趣小组从1000g隔夜熟肉中提取NaNO3和NaNO2后配成溶液,用0.005 mol/L的酸性高锰酸钾溶液滴定。反应原理为:2MnO +5NO
+5NO +6H+=2Mn2++5 NO
+6H+=2Mn2++5 NO +3H2O。测定三次消耗高锰酸钾溶液平均体积为8.00 mL。则NaNO2含量为
+3H2O。测定三次消耗高锰酸钾溶液平均体积为8.00 mL。则NaNO2含量为___________ mg•kg-1。


(1)图中所示反应是
(2)已知拆开1mol H—H键、1mol Cl—Cl、1mol H—Cl键分别需要吸收的能量为436kJ、243kJ、431kJ,则由1mol氢气和1mol 氯气反应生成2mol HCl会
(3)下列反应中,属于放热反应的是
① 物质燃烧 ② 炸药爆炸 ③ 煅烧石灰石 ④二氧化碳通过炽热的碳 ⑤ 酸碱中和反应 ⑥ Ba(OH)2·8H2O与NH4Cl晶体反应 ⑦浓硫酸稀释
Ⅱ.燃料电池是一种高效供能装置,上右图所示为甲烷燃料工作原理示意图。请回答下列问题:
(4)a电极为电池的
(5)写出a电极反应式:
Ⅲ.(6)为了检测熟肉中NaNO2含量,某兴趣小组从1000g隔夜熟肉中提取NaNO3和NaNO2后配成溶液,用0.005 mol/L的酸性高锰酸钾溶液滴定。反应原理为:2MnO
 +5NO
+5NO +6H+=2Mn2++5 NO
+6H+=2Mn2++5 NO +3H2O。测定三次消耗高锰酸钾溶液平均体积为8.00 mL。则NaNO2含量为
+3H2O。测定三次消耗高锰酸钾溶液平均体积为8.00 mL。则NaNO2含量为
您最近一年使用:0次





