某学生为探究 的影响因素,做了以下实验。
的影响因素,做了以下实验。
(1)查阅资料,不同温度下水的离子积常数如表所示。
由此推出:随着温度的升高, 的值
的值___________ (填“增大”“减小”或“不变”,下同);水的电离程度___________ ;水的电离平衡向___________ (填“左”或“右”)移动,水的电离过程是___________ (填“吸热”或“放热”)过程。
(2)取三只烧杯A、B、C,分别加入适量水,再向B、C烧杯中分别加入少量盐酸和NaOH溶液,分析并填写下表。
综上所述,可得出如下结论:
①温度、___________ 、___________ 均能影响水的电离平衡。
② 只受
只受___________ 的影响,而与其他因素无关。
 的影响因素,做了以下实验。
的影响因素,做了以下实验。(1)查阅资料,不同温度下水的离子积常数如表所示。
 | 0 | 10 | 20 | 25 | 40 | 50 | 90 | 100 |
 | 0.115 | 0.296 | 0.687 | 1.01 | 2.87 | 5.31 | 37.1 | 54.5 |
 的值
的值(2)取三只烧杯A、B、C,分别加入适量水,再向B、C烧杯中分别加入少量盐酸和NaOH溶液,分析并填写下表。
| A(纯水) | B(加少量盐酸) | C(加少量NaOH溶液) | |
 |  | 增大 | |
 |  | 增大 | |
 和 和 大小比较 大小比较 | 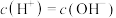 |   |   |
| 水的电离平衡移动方向 | |||
 | 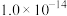 |
①温度、
②
 只受
只受
2018高二·全国·专题练习 查看更多[8]
3.1.2水的电离平衡 课后(已下线)3.1.4 水的电离平衡(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)(已下线)3.2.1 水的电离 溶液的酸碱性(基础过关A练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)3.2.1 水的电离-2021-2022学年高二化学课后培优练(人教版选修4)(已下线)3.1.3 水的电离平衡-2021-2022学年高二化学课后培优练(苏教版2019选择性必修1)选择性必修1(SJ)专题3第一单元课时3 水的电离人教版(2019)高二化学选择性必修1第三章 水溶液中的离子反应与平衡 第二节 水的电离和溶液的pH 课时1 水的电离高二人教版选修4 第三章 第二节 水的电离和溶液的酸碱性
更新时间:2021-12-06 12:40:42
|
相似题推荐
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】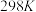 时,酸HA的电离平衡常数
时,酸HA的电离平衡常数 ,水的离子积
,水的离子积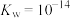 .试计算,在该温度下:
.试计算,在该温度下:
(1) 的HA溶液中,由水电离产生的
的HA溶液中,由水电离产生的
_____ ;
(2) 的NaA溶液中
的NaA溶液中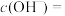
_____________
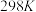 时,酸HA的电离平衡常数
时,酸HA的电离平衡常数 ,水的离子积
,水的离子积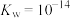 .试计算,在该温度下:
.试计算,在该温度下:(1)
 的HA溶液中,由水电离产生的
的HA溶液中,由水电离产生的
(2)
 的NaA溶液中
的NaA溶液中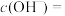
您最近半年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】已知水的电离平衡曲线如图所示,试回答下列问题:
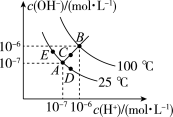
(1)图中A、B、C、D、E五点的KW间的大小关系是______ 。(用A、B、C、D、E表示)
(2)若从A点到D点,可采用的措施是___________ 。
a.升温 b.加入少量的盐酸 c.加入少量的NaOH固体
(3)点B对应温度条件下,某溶液pH═7,此时,溶液呈_______ (酸性、碱性、中性)。

(1)图中A、B、C、D、E五点的KW间的大小关系是
(2)若从A点到D点,可采用的措施是
a.升温 b.加入少量的盐酸 c.加入少量的NaOH固体
(3)点B对应温度条件下,某溶液pH═7,此时,溶液呈
您最近半年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】下表是不同温度下水的离子积:
请回答下列问题:
(1)若25<t1<t2,则a_____ 1×10-14(填“>”“<”或“=”)。
(2)25℃下,已知某Na2SO4溶液中,c( )=5×10-4mol/L。取该溶液1mL,加水稀释至10mL,则稀释后溶液中c(
)=5×10-4mol/L。取该溶液1mL,加水稀释至10mL,则稀释后溶液中c( ):c(Na+)=
):c(Na+)=_____ ,c(OH-):c(Na+)=_____ 。
(3)t2℃下,pH=2的稀硫酸中,水电离产生的c(H+)=_____ mol/L。
(4)t2℃下,将pH=12的氢氧化钠溶液V1L与pH=1的稀硫酸V2L混合(忽略反应前后溶液体积的变化),所得混合溶液的pH=2,则V1:V2=_____ 。
| 温度/℃ | 25 | t1 | t2 |
| 水的离子积 | 1×10-14 | a | 1×10-13 |
请回答下列问题:
(1)若25<t1<t2,则a
(2)25℃下,已知某Na2SO4溶液中,c(
 )=5×10-4mol/L。取该溶液1mL,加水稀释至10mL,则稀释后溶液中c(
)=5×10-4mol/L。取该溶液1mL,加水稀释至10mL,则稀释后溶液中c( ):c(Na+)=
):c(Na+)=(3)t2℃下,pH=2的稀硫酸中,水电离产生的c(H+)=
(4)t2℃下,将pH=12的氢氧化钠溶液V1L与pH=1的稀硫酸V2L混合(忽略反应前后溶液体积的变化),所得混合溶液的pH=2,则V1:V2=
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐2】已知水的电离平衡曲线如图所示:回答下列问题:A、B、C、D四点Kw的关系是_______ .( …表示)。
…表示)。
 …表示)。
…表示)。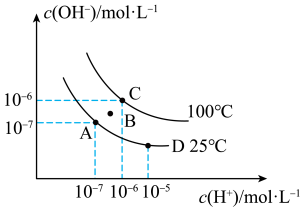
您最近半年使用:0次
填空题
|
较易
(0.85)
【推荐3】化学知识在生产和生活中处处都有体现,请用化学知识解释。
(1)冰箱能够在一定时间内保鲜食物,原因是_____ 。
(2)乳酸饮料(含乳酸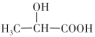 )显酸性的原因是
)显酸性的原因是_____ (用电离方程式表示)。
(3)工业上合成氨气时总是及时分离出反应器中的氨气,这样做的原因是_____ 。
(4)燃气灶具进风口通入的空气总是适当过量,这是为了_____ 。
(5)接近沸腾的纯净水pH<7,原因是_____ 。
(1)冰箱能够在一定时间内保鲜食物,原因是
(2)乳酸饮料(含乳酸
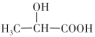 )显酸性的原因是
)显酸性的原因是(3)工业上合成氨气时总是及时分离出反应器中的氨气,这样做的原因是
(4)燃气灶具进风口通入的空气总是适当过量,这是为了
(5)接近沸腾的纯净水pH<7,原因是
您最近半年使用:0次

 的硫酸溶液中由水电离出的
的硫酸溶液中由水电离出的 。
。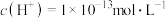 的
的 溶液中,
溶液中,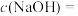
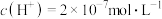 ,则此时纯水的
,则此时纯水的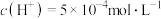 ,则溶液中
,则溶液中

