镁及其化合物在现代工业、国防建设中有着广泛的应用。回答下列问题:
(1)单质镁在空气中燃烧的主要产物是白色的___________ ,还生成少量的___________ (填化学式)。
(2)CH3MgCl是一种重要的有机合成剂,其中镁的化合价为___________ ,CH3MgCl水解时除生成甲烷外,还生成一种碱和一种盐。写出该反应的化学方程式:___________ 。
(3)Mg(OH)2是常用的阻燃材料。以白云石(CaCO3、MgCO3,不考虑杂质)为原料制备Mg(OH)2和CaCO3的工艺流程如下:

“煅烧”时称取27.6g白云石,高温加热到质量不再变化,收集到的CO2为6.72L(标准状况下),若工艺中不考虑Ca、Mg损失,则Mg(OH)2和CaCO3的质量分别为___________ 、___________ 。
(1)单质镁在空气中燃烧的主要产物是白色的
(2)CH3MgCl是一种重要的有机合成剂,其中镁的化合价为
(3)Mg(OH)2是常用的阻燃材料。以白云石(CaCO3、MgCO3,不考虑杂质)为原料制备Mg(OH)2和CaCO3的工艺流程如下:

“煅烧”时称取27.6g白云石,高温加热到质量不再变化,收集到的CO2为6.72L(标准状况下),若工艺中不考虑Ca、Mg损失,则Mg(OH)2和CaCO3的质量分别为
更新时间:2021-11-04 14:25:40
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】氯水和漂白粉都有漂白作用,也可用于水体的杀菌消毒。
(1)漂白粉在空气中容易变质的原因为(用化学方程式表示)___________ ,___________ 。
实验室制取氯气并研究氯气的性质。回答下列问题:
(2)实验室用MnO2固体和浓盐酸反应制备氯气的化学方程式为___________ 。
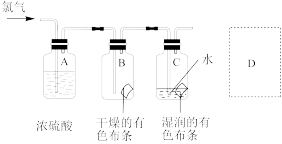
(3)某同学设计了如图实验装置进一步研究氯气的漂白性,已知通入的氯气中还含有空气和水蒸气。浓H2SO4的作用是___________ ,该实验设计存在事故隐患,应在D处增加一装置,若D装置为干燥管,则盛放的试剂名称为___________ 。
(4)如图中四条直线分别表示钠、镁、铝、铁和足量Cl2反应时消耗金属的质量(纵轴)与反应消耗氯气的质量(横轴)的关系,其中代表钠与Cl2反应的直线是___________ ,代表铁与Cl2反应的直线是___________ 。

(5)一定温度下,将氯气通入200 mL 3.0 mo/L的KOH溶液中,得到KCl、KClO、KClO3三种含氯产物,其中KCl与KClO3的物质的量之比为8:1,则得到的KClO质量为___________ g(结果保留1位小数)。
(1)漂白粉在空气中容易变质的原因为(用化学方程式表示)
实验室制取氯气并研究氯气的性质。回答下列问题:
(2)实验室用MnO2固体和浓盐酸反应制备氯气的化学方程式为
(3)某同学设计了如图实验装置进一步研究氯气的漂白性,已知通入的氯气中还含有空气和水蒸气。浓H2SO4的作用是

(4)如图中四条直线分别表示钠、镁、铝、铁和足量Cl2反应时消耗金属的质量(纵轴)与反应消耗氯气的质量(横轴)的关系,其中代表钠与Cl2反应的直线是

(5)一定温度下,将氯气通入200 mL 3.0 mo/L的KOH溶液中,得到KCl、KClO、KClO3三种含氯产物,其中KCl与KClO3的物质的量之比为8:1,则得到的KClO质量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】某兴趣小组利用废旧电池的铜帽(铜锌总含量约99%)制备了 样品,制备流程如下:
样品,制备流程如下:

(1)“溶解Ⅱ”过程中,发生反应的离子方程式为_______ 。
(2)“溶解Ⅱ”过程中应控制反应温度,温度不能过高的原因是_______ 。
(3)为测定所得 样品的纯度,兴趣小组进行了如下实验:称取3.00g样品,配制成250mL溶液,取25.00mL溶液于锥形瓶中,加入过量KI并充分振荡后,滴加几滴淀粉溶液,再滴入0.04mol/L的
样品的纯度,兴趣小组进行了如下实验:称取3.00g样品,配制成250mL溶液,取25.00mL溶液于锥形瓶中,加入过量KI并充分振荡后,滴加几滴淀粉溶液,再滴入0.04mol/L的 溶液至刚好完全反应,恰好完全反应时消耗
溶液至刚好完全反应,恰好完全反应时消耗 溶液的体积为25.00mL。实验过程中发生的反应如下:
溶液的体积为25.00mL。实验过程中发生的反应如下: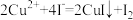 、
、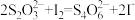
①配制250mL溶液所需的玻璃仪器除烧杯、玻璃棒外还有_______ 。
②计算出样品中 的质量分数。(写出计算过程)
的质量分数。(写出计算过程)_____
 样品,制备流程如下:
样品,制备流程如下:
(1)“溶解Ⅱ”过程中,发生反应的离子方程式为
(2)“溶解Ⅱ”过程中应控制反应温度,温度不能过高的原因是
(3)为测定所得
 样品的纯度,兴趣小组进行了如下实验:称取3.00g样品,配制成250mL溶液,取25.00mL溶液于锥形瓶中,加入过量KI并充分振荡后,滴加几滴淀粉溶液,再滴入0.04mol/L的
样品的纯度,兴趣小组进行了如下实验:称取3.00g样品,配制成250mL溶液,取25.00mL溶液于锥形瓶中,加入过量KI并充分振荡后,滴加几滴淀粉溶液,再滴入0.04mol/L的 溶液至刚好完全反应,恰好完全反应时消耗
溶液至刚好完全反应,恰好完全反应时消耗 溶液的体积为25.00mL。实验过程中发生的反应如下:
溶液的体积为25.00mL。实验过程中发生的反应如下: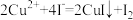 、
、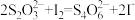
①配制250mL溶液所需的玻璃仪器除烧杯、玻璃棒外还有
②计算出样品中
 的质量分数。(写出计算过程)
的质量分数。(写出计算过程)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】加碘盐的推广让我国基本杜绝了“碘缺乏症”,我国在部分缺铁人群中又推广了“加铁盐”。某学习小组进行实验探究一种加铁盐(成分表中加铁成分为FeSO4,加碘成分为KIO3)的成分。
(1)配制溶液:准确称量10.00g该加铁盐,配制100mL加铁盐溶液。需要使用的玻璃仪器:烧杯、玻璃棒、____ 、____ 。
(2)离子检验:
①用洁净的铂丝蘸取溶液,灼烧铂丝,直接观察火焰呈黄色,甲同学认为含Na+,盐中未加KIO3,该加铁盐与宣传不符。“但乙同学进行实验,____ ,观察到火焰呈紫色,否定了甲同学的观点。
②另取适量溶液于试管中,先加入____ ,静置,用胶头滴管取上层清液于另一试管中,加足量稀硝酸和几滴____ 溶液,有白色沉淀,说明溶液中有Cl-。
(3)检验加铁成分:实验小组设计了以下实验,请完成表格。
(4)加铁盐国标是:含铁量为600-1000毫克每千克,含碘量不小于40毫克每千克。
定量测定:取20mL所配溶液,加入足量NaOH溶液,现象是____ ,充分反应后过滤,加热固体至质量不再变化,用分析天平称量剩余红色固体2.40mg,通过计算说明该加铁盐含铁量是否达标____ (请在答题卡写出计算过程)。
(1)配制溶液:准确称量10.00g该加铁盐,配制100mL加铁盐溶液。需要使用的玻璃仪器:烧杯、玻璃棒、
(2)离子检验:
①用洁净的铂丝蘸取溶液,灼烧铂丝,直接观察火焰呈黄色,甲同学认为含Na+,盐中未加KIO3,该加铁盐与宣传不符。“但乙同学进行实验,
②另取适量溶液于试管中,先加入
(3)检验加铁成分:实验小组设计了以下实验,请完成表格。
| 步骤 | 操作 | 现象 | 结论 |
| 步骤1 | 取所配溶液,加入 | 无明显现象 | 溶液中存在Fe2+,且未变质 |
| 步骤2 | 继续向溶液中加入 |
定量测定:取20mL所配溶液,加入足量NaOH溶液,现象是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某含砷(As )的有毒工业废水经如下图流程转化为粗Aa2O3。已知:亚砷酸钙微溶于水,砷酸钙难溶于水。

(1)加入试剂1的目的是:_________________________ 。
(2)“沉砷”是将砷元素转化为Ca5(AsO4)3OH 沉淀,发生的主要反应有:
A.Ca(OH)2(s) Ca2+(aq) + 2OH-(aq) ΔH <0
Ca2+(aq) + 2OH-(aq) ΔH <0
B.5Ca2+ + OH-+ 3AsO43- Ca5(AsO4)3OH ΔH >0
Ca5(AsO4)3OH ΔH >0
研究表明:“沉砷”的最佳温度是85℃, 用化学平衡原理解释温度高于85℃后,随温度升高沉淀率下降的原因是________ 。
(3)“还原”过程中H3AsO4转化为H3AsO3,反应的化学方程式是________ 。
(4)通过对H3AsO3溶液进行_____ (填操作名称),再过滤可制得粗As2O3。As2O3在不同温度和不同浓度硫酸中的溶解度(S)曲线如下图所示。为控制滤液2 中As2O3的浓度不高于6×10-5 mol·L-1 ,则“结晶”过程应控制的条件是______________________ (例举一例回答)
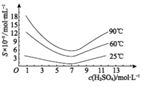
(5)从绿色化学和综合利用的角度考虑,对滤液2 处理方法是:________________________ 。

(1)加入试剂1的目的是:
(2)“沉砷”是将砷元素转化为Ca5(AsO4)3OH 沉淀,发生的主要反应有:
A.Ca(OH)2(s)
 Ca2+(aq) + 2OH-(aq) ΔH <0
Ca2+(aq) + 2OH-(aq) ΔH <0B.5Ca2+ + OH-+ 3AsO43-
 Ca5(AsO4)3OH ΔH >0
Ca5(AsO4)3OH ΔH >0研究表明:“沉砷”的最佳温度是85℃, 用化学平衡原理解释温度高于85℃后,随温度升高沉淀率下降的原因是
(3)“还原”过程中H3AsO4转化为H3AsO3,反应的化学方程式是
(4)通过对H3AsO3溶液进行

(5)从绿色化学和综合利用的角度考虑,对滤液2 处理方法是:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】通过海水晾晒可得粗盐,粗盐除NaCl外,还含有MgCl2、CaCl2、Na2SO4以及泥沙等杂质。以下是制备精盐的实验方案,各步操作流程如下:

(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是___ 。
(2)第②步操作的目的是除去粗盐中的___ (填化学式,下同),第⑥步操作的目的是除去滤液中___ 。
(3)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、___ 、___ (填化学式),写出操作②和操作③的相关化学方程式___ 、___ 。
(4)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是___ 。

(1)在第①步粗盐溶解操作中要用玻璃棒搅拌,作用是
(2)第②步操作的目的是除去粗盐中的
(3)第⑤步“过滤”操作中得到沉淀的成分有:泥沙、BaSO4、Mg(OH)2、
(4)在第③步操作中,选择的除杂的试剂不能用KOH代替NaOH,理由是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】实验室以一种工业废渣(主要成分为MgCO3、Mg2SiO4和少量Fe、Al的氧化物)为原料制备Al2O3和MgCO3。已知溶液中pH=8.5时Mg2+开始沉淀;pH=5.0时Al3+沉淀完全。实验过程如图:
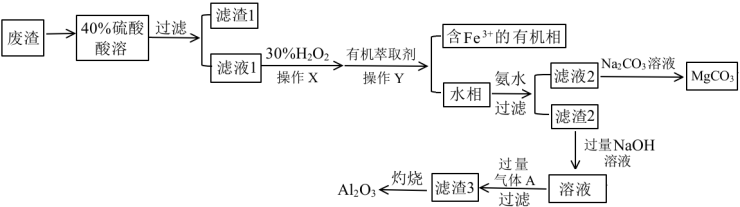
(1)操作X中加入H2O2氧化时发生发应的离子方程式为___ 。
(2)通入过量的气体A时,发生的离子反应为___ 。
(3)操作Y可采取的相关操作:向装有水溶液的___ (填仪器名称)中加入一定量的有机萃取剂,振荡、静置、分液,并重复多次。多次萃取后,取水相,加入适量氨水调节pH至___ 。某次实验,水相中加入一定量氨水后,取100mL溶液进行分析。该溶液中滴加1mol/L的氢氧化钠溶液,所得沉淀物质的量和加入氢氧化钠的体积关系如图所示,最后剩余固体质量为2.9g,原100mL溶液中主要存在的阳离子有:___ (忽略残留的微量铁离子),其中Mg2+和Al3+的物质的量之比为___ 。

(4)①工业上还可以用氧化铝直接和氯气在高温下反应制备无水氯化铝,反应方程式为:___ 。
②实际生产中需要加入一定量焦炭,其原因是___ ,试推断加入一定量焦炭反应后,产物中可能生成的气体成分为:___ 。
(5)加入碳酸钠溶液沉淀镁离子过程中,判断镁离子已沉淀完全的操作为:___ 。

(1)操作X中加入H2O2氧化时发生发应的离子方程式为
(2)通入过量的气体A时,发生的离子反应为
(3)操作Y可采取的相关操作:向装有水溶液的

(4)①工业上还可以用氧化铝直接和氯气在高温下反应制备无水氯化铝,反应方程式为:
②实际生产中需要加入一定量焦炭,其原因是
(5)加入碳酸钠溶液沉淀镁离子过程中,判断镁离子已沉淀完全的操作为:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
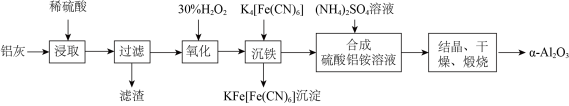
【推荐1】以冶铝的废弃物铝灰为原料制取超细α氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为Al2O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如下图:
(1)写出铝灰与氢氧化钠溶液反应涉及的化学方程式:_______________________ 。
(2)加30%H2O2溶液发生的离子反应方程式为______________________________ 。
(3)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)2·12H2O]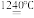 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过下图所示的装置。
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过下图所示的装置。
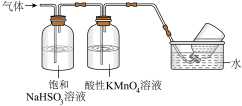
集气瓶中收集到的气体是_______ (填化学式)。
②酸性KMnO4溶液紫色变浅_______ (填“能”或“不能”)说明煅烧硫酸铝铵晶体产物中含有SO2气体?理由:______ 。
(1)写出铝灰与氢氧化钠溶液反应涉及的化学方程式:
(2)加30%H2O2溶液发生的离子反应方程式为
(3)煅烧硫酸铝铵晶体,发生的主要反应为:4[NH4Al(SO4)2·12H2O]
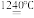 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过下图所示的装置。
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,将产生的气体通过下图所示的装置。
集气瓶中收集到的气体是
②酸性KMnO4溶液紫色变浅
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】氯化亚铜(CuCl)是重要的化工原料,广泛用作有机合成催化剂。
资料
1.水溶液中存在平衡:2Cl-(aq)+CuCl(s) CuCl
CuCl (aq)。
(aq)。
2.CuCl是难溶于水的白色固体,在热水中迅速水解生成Cu2O。
3.CuCl在潮湿的空气中易被氧化,生成的碱式盐为Cu2(OH)3Cl。
Ⅰ.实验室中用纯净的CuCl2固体可制备CuCl。取75gCuCl2固体于烧杯中,加入100mL0.2mol/L盐酸和水配成200mL溶液,然后在溶液中通入SO2气体。
(1)结合化学用语解释加入盐酸的主要目的是___ 。
(2)溶液中通入SO2气体后,发生反应的离子方程式为___ 。
Ⅱ.工业中,用初级铜矿粉(主要含Cu2S及少量Fe2O3、FeO等)为原料制备CuCl。流程如图:

(3)“酸浸”中,加入稀H2SO4不宜过量太多的原因是__ 。
(4)用化学用语解释,析出的CuCl晶体不能用水洗涤的原因是___ 。
(5)合成过程中适宜的反应条件为___ 。
(6)若要制99.5gCuCl,理论上至少需要含Cu2S50%的铜矿粉的质量为___ g。
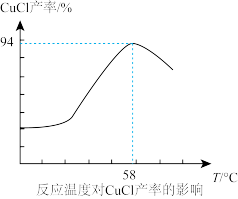
(7)相同时间内,反应物在最佳配比条件下,温度对CuCl产率影响如图所示。溶液温度控制在58℃时,CuCl产率最大,随温度升高CuCl产率降低,其原因是__ 。(答出2条即可)
资料
1.水溶液中存在平衡:2Cl-(aq)+CuCl(s)
 CuCl
CuCl (aq)。
(aq)。2.CuCl是难溶于水的白色固体,在热水中迅速水解生成Cu2O。
3.CuCl在潮湿的空气中易被氧化,生成的碱式盐为Cu2(OH)3Cl。
Ⅰ.实验室中用纯净的CuCl2固体可制备CuCl。取75gCuCl2固体于烧杯中,加入100mL0.2mol/L盐酸和水配成200mL溶液,然后在溶液中通入SO2气体。
(1)结合化学用语解释加入盐酸的主要目的是
(2)溶液中通入SO2气体后,发生反应的离子方程式为
Ⅱ.工业中,用初级铜矿粉(主要含Cu2S及少量Fe2O3、FeO等)为原料制备CuCl。流程如图:

(3)“酸浸”中,加入稀H2SO4不宜过量太多的原因是
(4)用化学用语解释,析出的CuCl晶体不能用水洗涤的原因是
(5)合成过程中适宜的反应条件为
(6)若要制99.5gCuCl,理论上至少需要含Cu2S50%的铜矿粉的质量为
(7)相同时间内,反应物在最佳配比条件下,温度对CuCl产率影响如图所示。溶液温度控制在58℃时,CuCl产率最大,随温度升高CuCl产率降低,其原因是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】草酸亚铁晶体(FeC2O4•2H2O)是一种浅黄色固体,难溶于水,受热易分解,是生产锂电池的原材料,也常用作分析试剂及显影剂等,其制备流程如下:
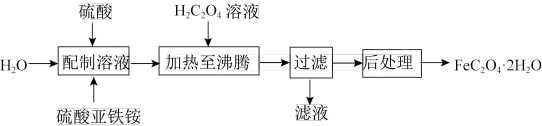
(1)配制硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液时,除需加硫酸外还需要加少量铁屑的目的是________ 。
(2)加热至沸腾生成沉淀时反应的化学方程式为________________________ 。
(3)向盛有草酸亚铁晶体的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现溶液的颜色由紫红色变为棕黄色,同时有气体生成.这说明草酸亚铁晶体具有________ (填“氧化”或“还原”)性.若反应中消耗1mol FeC2O4•2H2O,则参加反应的n(KMnO4)为________ 。
(4)称取3.60g草酸亚铁晶体(摩尔质量是180g•mol﹣1)用热重法对其进行热分解,得到剩余固体质量随温度变化的曲线如图所示:

①过程Ⅰ发生反应的化学方程式为________________________ 。
②300℃时剩余固体是铁的一种氧化物,试通过计算确定该氧化物的化学式___________ (写出计算过程)

(1)配制硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液时,除需加硫酸外还需要加少量铁屑的目的是
(2)加热至沸腾生成沉淀时反应的化学方程式为
(3)向盛有草酸亚铁晶体的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现溶液的颜色由紫红色变为棕黄色,同时有气体生成.这说明草酸亚铁晶体具有
(4)称取3.60g草酸亚铁晶体(摩尔质量是180g•mol﹣1)用热重法对其进行热分解,得到剩余固体质量随温度变化的曲线如图所示:

①过程Ⅰ发生反应的化学方程式为
②300℃时剩余固体是铁的一种氧化物,试通过计算确定该氧化物的化学式
您最近一年使用:0次



