回答下列问题:
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填标号)。
(2)近年来我国科学家发现了一系列意义重大的铁系超导材料,其中一类为FeSmAsFO组成的化合物。回答下列问题:
①Fe成为阳离子时首先失去___________ 轨道电子,Sm的价层电子排布式为4f66s2,Sm3+价层电子排布式为___________ 。
②比较离子半径:F___________ O2-(填“大于”“等于”或“小于”)。
(3)在周期表中,与Li的化学性质最相似的邻族元素是___________ ,该元素基态原子核外M层电子的自旋状态___________ (填“相同”或“相反”)。
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是___________(填标号)。
A.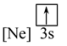 | B.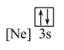 | C.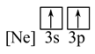 | D.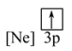 |
①Fe成为阳离子时首先失去
②比较离子半径:F
(3)在周期表中,与Li的化学性质最相似的邻族元素是
2021高三·全国·专题练习 查看更多[1]
(已下线)考向36 原子结构与性质-备战2022年高考化学一轮复习考点微专题
更新时间:2021/12/09 07:07:51
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】有下列四种微粒:①168O、②2311Na、③2412Mg、④14 7N
(1)按原子半径由大到小顺序排列的是___________________ (用序号回答,下同)
(2)微粒中质子数小于中子数的是______________________________
(3)在化合物中呈现的化合价的数值最多的是____________________
(4)能形成X2Y2型化合物的是___________ 。
(1)按原子半径由大到小顺序排列的是
(2)微粒中质子数小于中子数的是
(3)在化合物中呈现的化合价的数值最多的是
(4)能形成X2Y2型化合物的是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】K+与Cl-具有相同的核外电子排布,r(K+)小于r(Cl-),原因是___________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】在短周期元素中,(均用化学符号表示)
(1)常温下有颜色的气体单质有_______________________ ;
(2)除稀有气体外,原子半径最大的元素是______________ ;最小的元素是______________ 。
(3)气态氢化物中最稳定的是_______________ ,其水溶液呈碱性的元素是__________________ 。
(4)在最高价氧化物中,化合价最高的元素是____________________ ;
(5)地壳中含量最多的元素______________________ 。
(1)常温下有颜色的气体单质有
(2)除稀有气体外,原子半径最大的元素是
(3)气态氢化物中最稳定的是
(4)在最高价氧化物中,化合价最高的元素是
(5)地壳中含量最多的元素
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】硅是典型的半导体元素,在电子、材料等领域应用广泛。请回答下列问题。
(1)基态硅(Si)原子的核外电子排布式为[Ne]_______ ,有_______ 个未成对电子。
(2)碳(C)、硅(Si)、锗(Ge)是同族元素。
①C的基态原子核外电子排布式为_______ ;基态C原子核外电子的空间运动状态有_______ 种。
②基态Ge原子的核外电子占据_______ 个能层、_______ 个能级。
③Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______ ,微粒之间存在的相互作用是_______ 。
④Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是_______ 。
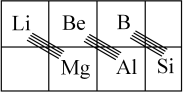
(3)在元素周期表中,某些元素与其右下方的主族元素(如图所示)的一些性质是相似的。如Be与Al的化学性质相似,Be与NaOH溶液反应生成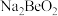 和
和 ,请写出
,请写出 与NaOH溶液反应的离子方程式
与NaOH溶液反应的离子方程式_______ 。
(1)基态硅(Si)原子的核外电子排布式为[Ne]
(2)碳(C)、硅(Si)、锗(Ge)是同族元素。
①C的基态原子核外电子排布式为
②基态Ge原子的核外电子占据
③Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为
④Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是
(3)在元素周期表中,某些元素与其右下方的主族元素(如图所示)的一些性质是相似的。如Be与Al的化学性质相似,Be与NaOH溶液反应生成
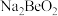 和
和 ,请写出
,请写出 与NaOH溶液反应的离子方程式
与NaOH溶液反应的离子方程式
您最近一年使用:0次
【推荐2】在元素周期表中,某些主族元素与其右下方的主族元素的性质相似的(如锂和镁,铍和铝)。根据周期表对角线规律,金属Be单质及其化合物的性质与铝单质及其化合物的性质相似。
(1)写出BeCl2的电子式___________ 。
(2)下列关于铍及其化合物性质推断正确的是________。
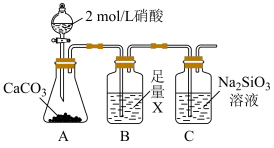
(3)已知H2SiO3是一种白色胶状沉淀,M同学利用下图探究N、C、Si的非金属性大小,试剂X是___________ 。证明三者金属性强弱的实验现象是___________ 。
(1)写出BeCl2的电子式
(2)下列关于铍及其化合物性质推断正确的是________。
| A.可通过氨水与硝酸铍溶液反应制备氢氧化铍 | B.氢氧化铍不能溶于氢氧化钠溶液 |
| C.氯化铍难溶于水 | D.氧化铍的化学式Be2O3 |
(3)已知H2SiO3是一种白色胶状沉淀,M同学利用下图探究N、C、Si的非金属性大小,试剂X是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】回答下列问题
(1)为什么副族元素又称为过渡元素?_______
(2)为什么在元素周期表中非金属元素主要集中在右上角三角区内?处于非金属三角区边缘的元素常被称为半金属或准金属。为什么?_______
(3)在周期表里找出Cr和Cu的价层电子,它们的电子排布符合构造原理吗?此外还有哪些元素的基态原子电子排布不符合构造原理?_______
(4)预言119号元素基态原子最外层电子排布;预言第八周期有多少种元素?_______
(5)对角线规则:元素周期表中的某些主族元素其某些性质与_______ 元素相似。
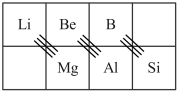
如铍、铝两元素的性质相似性
(1)为什么副族元素又称为过渡元素?
(2)为什么在元素周期表中非金属元素主要集中在右上角三角区内?处于非金属三角区边缘的元素常被称为半金属或准金属。为什么?
(3)在周期表里找出Cr和Cu的价层电子,它们的电子排布符合构造原理吗?此外还有哪些元素的基态原子电子排布不符合构造原理?
(4)预言119号元素基态原子最外层电子排布;预言第八周期有多少种元素?
(5)对角线规则:元素周期表中的某些主族元素其某些性质与

如铍、铝两元素的性质相似性
| 与酸反应 | 与碱反应 | |
| 单质 | ||
| 氧化物 | ||
| 氢氧化物 |
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】2016年9月南开大学学者首次测试了一种新型锌离子电池,该电池以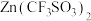 为电解质,用有阳离子型缺陷的
为电解质,用有阳离子型缺陷的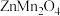 为电极,成功的获得了稳定的大功率电流。
为电极,成功的获得了稳定的大功率电流。
(1)写出基态 原子核外M能层的电子排布式
原子核外M能层的电子排布式_____ 。
(2)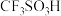 是一种有机强酸,结构式如图所示,通常用
是一种有机强酸,结构式如图所示,通常用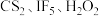 等为主要原料制取。
等为主要原料制取。
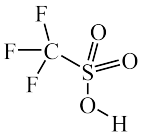
①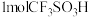 分子中含有的
分子中含有的 键的数目为
键的数目为_____ 。
② 分子中O原子的杂化方式与
分子中O原子的杂化方式与 中硫原子杂化方式
中硫原子杂化方式_____ (填“相同”或“不同”)
③ 难溶于水的原因是
难溶于水的原因是_____ 。与 互为等电子体的一种分子为
互为等电子体的一种分子为_____ 。
④ 遇水完全水解生成两种酸,写出相关化学方程式:
遇水完全水解生成两种酸,写出相关化学方程式:_____ 。
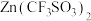 为电解质,用有阳离子型缺陷的
为电解质,用有阳离子型缺陷的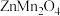 为电极,成功的获得了稳定的大功率电流。
为电极,成功的获得了稳定的大功率电流。(1)写出基态
 原子核外M能层的电子排布式
原子核外M能层的电子排布式(2)
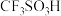 是一种有机强酸,结构式如图所示,通常用
是一种有机强酸,结构式如图所示,通常用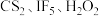 等为主要原料制取。
等为主要原料制取。
①
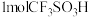 分子中含有的
分子中含有的 键的数目为
键的数目为②
 分子中O原子的杂化方式与
分子中O原子的杂化方式与 中硫原子杂化方式
中硫原子杂化方式③
 难溶于水的原因是
难溶于水的原因是 互为等电子体的一种分子为
互为等电子体的一种分子为④
 遇水完全水解生成两种酸,写出相关化学方程式:
遇水完全水解生成两种酸,写出相关化学方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】[Zn(CN)4]2–在水溶液中与HCHO发生如下反应:4HCHO+[Zn(CN)4]2–+4H++4H2O=[Zn(H2O)4]2++4HOCH2CN
(1)Zn2+基态核外电子排布式为____________________ 。
(2)1 mol HCHO分子中含有σ键的数目为_________ mol。
(3)HOCH2CN分子中碳原子轨道的杂化类型是________ 。
(4)与H2O分子互为等电子体的阴离子为________ 。
(1)Zn2+基态核外电子排布式为
(2)1 mol HCHO分子中含有σ键的数目为
(3)HOCH2CN分子中碳原子轨道的杂化类型是
(4)与H2O分子互为等电子体的阴离子为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】根据信息回答下列问题:
I.元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出10种元素的电负性:
已知:
i.两成键元素间电负性差值大于1.7时,形成离子键;两成键元素间电负性差值小于1.7时,形成共价键。
ii.在水等强极性溶剂中,成键原子电负性的差异是影响化学键断裂难易程度的原因之一。水化物M−O−H结构中,成键原子电负性差异越大,所成化学键越容易断裂,电离出OH−或H+。
(1)通过分析电负性的变化规律,确定Mg元素电负性的最小范围___________ 。
(2)判断下列物质是离子化合物还是共价化合物:
A.Li3N B.BeCl2 C.AlCl3 D.SiC
①属于离子化合物的是___________ (填字母)。
②请设计实验方案证明其为离子化合物___________ 。
(3)HClO水溶液显酸性而不显碱性的依据是___________ 。
II.元素原子的第一电离能I1随原子序数呈周期性变化,请解释:
(4)Na的第一电离能小于Li,从原子结构的角度解释其原因___________ 。
(5)S的第一电离能小于P,结合价电子排布式解释其原因___________ 。
I.元素的电负性和元素的化合价一样,也是元素的一种基本性质。下面给出10种元素的电负性:
| 元素 | Al | Be | Mg | C | Cl | Na | Li | N | Si | O | H |
| 电负性 | 1.5 | 1.5 | 2.5 | 3.0 | 0.9 | 1.0 | 3.0 | 1.8 | 3.5 | 2.1 |
i.两成键元素间电负性差值大于1.7时,形成离子键;两成键元素间电负性差值小于1.7时,形成共价键。
ii.在水等强极性溶剂中,成键原子电负性的差异是影响化学键断裂难易程度的原因之一。水化物M−O−H结构中,成键原子电负性差异越大,所成化学键越容易断裂,电离出OH−或H+。
(1)通过分析电负性的变化规律,确定Mg元素电负性的最小范围
(2)判断下列物质是离子化合物还是共价化合物:
A.Li3N B.BeCl2 C.AlCl3 D.SiC
①属于离子化合物的是
②请设计实验方案证明其为离子化合物
(3)HClO水溶液显酸性而不显碱性的依据是
II.元素原子的第一电离能I1随原子序数呈周期性变化,请解释:
(4)Na的第一电离能小于Li,从原子结构的角度解释其原因
(5)S的第一电离能小于P,结合价电子排布式解释其原因
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】(1)基态硅原子中,电子占据的最高电子层符号为___ ,该电子层具有的原子轨道数为___ 、电子数为___ 。
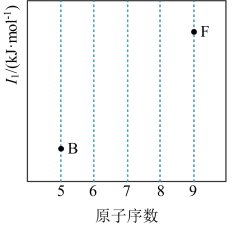
(2)依据第2周期元素第一电离能的变化规律,参照如图B、F元素的位置,用小黑点标出C、N、O三种元素的相对位置___ 。
(3)①N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:578,1817,2745,11578,……则该元素是___ (填元素符号)。
②基态锗(Ge)原子的电子排布式是___ 。Ge的最高价氯化物的分子式是___ 。
(2)依据第2周期元素第一电离能的变化规律,参照如图B、F元素的位置,用小黑点标出C、N、O三种元素的相对位置

(3)①N、Al、Si、Zn四种元素中,有一种元素的电离能数据如下:578,1817,2745,11578,……则该元素是
②基态锗(Ge)原子的电子排布式是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
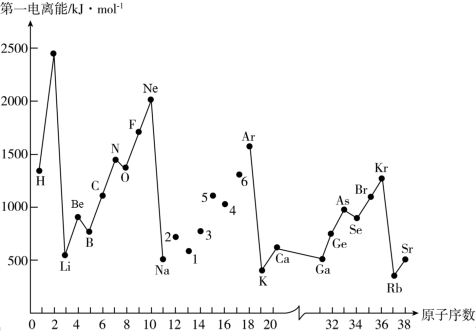
【推荐3】第一电离能I1是指气态原子X(g)失去一个电子成为气态阳离子X+(g)所需的能量。如图是部分元素原子的第一电离能I1随原子序数变化的曲线图。
请回答以下问题:
(1)认真分析图中同周期元素第一电离能的变化规律,将Na—Ar之间六种元素用短线连接起来,构成完整的图象______ 。
(2)从图中分析可知,同一主族元素原子的第一电离能I1变化规律是_______ ;
(3)图中5号元素在周期表中的位置是_________ ;
(4)同周期内,随原子序数增大,I1值增大。但个别元素的I1值出现反常现试预测下列关系式中正确的是_______ 。
①E(砷)>E(硒) ②E(砷)<E(硒) ③E(溴)>E(硒) ④E(溴)<E(硒)

请回答以下问题:
(1)认真分析图中同周期元素第一电离能的变化规律,将Na—Ar之间六种元素用短线连接起来,构成完整的图象
(2)从图中分析可知,同一主族元素原子的第一电离能I1变化规律是
(3)图中5号元素在周期表中的位置是
(4)同周期内,随原子序数增大,I1值增大。但个别元素的I1值出现反常现试预测下列关系式中正确的是
①E(砷)>E(硒) ②E(砷)<E(硒) ③E(溴)>E(硒) ④E(溴)<E(硒)
您最近一年使用:0次

 的价层电子排布式
的价层电子排布式

