回答下列问题:
(1)①下列Li原子电子排布图表示的状态中,能量最低和最高的分别是____ (填标号)。
A、 B、
B、 C、
C、 D、
D、
②Li+与H-具有相同的电子构型,r(Li+)小于r(H-),原因是____
(2)①Zn原子核外电子排布式为____
②黄铜是人类最早使用的合金之一,主要由Zn和Cu组成,第一电离能I1(Zn)___________ I1(Cu)(填“大于”或“小于”)。原因是___________ 。
(3)基态Fe原子价层电子的电子排布图(轨道表达式)为___________ ,基态S原子电子占据最高能级的电子云轮廓图为___________ 形。
(1)①下列Li原子电子排布图表示的状态中,能量最低和最高的分别是
A、
 B、
B、 C、
C、 D、
D、
②Li+与H-具有相同的电子构型,r(Li+)小于r(H-),原因是
(2)①Zn原子核外电子排布式为
②黄铜是人类最早使用的合金之一,主要由Zn和Cu组成,第一电离能I1(Zn)
(3)基态Fe原子价层电子的电子排布图(轨道表达式)为
2021高三·全国·专题练习 查看更多[1]
(已下线)考向36 原子结构与性质-备战2022年高考化学一轮复习考点微专题
更新时间:2021-12-09 07:07:51
|
【知识点】 物质结构与性质综合考查解读
相似题推荐
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐1】镁、铜等金属离子是人体内多种酶的辅因子。工业上从海水中提取镁时,先制备无水氯化镁,然后将其熔融电解,得到金属镁。
(1)以MgCl2为原料用熔融盐电解法制备镁时,常加入NaCl、KCl或CaCl2等金属氯化物,其主要作用除了降低熔点之外还有________ 。
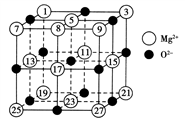
(2)已知MgO的晶体结构属于NaCl型。某同学画出的MgO晶胞结构示意图如图所示,请改正图中错误:__________________ 。
(3)Mg是第三周期元素,该周期部分元素氟化物的熔点见下表:
解释表中氟化物熔点差异的原因:_____________________________________ 。
(1)以MgCl2为原料用熔融盐电解法制备镁时,常加入NaCl、KCl或CaCl2等金属氯化物,其主要作用除了降低熔点之外还有
(2)已知MgO的晶体结构属于NaCl型。某同学画出的MgO晶胞结构示意图如图所示,请改正图中错误:

(3)Mg是第三周期元素,该周期部分元素氟化物的熔点见下表:
| 氟化物 | NaF | MgF2 | SiF4 |
| 熔点/K | 1 266 | 1 534 | 183 |
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
名校
解题方法
【推荐2】回答下列问题:
(1)与 同族且相邻周期的元素
同族且相邻周期的元素 的基态原子价电子排布式为
的基态原子价电子排布式为___________ 。与钛同周期元素的基态原子中,未成对电子数与钛相同的元素有___________ 种。
(2)①基态S原子的价电子中,两种自旋状态的电子数之比为___________ 。
②根据“相似相溶”规律推测硫单质易溶于下列哪些溶剂_________ 。
A.水 B. C.
C.
(3) 分子中B为
分子中B为 杂化,且存在两个硼氧单键,画出
杂化,且存在两个硼氧单键,画出 的结构式
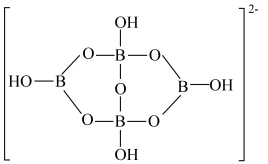
的结构式___________ ,该分子的空间构型为___________ ;硼砂阴离子的结构如图所示,分析B原子的杂化方式为___________ 。
(1)与
 同族且相邻周期的元素
同族且相邻周期的元素 的基态原子价电子排布式为
的基态原子价电子排布式为(2)①基态S原子的价电子中,两种自旋状态的电子数之比为
②根据“相似相溶”规律推测硫单质易溶于下列哪些溶剂
A.水 B.
 C.
C.
(3)
 分子中B为
分子中B为 杂化,且存在两个硼氧单键,画出
杂化,且存在两个硼氧单键,画出 的结构式
的结构式
您最近一年使用:0次
解答题-结构与性质
|
较易
(0.85)
解题方法
【推荐3】铁(Fe)、钴(Co)、镍(Ni)是第四周期第Ⅷ族的元素,在化学上称为铁系元素,其化合物在生产生活中应用广泛。
(1)Fe、Co、Ni位于元素周期表的_______ 区;基态Ni原子核外价层电子的轨道表示式为_______ 。
(2)铁系元素能与CO形成Fe(CO)5、Ni(CO)4等化合物,室温时Ni(CO)4为无色液体,沸点42.1℃,主要用于制高纯镍和催化剂,则Ni(CO)4中所含的化学键类型有_______ (填序号)。
A.离子键 B.极性键 C.配位键 D.范德华力 E.金属键
(3)CoxNi(1-x)Fe2O4(其中Co、Ni的化合价均为+2)在磁性材料和催化剂领域具有广泛的应用,CoxNi(1-x)Fe2O4中Fe的化合价是_______ ;Fe3+比Fe2+更稳定的原因是_______ 。
(4)将1molCoCl3·4NH3溶于水中,加入足量AgNO3溶液生成1molAgCl沉淀。则CoCl3·4NH3中配离子的化学式为_______ ;已知孤电子对与成键电子对的排斥作用大于成键电子对间的排斥作用,则NH3分子与Co3+形成配合物后,H—N—H键角_______ (填“变大”“变小”或“不变”)。
(5)Fe、Co、Ni与Ca元素最外层电子数相同,但相应单质的熔点,Fe、Co、Ni明显高于Ca,其原因_______ 。
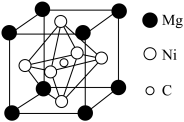
(6)超导材料在电力、交通、医学等方面有着广泛的应用,某含Ni、Mg和C三种元素的晶体具有超导性,该晶体的晶胞结构如图所示。已知该晶胞的边长为anm,阿伏加德罗常数为NA,该晶体的密度为_______ g·cm-3(1nm=10-9m)。
(1)Fe、Co、Ni位于元素周期表的
(2)铁系元素能与CO形成Fe(CO)5、Ni(CO)4等化合物,室温时Ni(CO)4为无色液体,沸点42.1℃,主要用于制高纯镍和催化剂,则Ni(CO)4中所含的化学键类型有
A.离子键 B.极性键 C.配位键 D.范德华力 E.金属键
(3)CoxNi(1-x)Fe2O4(其中Co、Ni的化合价均为+2)在磁性材料和催化剂领域具有广泛的应用,CoxNi(1-x)Fe2O4中Fe的化合价是
(4)将1molCoCl3·4NH3溶于水中,加入足量AgNO3溶液生成1molAgCl沉淀。则CoCl3·4NH3中配离子的化学式为
(5)Fe、Co、Ni与Ca元素最外层电子数相同,但相应单质的熔点,Fe、Co、Ni明显高于Ca,其原因
(6)超导材料在电力、交通、医学等方面有着广泛的应用,某含Ni、Mg和C三种元素的晶体具有超导性,该晶体的晶胞结构如图所示。已知该晶胞的边长为anm,阿伏加德罗常数为NA,该晶体的密度为

您最近一年使用:0次



