实验室用如图所示的仪器药品制取氯化铁粉末,已知氯化铁粉末很容易吸水生成结晶水化合物:FeCl3+6H2O=FeCl3·6H2O。

(1)按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序)①接___________ ,___________ 接___________ ,___________ 接___________ 。
(2)装置A中发生反应的化学方程式是_______ ,还原剂是___________ 。
(3)A、B中的酒精灯应先点燃_______ 处(填“A”或“B”)的酒精灯,理由是_______ 。
(4)这套实验装置是否完整?___________ (填“是”或“否”),若不完整还需补充___________ 装置(若第一问填“是”,则此问不需要作答)。

(1)按照气体流向从左到右顺序连接仪器应是(填仪器接口顺序)①接
(2)装置A中发生反应的化学方程式是
(3)A、B中的酒精灯应先点燃
(4)这套实验装置是否完整?
更新时间:2021-11-11 15:15:23
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】 (易升华、易潮解)是常见的化学试剂。某学习小组开展了与
(易升华、易潮解)是常见的化学试剂。某学习小组开展了与 相关的系列实验,回答下列问题:
相关的系列实验,回答下列问题:
Ⅰ.铁粉制备 (实验装置如图所示)
(实验装置如图所示)
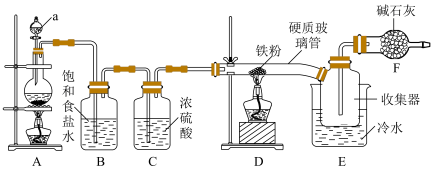
(1)仪器a的名称为_______ 。
(2)制取 的化学方程式为
的化学方程式为_______ 。
(3)饱和食盐水的作用是_______ 。
(4)硬质玻璃管直接接入收集器的优点是_______ 。
(5)碱石灰的主要作用是_______ 。
Ⅱ.探究溶液与Cu的反应。
(6)向 溶液中滴加几滴KSCN溶液,溶液颜色变红,再加入过量Cu粉,发现溶液的红色褪去,用离子方程式解释红色褪去的原因:
溶液中滴加几滴KSCN溶液,溶液颜色变红,再加入过量Cu粉,发现溶液的红色褪去,用离子方程式解释红色褪去的原因:_______ 。
 (易升华、易潮解)是常见的化学试剂。某学习小组开展了与
(易升华、易潮解)是常见的化学试剂。某学习小组开展了与 相关的系列实验,回答下列问题:
相关的系列实验,回答下列问题:Ⅰ.铁粉制备
 (实验装置如图所示)
(实验装置如图所示)
(1)仪器a的名称为
(2)制取
 的化学方程式为
的化学方程式为(3)饱和食盐水的作用是
(4)硬质玻璃管直接接入收集器的优点是
(5)碱石灰的主要作用是
Ⅱ.探究溶液与Cu的反应。
(6)向
 溶液中滴加几滴KSCN溶液,溶液颜色变红,再加入过量Cu粉,发现溶液的红色褪去,用离子方程式解释红色褪去的原因:
溶液中滴加几滴KSCN溶液,溶液颜色变红,再加入过量Cu粉,发现溶液的红色褪去,用离子方程式解释红色褪去的原因:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】实验室里除了用二氧化锰和浓盐酸加热制取氯气,也可以利用反应:2KMnO4+16HCl(浓)=2KCl+2MnC12+5Cl2↑+8H2O制取并收集纯净、干燥的氯气,部分装置如图所示:
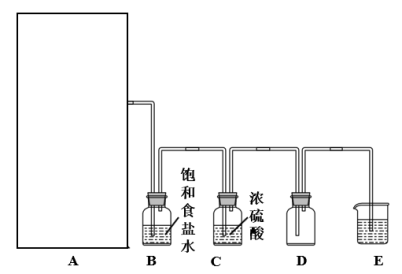
(1)若以KMnO4和浓盐酸为原料制取氯气,请根据反应原理从图中选择合适的制气装置___ (填代号)。
a.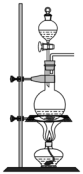 b.
b.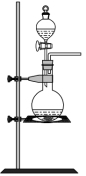 c.
c.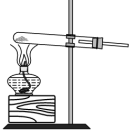
(2)装置B的作用___ 。
(3)E中的试剂选最好的是___ 。
A.NaOH溶液 B.NaCl溶液 C.Na2CO3溶液 D.水

(1)若以KMnO4和浓盐酸为原料制取氯气,请根据反应原理从图中选择合适的制气装置
a.
 b.
b. c.
c.
(2)装置B的作用
(3)E中的试剂选最好的是
A.NaOH溶液 B.NaCl溶液 C.Na2CO3溶液 D.水
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】实验Ⅰ:下图1为实验室制取氨的实验装置。

(1)写出A中所发生反应的化学方程式____________________________________ 。
(2)在收集氨时试管口棉花的作用是______________________________________ 。
(3)另一学生积极思考产生喷泉的其他方法,设计了图3装置。首先在锥形瓶中分别加入足量的下列物质,反应后产生喷泉的是( )
A.CaCO3粉末和浓盐酸 B.锌粒和稀硫酸 C.稀盐酸和AgNO3溶液
(4)该同学又向锥形瓶中加入酒精,水槽中加入冷水后,再加入足量的下列物质,结果也产生了喷泉。水槽中加入的物质可以是( )
A.生石灰 B.食盐 C.浓硫酸
实验Ⅱ:为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为橙黄色时,夹紧弹簧夹。
Ⅲ.当B中橙黄色溶液颜色变深时,关闭活塞a。
Ⅳ. 打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡。
(1)A中产生黄绿色气体,其化学方程式是__________________
(2)B中溶液发生反应的离子方程式是____________________
(3)过程Ⅳ的目的为______________
(4)D中出现的现象为____________________________
(5)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下_______ ,得电子能力逐渐减弱。

(1)写出A中所发生反应的化学方程式
(2)在收集氨时试管口棉花的作用是
(3)另一学生积极思考产生喷泉的其他方法,设计了图3装置。首先在锥形瓶中分别加入足量的下列物质,反应后产生喷泉的是
A.CaCO3粉末和浓盐酸 B.锌粒和稀硫酸 C.稀盐酸和AgNO3溶液
(4)该同学又向锥形瓶中加入酒精,水槽中加入冷水后,再加入足量的下列物质,结果也产生了喷泉。水槽中加入的物质可以是
A.生石灰 B.食盐 C.浓硫酸
实验Ⅱ:为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。

实验过程:
Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。
Ⅱ.当B和C中的溶液都变为橙黄色时,夹紧弹簧夹。
Ⅲ.当B中橙黄色溶液颜色变深时,关闭活塞a。
Ⅳ. 打开活塞b,将少量C中溶液滴入D中,关闭活塞b,取下D振荡。
(1)A中产生黄绿色气体,其化学方程式是
(2)B中溶液发生反应的离子方程式是
(3)过程Ⅳ的目的为
(4)D中出现的现象为
(5)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室中某学习小组利用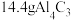 与足量的S制取
与足量的S制取 并进行提纯,装置如下:
并进行提纯,装置如下:

已知:①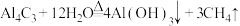
②
回答下列问题:
(1)装置甲虚线内加入 所需仪器名称为
所需仪器名称为_____ 。
(2)装置乙中的试剂为_____ ;实验开始时,首先点燃装置甲处的酒精灯,其目的是_____ 。
(3)装置丙中发生反应生成的气体为_____ ;装置丁中冰水的作用是_____ 。
(4)装置戊中发生反应的离子反应方程式为_____ 。
(5)依次用 、
、 、
、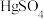 处理收集到的
处理收集到的 粗品后,再向获得的有机层加入
粗品后,再向获得的有机层加入 后进行分离操作,该操作的名称为
后进行分离操作,该操作的名称为_____ ,最终获得精品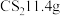 。则
。则 的产率为
的产率为_____ 。
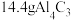 与足量的S制取
与足量的S制取 并进行提纯,装置如下:
并进行提纯,装置如下:
已知:①
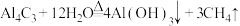
②
| 物质 | 熔点 | 沸点 | 溶解性 |
 |  | 46℃ | 不溶于水 |
| S | 118℃ | 445℃ | 不溶于水,易溶于 |
(1)装置甲虚线内加入
 所需仪器名称为
所需仪器名称为(2)装置乙中的试剂为
(3)装置丙中发生反应生成的气体为
(4)装置戊中发生反应的离子反应方程式为
(5)依次用
 、
、 、
、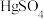 处理收集到的
处理收集到的 粗品后,再向获得的有机层加入
粗品后,再向获得的有机层加入 后进行分离操作,该操作的名称为
后进行分离操作,该操作的名称为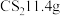 。则
。则 的产率为
的产率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】以重晶石(主要成分是BaSO4,含Al、Fe等元素的杂质)为原料制备产品(BaCl2·2H2O)的一种流程如下:

已知:滤液2主要含BaCl2,还含有AlCl3、FeCl3和HCl等杂质。298K下,Fe(OH)3、Al(OH)3完全沉淀的pH依次为3.0和5.4。
回答下列问题:
(1)高温焙烧时将重晶石粉碎的目的是______________________ 。若4.66 g BaSO4完全反应转移9.632×1022个电子,写出BaSO4与C反应的化学方程式:______________________ 。
(2)“固体”(微溶于水)与盐酸反应生成的一种气体通入CuSO4溶液中产生黑色沉淀,则生成该气体的离子方程式为______________________ 。滤渣3的成分是___________ (填化学式)。
(3)加入BaCO3的目的是____________________________________________ 。
(4)常温下,Fe3+沉淀完全[溶液中c(Fe3+)=1×10-5mol·L-1]时溶液的pH=3,则Fe(OH)3的Ksp约为_____ 。
(5)滤液4经蒸发浓缩、降温结晶、过滤,洗涤和干燥,得到产品。采用电化学法以过滤后的废液为原料制备Ba(OH)2,实现资源综合利用和环境保护。气体X的电子式为____________________ ;写出阴极的电极反应式:__________________ 。

已知:滤液2主要含BaCl2,还含有AlCl3、FeCl3和HCl等杂质。298K下,Fe(OH)3、Al(OH)3完全沉淀的pH依次为3.0和5.4。
回答下列问题:
(1)高温焙烧时将重晶石粉碎的目的是
(2)“固体”(微溶于水)与盐酸反应生成的一种气体通入CuSO4溶液中产生黑色沉淀,则生成该气体的离子方程式为
(3)加入BaCO3的目的是
(4)常温下,Fe3+沉淀完全[溶液中c(Fe3+)=1×10-5mol·L-1]时溶液的pH=3,则Fe(OH)3的Ksp约为
(5)滤液4经蒸发浓缩、降温结晶、过滤,洗涤和干燥,得到产品。采用电化学法以过滤后的废液为原料制备Ba(OH)2,实现资源综合利用和环境保护。气体X的电子式为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某兴趣小组在实验室使用多孔硫颗粒作催化剂,将一氯乙酸( )转化为应用更广泛的三氯乙酸(
)转化为应用更广泛的三氯乙酸(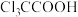 )。主要反应方程式:
)。主要反应方程式: 。制备装置如图所示(部分夹持装置和加热装置已省略)。
。制备装置如图所示(部分夹持装置和加热装置已省略)。
(1)仪器X的名称为______ ,冷凝水的进水口为______ (填“a”或“b”)。
(2)检查虚线框内装置的气密性方法为______ 。
(3)装置甲中制取 的离子方程式为
的离子方程式为______ ,装置戊的作用是______ 。
(4)制备三氯乙酸时,需要控制温度在140℃左右持续加热,则丁的加热方法是______ (填“水浴加热”或“油浴加热”),该过程中不需要另加沸石,原因是______ 。
(5)已知 ,常温下
,常温下 、
、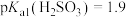 、
、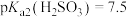 ,则在
,则在 溶液中加入足量的
溶液中加入足量的 ,发生反应的离子方程式为
,发生反应的离子方程式为______ 。
 )转化为应用更广泛的三氯乙酸(
)转化为应用更广泛的三氯乙酸(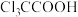 )。主要反应方程式:
)。主要反应方程式: 。制备装置如图所示(部分夹持装置和加热装置已省略)。
。制备装置如图所示(部分夹持装置和加热装置已省略)。
(1)仪器X的名称为
(2)检查虚线框内装置的气密性方法为
(3)装置甲中制取
 的离子方程式为
的离子方程式为(4)制备三氯乙酸时,需要控制温度在140℃左右持续加热,则丁的加热方法是
(5)已知
 ,常温下
,常温下 、
、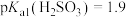 、
、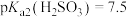 ,则在
,则在 溶液中加入足量的
溶液中加入足量的 ,发生反应的离子方程式为
,发生反应的离子方程式为
您最近一年使用:0次



