铝是重要的金属材料,铝土矿(主要成分是Al2O3和少量的SiO2、Fe2O3杂质)是工业上制取铝的原料。实验室模拟工业上以铝土矿为原料制取Al2(SO4)3和铵明矾晶体[NH4Al(SO4)2•12H2O]的工艺流程如图所示:
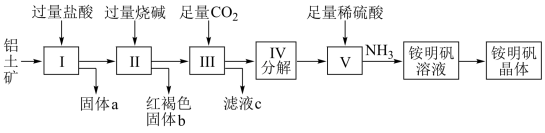
请回答下列问题:
(1)固体a的化学式为_______ 。
(2)加快I的反应速率的措施有_______ (任写两点即可)。
(3)写出II中加过量的烧碱涉及的反应离子方程式:_______ ;III中通入足量CO2气体发生反应的离子方程式为_______ 。
(4)由I中得到固体a的实验操作为_______ ,从铵明矾溶液中获得铵明矾晶体的实验操作依次为(填操作名称)_______ 、_______ 、过滤、洗涤。
(5)向铵明矾NH4Al(SO4)2中加氢氧化钡使硫酸根离子刚好完全沉淀的化学反应方程式为_______ 。

请回答下列问题:
(1)固体a的化学式为
(2)加快I的反应速率的措施有
(3)写出II中加过量的烧碱涉及的反应离子方程式:
(4)由I中得到固体a的实验操作为
(5)向铵明矾NH4Al(SO4)2中加氢氧化钡使硫酸根离子刚好完全沉淀的化学反应方程式为
更新时间:2021-12-16 16:46:20
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】铬及其化合物常被应用于冶金、化工、电镀、制药、纺织等行业,但使用后的废水因其中含高价铬的化合物而毒性很强,必须进行处理。
工业上往往采取下列循环工艺防止铬的污染:

(1)上述各步反应中属于氧化还原反应的是___________ (填序号)。
(2)第①步,含 的废水在酸性条件下用绿矾FeSO4·7H2O处理,写出并配平反应的离子方程式:
的废水在酸性条件下用绿矾FeSO4·7H2O处理,写出并配平反应的离子方程式:___________ 。
(3)第②步,向上述反应后的溶液中加入适量的碱石灰,使铬离子转变为Cr(OH)3沉淀。处理后,沉淀物中除了Cr(OH)3外,还有___________ 、___________ (写化学式)。已知Cr(OH)3性质类似Al(OH)3,是既能与强酸反应又能与强碱反应的两性物质,写出从该沉淀物中分离出Cr(OH)3的离子方程式:___________ 。
(4)回收所得的Cr(OH)3,经③④⑤步处理后又可转变成K2Cr2O7。纯净的K2Cr2O7常用于准确测定Na2S2O3溶液的物质的量浓度,方法如下:
① +6I-+14H+ =3I2+2Cr3++7H2O
+6I-+14H+ =3I2+2Cr3++7H2O
②2S2O +I2 =
+I2 = +2I-
+2I-
准确称取纯净的K2Cr2O7 0.122 5 g,配成溶液,用上述方法滴定,消耗Na2S2O3溶液25.00 mL。则Na2S2O3溶液的物质的量浓度为___________ (保留四位有效数字)。
工业上往往采取下列循环工艺防止铬的污染:

(1)上述各步反应中属于氧化还原反应的是
(2)第①步,含
 的废水在酸性条件下用绿矾FeSO4·7H2O处理,写出并配平反应的离子方程式:
的废水在酸性条件下用绿矾FeSO4·7H2O处理,写出并配平反应的离子方程式:(3)第②步,向上述反应后的溶液中加入适量的碱石灰,使铬离子转变为Cr(OH)3沉淀。处理后,沉淀物中除了Cr(OH)3外,还有
(4)回收所得的Cr(OH)3,经③④⑤步处理后又可转变成K2Cr2O7。纯净的K2Cr2O7常用于准确测定Na2S2O3溶液的物质的量浓度,方法如下:
①
 +6I-+14H+ =3I2+2Cr3++7H2O
+6I-+14H+ =3I2+2Cr3++7H2O②2S2O
 +I2 =
+I2 = +2I-
+2I-准确称取纯净的K2Cr2O7 0.122 5 g,配成溶液,用上述方法滴定,消耗Na2S2O3溶液25.00 mL。则Na2S2O3溶液的物质的量浓度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】在盛有AgNO3、HCl、Na2CO3、CaCl2、NaCl五种无色溶液的试剂瓶上,分别贴有①~⑤的编号。将它们两两混合,产生的现象如表所列(其中“↑”表示产生气体,“↓”表示生成沉淀,“-”表示无现象):

(1)写出③、④、⑤三种物质的化学式为:③______ ,④________ ,⑤_______ 。
(2)写出下列反应的离子方程式:①+②___________ 。

(1)写出③、④、⑤三种物质的化学式为:③
(2)写出下列反应的离子方程式:①+②
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】化合物A由两种元素组成,是一种重要的还原剂,在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3)。将4.80g化合物A隔绝空气加热至完全分解,得到金属单质X和2.24L的气体Y;所得单质X与水反应又得到2.24L气体Y和强碱溶液Z(气体体积均已折算为标准状况)。回答下列问题:
(1)气体Y的分子式为_______ 。
(2)单质X与水反应的离子方程式_______ 。
(3)化合物A在钢铁制品脱锈过程发生反应的化学方程式_______ 。
(4)化合物A化学活性很高,在潮湿空气中能自燃。若着火,_______ (填“能”或“不能”)用二氧化碳灭火;若不能,写出原因_______ (用化学方程式表示)。
(1)气体Y的分子式为
(2)单质X与水反应的离子方程式
(3)化合物A在钢铁制品脱锈过程发生反应的化学方程式
(4)化合物A化学活性很高,在潮湿空气中能自燃。若着火,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】工业上用铝土矿(主要成分Al2O3、Fe2O3、SiO2)提取氧化铝作冶炼铝的原料,提取的操作过程如下:

(1)写出步骤①中所发生反应的化学方程式____
(2)沉淀1是_________ (写化学式);沉淀2是________ (写化学式)。
(3)写出步骤②中所发生反应的离子方程式__________
(4)用氧化铝冶炼铝的化学方程式是______
(5)请设计另一个实验方案提取氧化铝________

(1)写出步骤①中所发生反应的化学方程式
(2)沉淀1是
(3)写出步骤②中所发生反应的离子方程式
(4)用氧化铝冶炼铝的化学方程式是
(5)请设计另一个实验方案提取氧化铝
您最近一年使用:0次
【推荐2】硫酸镍是一种重要的化工中间体,是镍行业研究的热点。一种以石油化工中的废镍催化剂(主要成分为NiCO3和SiO2,还含有少量Fe2O3、Cr2O3)为原料制备硫酸镍的工业流程如下:
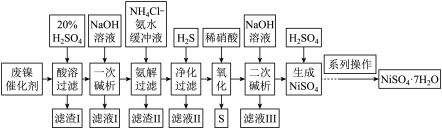
已知:Ⅰ. NiS、Ni(OH)2、Cr(OH)3均难溶于水,Cr(OH)3是两性氢氧化物;
Ⅱ. Fe(OH)3不溶于NH4Cl—氨水的混合液,Ni(OH)2溶于NH4Cl—氨水的混合液生成[Ni(NH3)6]2+。
请回答下列问题:
(1)“酸溶”时应先将废镍催化剂粉碎,再与20%硫酸在100℃下反应2h,该操作的目的为____ 。
(2)“滤渣I”主要成分在工业上的用途为_______ (只写1种即可),NH4Cl的电子式为_______ 。
(3)“一次碱析”时,加入的NaOH溶液需过量,含铬微粒发生反应的离子方程式为________ 。
(4)“氨解”的目的为_____________________ 。
(5)“氧化”时发生反应的离子方程式为___________________________ 。
(6)“二次碱浸”时,若使溶液中的Ni2+沉淀完全,则需维持c(OH-)不低于__________ 。(已知Ni(OH)2的Ksp=2×10-15, ≈1.4)。
≈1.4)。
(7)“系列操作”具体是指____________ 、过滤、洗涤、干燥。若所得NiSO4·7H2O晶体不纯,应继续进行的提纯操作名称为____________ 。

已知:Ⅰ. NiS、Ni(OH)2、Cr(OH)3均难溶于水,Cr(OH)3是两性氢氧化物;
Ⅱ. Fe(OH)3不溶于NH4Cl—氨水的混合液,Ni(OH)2溶于NH4Cl—氨水的混合液生成[Ni(NH3)6]2+。
请回答下列问题:
(1)“酸溶”时应先将废镍催化剂粉碎,再与20%硫酸在100℃下反应2h,该操作的目的为
(2)“滤渣I”主要成分在工业上的用途为
(3)“一次碱析”时,加入的NaOH溶液需过量,含铬微粒发生反应的离子方程式为
(4)“氨解”的目的为
(5)“氧化”时发生反应的离子方程式为
(6)“二次碱浸”时,若使溶液中的Ni2+沉淀完全,则需维持c(OH-)不低于
 ≈1.4)。
≈1.4)。(7)“系列操作”具体是指
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】某工厂从含硫酸钡、氧化铜、氧化亚铁、氧化铝和少量氧化银的废渣中回收金属的工艺流程如图所示:

(1)滤渣①的化学式为___________ ,是___________ (填“强”“弱”或“非”)电解质。
(2)用滤渣②作粗铜电解精炼铜时,粗铜作___________ (填“阳”或“阴”)极。
(3)加入过量铁粉,被还原的金属阳离子有___________ 。过氧化钠的电子式为___________ 。
(4)滤液④的溶质是___________ 。B电解方程式为___________ 。
(5)写出滤渣③生成A的化学方程式:___________ 。

(1)滤渣①的化学式为
(2)用滤渣②作粗铜电解精炼铜时,粗铜作
(3)加入过量铁粉,被还原的金属阳离子有
(4)滤液④的溶质是
(5)写出滤渣③生成A的化学方程式:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】近日,科学家利用光催化剂 实现高选择性制备氢气。某小组以辉铋矿(主要成分是
实现高选择性制备氢气。某小组以辉铋矿(主要成分是 ,含少量
,含少量 、Bi、
、Bi、 和
和 等杂质)为原料制备钒酸铋(
等杂质)为原料制备钒酸铋( )的流程如下:
)的流程如下:

已知:
①滤液1中所含阳离子主要有 、
、 、
、 和
和 。
。
②几种氢氧化物沉淀的pH如表所示。
回答下列问题:
(1)滤渣2的主要成分是_______ (填化学式)。将辉铋矿粉碎过筛制成矿粉,其目的是_______ 。
(2)“酸洗”中用盐酸代替水的目的是_______ 。滤液3可以循环用于“_______ ”工序(填名称)。
(3)“氯化”的化学方程式为_______ 。
(4)“合成”过程中将 溶液和
溶液和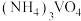 溶液混合容易形成
溶液混合容易形成 胶体,导致过滤困难。为防止生成胶体可采用的措施为
胶体,导致过滤困难。为防止生成胶体可采用的措施为_______ (任答一条)。
(5)已知辉铋矿中所含Bi元素的质量分数为a%,wt这种矿石经上述转化最终制得b kg ,则铋的收率为
,则铋的收率为_______ %( )。
)。
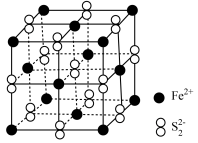
(6) 的立方晶胞结构如图所示。已知晶体密度为
的立方晶胞结构如图所示。已知晶体密度为 ,设
,设 为阿伏加德罗常数的值,则该晶体中与
为阿伏加德罗常数的值,则该晶体中与 距离最近且相等的
距离最近且相等的 有
有_______ 个,相邻2个 的核间距为
的核间距为_______ nm。
 实现高选择性制备氢气。某小组以辉铋矿(主要成分是
实现高选择性制备氢气。某小组以辉铋矿(主要成分是 ,含少量
,含少量 、Bi、
、Bi、 和
和 等杂质)为原料制备钒酸铋(
等杂质)为原料制备钒酸铋( )的流程如下:
)的流程如下:
已知:
①滤液1中所含阳离子主要有
 、
、 、
、 和
和 。
。②几种氢氧化物沉淀的pH如表所示。
| 氢氧化物 |  |  |  |
| 开始沉淀pH | 7.5 | 2.3 | 4.0 |
| 沉淀完全pH | 9.7 | 3.7 |
(1)滤渣2的主要成分是
(2)“酸洗”中用盐酸代替水的目的是
(3)“氯化”的化学方程式为
(4)“合成”过程中将
 溶液和
溶液和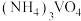 溶液混合容易形成
溶液混合容易形成 胶体,导致过滤困难。为防止生成胶体可采用的措施为
胶体,导致过滤困难。为防止生成胶体可采用的措施为(5)已知辉铋矿中所含Bi元素的质量分数为a%,wt这种矿石经上述转化最终制得b kg
 ,则铋的收率为
,则铋的收率为 )。
)。(6)
 的立方晶胞结构如图所示。已知晶体密度为
的立方晶胞结构如图所示。已知晶体密度为 ,设
,设 为阿伏加德罗常数的值,则该晶体中与
为阿伏加德罗常数的值,则该晶体中与 距离最近且相等的
距离最近且相等的 有
有 的核间距为
的核间距为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】钼酸钠晶体(Na2MoO4·2H2O)可抑制金属腐蚀。以钼精矿(主要成分为MoS2,含少量杂质)为原料,制备钼酸钠晶体的主要流程图如下。
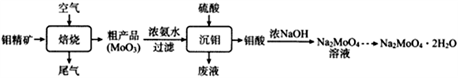
回答下列问题
(1)完成下列反应:_____ MoS2+ _____O2 _____SO2+ _____MoO3
_____SO2+ _____MoO3
在焙烧炉中,空气从炉底进入矿石经粉碎后从炉顶进入,这样处理的目的是__________________ 。
(2)浓氨水浸取粗产品获得(NH4)2MoO4溶液,其化学反应方程式为____________________________ ;该反应说明MoO3______ (填“有”或“没有”)酸性氧化物的性质。
(3)常温下,沉钼阶段所得废液为(NH4)2SO4稀溶液。若(NH4)2SO4稀溶液的pH=a,则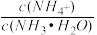 =
=_______ (用含a的代数式表示,NH3·H2O的Kb=1.8×10-5),若将此稀溶液蒸发浓缩,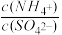 将
将_________ (填“变大”“不变”或“变小”)。
(4)已知钼酸钠在一定温度范围内的析出物质及相应物质的溶解度如下表所示,获得Na2MoO4·2H2O的操作为_____________ 。
结晶得到的母液可以在下次结晶时重复使用,但达到一定次数后必须净化处理,原因是_____________ 。
(5)空气中钼酸盐对碳钢的缓蚀原理是在钢铁表面形成FeMoO4-Fe2O3保护膜,在密闭式循环冷却水系统中的碳钢管道缓蚀,除需加入钼酸盐外还需加入的物质是___________ (填选项字母)。
A. NaNO2 B.通入适量N2 C.油脂 D.盐酸

回答下列问题
(1)完成下列反应:
 _____SO2+ _____MoO3
_____SO2+ _____MoO3在焙烧炉中,空气从炉底进入矿石经粉碎后从炉顶进入,这样处理的目的是
(2)浓氨水浸取粗产品获得(NH4)2MoO4溶液,其化学反应方程式为
(3)常温下,沉钼阶段所得废液为(NH4)2SO4稀溶液。若(NH4)2SO4稀溶液的pH=a,则
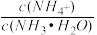 =
=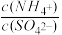 将
将(4)已知钼酸钠在一定温度范围内的析出物质及相应物质的溶解度如下表所示,获得Na2MoO4·2H2O的操作为
| 温度(℃) | 0 | 4 | 9 | 10 | 15.5 | 32 | 51.5 | 100 |
| 析出物质 | Na2MoO4·10H2O | Na2MoO4·2H2O | ||||||
| 溶解度 | 30.63 | 33.85 | 38.16 | 39.28 | 39.27 | 39.82 | 41.27 | 45. |
(5)空气中钼酸盐对碳钢的缓蚀原理是在钢铁表面形成FeMoO4-Fe2O3保护膜,在密闭式循环冷却水系统中的碳钢管道缓蚀,除需加入钼酸盐外还需加入的物质是
A. NaNO2 B.通入适量N2 C.油脂 D.盐酸
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】CuCl2是常见的化学试剂,某学习小组利用废铜屑“湿法”制备CuCl2·2H2O。
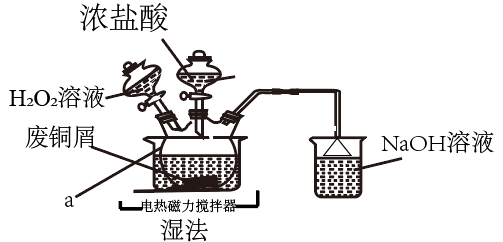
氯化铜在不同温度下结晶形成的结晶水合物
回答下列问题:
(1)仪器 的名称为
的名称为___________ , 溶液的作用是
溶液的作用是___________ 。
(2)“湿法”制备 的离子方程式为
的离子方程式为___________ ,实验中, 的实际用量要大于理论用量,原因是
的实际用量要大于理论用量,原因是___________ 。
(3)为得到纯净的 晶体,反应完全后要进行的操作是:除去其他可能的金属离子后,过滤,向滤液中持续通入
晶体,反应完全后要进行的操作是:除去其他可能的金属离子后,过滤,向滤液中持续通入 气体,加热蒸发浓缩,
气体,加热蒸发浓缩,___________ ,过滤,洗涤,低温干燥。其中,持续通入 的作用是
的作用是___________ 。
(4)用“间接碘量法”测定 废铜屑的利用率。取所得试样溶于水配成
废铜屑的利用率。取所得试样溶于水配成 ,取出
,取出 ,向其中加入过量
,向其中加入过量 固体,充分反应,生成白色
固体,充分反应,生成白色 沉淀,滴入几滴淀粉溶液作指示剂,用
沉淀,滴入几滴淀粉溶液作指示剂,用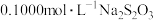 标准溶液滴定,到达滴定终点时,消耗
标准溶液滴定,到达滴定终点时,消耗 标准溶液
标准溶液 。(涉及到的反应为:
。(涉及到的反应为: ,
, )
)
①滴定终点的判断:当滴入最后一滴标准液,溶液恰好___________ (填颜色变化),且半分钟不再发生变化。
②废铜屑中铜的百分含量为___________ 。
(5)查阅资料: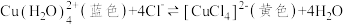 ,等量黄色与蓝色混合呈绿色。设计实验证明
,等量黄色与蓝色混合呈绿色。设计实验证明 溶液中存在上述平衡;取少量蓝色
溶液中存在上述平衡;取少量蓝色 稀溶液于试管中,
稀溶液于试管中,___________ 。

氯化铜在不同温度下结晶形成的结晶水合物
| 温度 | 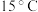 以下 以下 | 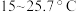 |  |  以上 以上 |
| 结晶水合物 | 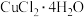 |  |  | 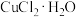 |
(1)仪器
 的名称为
的名称为 溶液的作用是
溶液的作用是(2)“湿法”制备
 的离子方程式为
的离子方程式为 的实际用量要大于理论用量,原因是
的实际用量要大于理论用量,原因是(3)为得到纯净的
 晶体,反应完全后要进行的操作是:除去其他可能的金属离子后,过滤,向滤液中持续通入
晶体,反应完全后要进行的操作是:除去其他可能的金属离子后,过滤,向滤液中持续通入 气体,加热蒸发浓缩,
气体,加热蒸发浓缩, 的作用是
的作用是(4)用“间接碘量法”测定
 废铜屑的利用率。取所得试样溶于水配成
废铜屑的利用率。取所得试样溶于水配成 ,取出
,取出 ,向其中加入过量
,向其中加入过量 固体,充分反应,生成白色
固体,充分反应,生成白色 沉淀,滴入几滴淀粉溶液作指示剂,用
沉淀,滴入几滴淀粉溶液作指示剂,用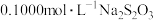 标准溶液滴定,到达滴定终点时,消耗
标准溶液滴定,到达滴定终点时,消耗 标准溶液
标准溶液 。(涉及到的反应为:
。(涉及到的反应为: ,
, )
)①滴定终点的判断:当滴入最后一滴标准液,溶液恰好
②废铜屑中铜的百分含量为
(5)查阅资料:
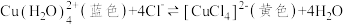 ,等量黄色与蓝色混合呈绿色。设计实验证明
,等量黄色与蓝色混合呈绿色。设计实验证明 溶液中存在上述平衡;取少量蓝色
溶液中存在上述平衡;取少量蓝色 稀溶液于试管中,
稀溶液于试管中,
您最近一年使用:0次



